
科目: 来源: 题型:
【题目】Ⅰ.A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:

(1)若A的溶液能使淀粉溶液变蓝,C为非金属氧化物,能使品红溶液褪色,该反应的离子方程式为____________________________________。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行。写出C溶液呈强碱性时反应的离子方程式:_____________________________。
(3)若A、C均为化合物,E为白色沉淀(不含金属元素),C为引起温室效应的主要气体,则该反应的离子方程式为__________________________________。
Ⅱ. FeCl3可用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(4)将标准状况下a L氯化氢气体溶于1000g水中得到盐酸,若该盐酸的密度为b g·mL-1,则该盐酸的物质的量浓度是____________________。
(5)向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为____________。
(6)用100 mL 2 mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数_____0.2NA (填“大于”“等于”或“小于”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
[查阅资料] ①BCl3的熔点为-107.3 ℃,沸点为12.5 ℃;②2B+6HCl![]() 2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
[设计实验] 某同学设计如图所示装置制备三氯化硼:

请回答下列问题:
(1)常温下,可用高锰酸钾与浓盐酸发生的反应可替代A装置中的反应,请写出高锰酸钾与浓盐酸反应的离子方程式:_______________________________________________。
(2)E装置的作用是________________________________。如果拆去B装置,可能的后果是______________________________________________________________________。
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式______________________________________________________。实验室保存三氯化硼的注意事项是___________________________________。
(4)实验中可以用一个盛装____________________(填试剂名称)的干燥管代替F和G装置,使实验更简便。
(5)为了顺利完成实验,正确的操作是_____(填序号)。
①先点燃A处酒精灯,后点燃D处酒精灯 ②同时点燃A、D处酒精灯 ③先点燃D处酒精灯,后点燃A处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓________________(填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)每消耗8g CH4转移的电子的数目为________________。
(2)已知:①2CO(g)+O2(g)=2CO2(g) △H1=akJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g)△H2=bkJ·mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=ckJ·mol-1
④CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H4
CO(g)+3H2(g) △H4
由此计算△H4=_____________kJ·mol-1。
(3)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时,c(CH4)=0.5mol·L-1。
CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时,c(CH4)=0.5mol·L-1。
①0~tmin内,该反应的平均反应速率v(H2)=___________。
②T℃时,该反应的甲烷的转化率是_________。
③下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(CH4):v(H2) =1:3 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n molH2O的同时,生成3n mol H2 f.单位时间内4mol C—H键断裂的同时2mol O—H键也断裂
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法或表示法正确的是
A. 氢气与氧气反应生成等量的水蒸气和液态水,前者放出热量多
B. 需要加热的反应说明它是吸热反应
C. 在稀溶液中:H+(aq)+OH-(aq) =H2O(l) ΔH=-57.3 kj/mol,若将含0.5 mol H2SO4 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D. 由N2O4(g) ![]() 2NO2(g) △H=-56.9 kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ
2NO2(g) △H=-56.9 kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ
查看答案和解析>>
科目: 来源: 题型:
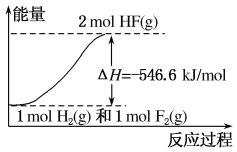
【题目】已知:H2(g)+F2(g)===2HF(g) ΔH=-546.6 kJ/mol,下列说法正确的是 ( )
A. 氟化氢气体分解生成氢气和氟气的反应是放热反应
B. 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于546.6 kJ
C. 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF的能量
D. 该反应中的能量变化可用如图来表示
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以浓缩海水为原料提取溴的部分流程如右图:下列说法正确的是
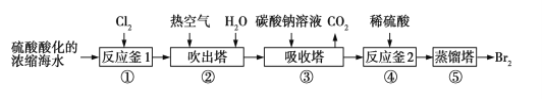
A. 海水需要浓缩,是因为海水中的Br2含量较低
B. 热空气的作用是将多余的Cl2吹出
C. 吸收塔中发生的反应是3Br2+3CO32-=5Br-+BrO3-+3CO2↑
D. 反应釜2中发生的反应是5Br-+BrO3-+3H2O=3Br2+6OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、乙酸,D中放有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成微溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用为__________,圆底烧瓶中发生的化学反应方程式:_________。
(2)球形干燥管C的作用是_________,反应结束后D中的现象是_______________。
(3)该小组同学在实验时加入过量的乙醇,目的是_________________。
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出____________;再加入(此空从下列选项中选择)________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
查看答案和解析>>
科目: 来源: 题型:
【题目】镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高且平稳,因此镁电池越来越成为人们研制绿色电池的焦点。其中一种镁电池的反应:为:xMg+Mo3S4![]() MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
A. Mg2+向正极迁移 B. 正极反应为:Mo3S4+2xe-═Mo3S42x-
C. Mo3S4发生氧化反应 D. 负极反应为:xMg-2xe-═xMg2+
查看答案和解析>>
科目: 来源: 题型:
【题目】利用反应6NO2+8NH3===7N2+12H2O构成电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。下列说法正确的是()

A. 电流从左侧电极经过负载后流向右侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为2NH3-6e-===N2+6H+
D. 当有4.48 L NO2被处理时,转移电子数为0.8NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)请写出硬质玻璃管中发生的化学反应方程式______________________。
(2)甲处需要采用水浴加热,目的是_______________________________。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是___________;集气瓶中收集到的气体的主要成分是__________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有_____。要除去该物质,可先在混合液中加入_______ (填写字母),然后再通过蒸馏即可除去。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com