
科目: 来源: 题型:
【题目】已知液氨的性质与水相似。T℃时,NH3+NH3![]() NH4++NH2-,NH4+的平衡浓度为1×10-15mol/L,则下列说法中正确的是( )
NH4++NH2-,NH4+的平衡浓度为1×10-15mol/L,则下列说法中正确的是( )
A. 在此温度下液氨的离子积为1×10-17
B. 在液氨中放入金属钠,可生成NaNH2
C. 恒温下,在液氨中加入NH4Cl,可使液氨的离子积减小
D. 降温,可使液氨电离平衡逆向移动,且c(NH4+)<c(NH2-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应的离子方程式中正确的是( )
A. 盐酸与碳酸钡反应:CO32-+2H+ = CO2↑+H2O
B. 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++SO42-= BaSO4↓
C. 澄清石灰水与少量小苏打溶液混合:Ca2+ + OH-+ HCO3-= CaCO3↓ + H2O
D. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,浓度均为 0.10 mol/L,体积均为 V0 的 MOH 和ROH 溶液,分别加水稀释至体积 V,pH 随![]() 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

A. 稀释前两溶液的 Ka : MOH 溶液>ROH 溶液
B. ROH 的电离程度:b 点小于 a 点
C. 两溶液在稀释过程中,c(H+)均逐渐减少
D. 当![]() 时,若两溶液同时升高温度,则c(R+)/c(M+)增大
时,若两溶液同时升高温度,则c(R+)/c(M+)增大
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步骤1:将铜粉加入稀盐酸中,并持续通空气反应生成CuCl2。已知Fe3+对该反应有催化作用,其催化原理如下图所示。步骤2:在制得的CuCl2溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。
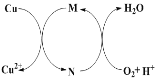
下列有关说法正确的是
A. a、b、c 之间的关系式为:a=b+c
B. 图中M、N分别为Fe2+、Fe3+
C. 步骤1充分反应后,加入少量CuO是为了除去Fe3+
D. 若制备1 mol的CuCl2,理论上消耗11.2 LO2
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列问题:
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1.
N2(g)+O2(g)=2NO(g) △H=+180.0kJ·mol-1。则相同条件下破坏1mol NO分子中的化学键需要吸收的能量为_______kJ。
(2)25℃时,pH=5的CH3COOH溶液中.由水电离出的氢离子浓度c(H+)=________ kJ·mol-1;往溶液中加入少量NaOH固体,则溶液中![]() _______(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:_________________。
_______(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:_________________。
(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其中含碳元素的各种微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。
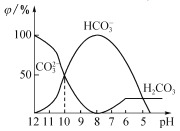
①在同一溶液中,H2CO3、HCO3-、CO32-______(填“能”或“不能”)大量共存。
②当pH =7时,溶液中含碳元素的微粒主要为________。溶液中各种离子的物质的量浓度大小关系为______________。
③反应的CO32-+H2O![]() HCO3-+OH-的平衡常数Kh=______________________。
HCO3-+OH-的平衡常数Kh=______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质在水溶液中的电离方程式正确的是( )
A. NaHSO4 = Na++ HSO4-B. BaSO4 = Ba2++SO42-
C. CH3COONH4![]() NH4+ + CH3COO-D. H2CO3
NH4+ + CH3COO-D. H2CO3![]() 2H++CO32-
2H++CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com