
科目: 来源: 题型:
【题目】Se 元素是人类必须的微量元素之一。下列说法不正确的是
A.SeO2 可以被氧化B.H2Se 比 H2S 不稳定
C.Se 原子的半径比 Cl 原子大D.是性质最接近金属的非金属
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体,火力发电厂释放出大量的NOx、SO2和CO2等气体也是其原因,现在对其中的一些气体进行了一定的研究:
(1)用 CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) △H = - 574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H = - 1160 kJ/mol
③H2O(g) = H2O(l) △H = - 44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式: _____________________________________________________________。
(2)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体。4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是________________(填代号)。

(3)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH=a kJ/mol
N2(g)+CO2(g) ΔH=a kJ/mol
在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(NO)=_____________________;计算该反应的平衡常数K=____________________。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_________(填字母代号)。
A.通入一定量的CO2 B.加入合适的催化剂
C.适当缩小容器的体积 D.通入一定量的NO
E.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则达到新平衡时NO的转化率____________(填“升高”或“降低”),a________0(填“>”或“<”)。
(4)温度T1和T2时,分别将0.50 mol CH4和1.2mol NO2充入1 L的密闭容器中发生反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=bkJ/mol。
N2(g)+CO2(g)+2H2O(g) △H=bkJ/mol。
测得有关数据如下表:
温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法正确的是__________________。
A.T1>T2,且b>0
B.当温度为T2、反应进行到40 min时, x>0.15
C.温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)<0.70mol
D.温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50molH2O(g),反应开始时,ν(正)>ν(逆)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:(1)实验室制取Cl2的方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,其中MnO2发生了__反应,是__剂;每4分子氯化氢中只有___分子发生了___反应,盐酸是___剂。
MnCl2+Cl2↑+2H2O,其中MnO2发生了__反应,是__剂;每4分子氯化氢中只有___分子发生了___反应,盐酸是___剂。
(2)室温下KMnO4与浓盐酸反应制取氯气的化学方程式:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,请在上式中用单线桥法表示出不同元素的原子间得失电子的情况。___
(3)用CuCl2作催化剂,在450℃时用空气中的O2跟HCl反应也能制得氯气,其化学方程式:4HCl+O2![]() 2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是__;比较以上三个反应,可以认为氧化剂的氧化能力从强到弱的顺序为___。
2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是__;比较以上三个反应,可以认为氧化剂的氧化能力从强到弱的顺序为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】HIO4主要以H5IO6形式存在,H5IO6是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化Mn2+。
(1)请完成并配平下列离子反应。
____Mn2++____H5IO6===_____MnO4-+____IO3-+_____H++_____
(2)根据以上离子方程式判断H5IO6是_____酸(填“强”或“弱”)。
(3)上述反应,被氧化的元素是_____(填元素符号),该反应的转移电子数______。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 用浓盐酸分别和MnO2、KClO3反应制备1mol氯气,转移的电子数均为2NA
B. 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA
C. 常温下,1L pH=2的H2SO4溶液中,硫酸和水电离的H+总数为0.01NA
D. 常温常压下,NO2与N2O4的混合气体46g,原子总数为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质结构的命题中,错误的项数有
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④冰中存在极性共价键和氢键两种化学键的作用
⑤Cu(OH)2是一种蓝色絮状沉淀,既溶于硝酸、氨水,也能溶于硫酸氢钠溶液中
⑥熔融态的HgCl2不导电,HgCl2稀溶液有弱的导电能力说明固态HgCl2是分子晶体,为非电解质
⑦氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3.H2O分子,根据氨水的性质可知NH3.H2O的结构式可记为:
A. 4项 B. 5项 C. 6项 D. 7项
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸钙晶体(CaC2O4·H2O)是一种受热容易分解的盐,某班同学要探究其受热分解的产物,甲组同学认为其分解产物可能是CaCO3、CO和H2O,乙组同学认为其分解产物可能是CaO、CO2和H2O。两组同学将草酸钙晶体放入石英试管进行加热,按照下图所示装置进行探究,请回答相关问题。
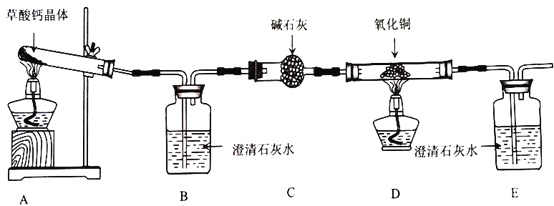
(1)盛放碱石灰的仪器名称是___________。证明分解产物中有CO的现象是______________________。
(2)装置存在一处明显缺陷,该缺陷是________________,改进的方法是______________________(任写一种)。
(3)实验中B中澄清石灰水未变浑浊,甲组同学认为自己的判断正确,但乙组同学认为可能是因为温度不够,需将试管下方酒精灯更换为___________重新实验。
(4)更换仪器及各种试剂后重新实验,B中澄清石灰水变浑浊,装置C的作用是______________________。
(5)更换仪器重新实验时发生的反应方程式是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Donepezil(G物质)是一种高度选择性的乙酰胆碱酯酶抑制剂,用于治疗轻度和中度阿尔茨海默型痴呆症状,它能提高患者的认知能力,其合成路线如下图所示(箭头上方表示反应物,箭头下方表示反应条件),请回答相关问题。
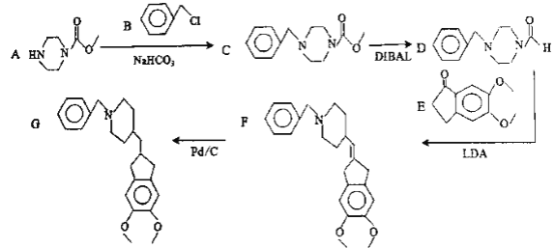
(1)D物质的分子式是___________,E物质的官能团名称是___________。
(2)F→G的反应类型是___________。A→C的反应方程式是______________________。
(3)B物质发生水解反应的条件是___________,水解所得有机产物的名称是___________。
(4)E物质的同分异构体中符合下列要求的有___________种,其中核磁共振氢谱中峰的数目最少的结构简式是_____________。
a.分子中含有苯环
b.苯环上有两个取代基且其中一个是甲基,含有羧基和醛基
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com