
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
B. 标准状况下,2.24LSO3中所含原子数为0.4 NA
C. 常温常压下,16gO2和O3的混合气体中所含原子数目为NA
D. 在一定条件下lmolN2与3molH2反应生成的NH3分子数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,H2 + CO2![]() CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的( )
CO+ H2O(g)的平衡常数K=9/4。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的( )

A. 平衡时,甲中和丙中H2的转化率是60%
B. 平衡时,乙中CO2的转化率小于60%
C. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
D. 平衡时,丙中c(CO2)是甲中的2倍,是0.008mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列有关叙述正确的是( )
A. 标准状况下,22.4 L H2O所含的分子数为NA
B. 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
C. 1L一氧化碳气体一定比1L氧气的质量小
D. 常温常压下8g O3中含有8NA个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】以A和B为原料合成扁桃酸衍生物F的路线如下:

(1)A的分子式为C2H2O3,可发生银镜反应,且具有酸性,A所含官能团的名称为_________。写出A+B![]() C的反应类型:_________。
C的反应类型:_________。
(2) 中①、②、③三个-OH与钠反应活性由强到弱的顺序是_____。
中①、②、③三个-OH与钠反应活性由强到弱的顺序是_____。
(3)E是由2分子C生成的含有3个六元环的化合物,E分子核磁共振氢谱峰面积之比_______。
(4)D![]() F的反应方程式是______________,1molF在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为____________mol,符合下列条件的F的所有同分异构体有四种(不考虑立体异构),写出其中两种的结构简式:___________。
F的反应方程式是______________,1molF在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为____________mol,符合下列条件的F的所有同分异构体有四种(不考虑立体异构),写出其中两种的结构简式:___________。
①属于一元酸类化合物 ②苯环上只有2个取代基且处于对位,其中一个是羟基
(5)已知: ,下列流程是A的一种合成方法___________,写出方框中各物质的结构简式:
,下列流程是A的一种合成方法___________,写出方框中各物质的结构简式:
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A~M有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与NaHCO3溶液反应,F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色,D能发生银镜反应,M与NaOH溶液反应后的产物,其一氯代物只有一种。

已知: (R1、R2表烃基或氢原子)
(R1、R2表烃基或氢原子)
请回答:
(1)B、F的结构简式分别为________、________。
(2)反应①~⑦中,属于消去反应的是________(填反应序号)。
(3)D发生银镜反应的化学方程式为______________________________;反应⑦的化学方程式为______________________________。
(4)A的相对分子质量在180~260之间,从以上转化中不能确认A中的某一官能团,确定该官能团的实验步骤和现象为__________________________________________。
(5)符合下列条件的F的同分异构体共有________种。
a.能发生银镜反
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1∶1∶2∶6
查看答案和解析>>
科目: 来源: 题型:
【题目】三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:

已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是__________________________(写一点);浸取铬时反应的离子方程式为_______________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是_____________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图1所示:

图1 图2
pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是________________________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图2所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】图1是甲、乙、丙三种固体物质的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )
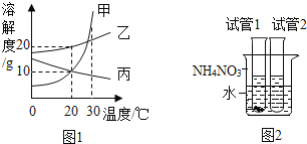
A. 甲物质的溶解度比乙物质的溶解度大
B. 加入试管1的固体是丙
C. 向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出
D. 将30℃时甲、乙、丙三种物质的饱和溶液各100g降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com