
科目: 来源: 题型:
【题目】用Cl2生产含氯有机物时会产生HCl,利用如下反应可实现氯的循环利用。4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)+Q(Q>0)在2L密闭容器中进行该反应,在不同时间测得实验数据如下表:
物质 物质的量 (mol) 时间 | HCl(g) | O2(g) | H2O(g) | Cl2(g) |
0min | 4 | 1 | 0 | 0 |
2min | 1.2 | 0.3 | 1.4 | |
3min | 1.2 | 0.3 | 1.4 | |
4min | 1.0 | 0.35 | 1.5 |
(1)计算0~2min内Cl2的平均生成速率___________________。 该反应合适的温度范围是380~440℃,选择该温度范围可能的原因是:①加快反应速率;②_______________________________。
(2)工业上用传感器检测反应容器中的气体压强,当压强保持不变时,表面反应已达平衡。能通过检测压强判断反应是否达到平衡状态的理由是__________________________。
(3)实验时,在3~4min之间改变了某一条件造成平衡移动。表中数据说明平衡向____移动(填“左”或“右”);达到新平衡后,与原来相比平衡常数_______(填“变大”、“变小”、“不变”)。
(4)Cl2也可用于制备新型净水剂高铁酸钠(Na2FeO4)。配平制备反应的化学方程式___Fe(NO3)3+___NaOH+___Cl2→___Na2FeO4+___NaNO3+___NaCl+___H2O若反应消耗3.36L Cl2(标准状况),则转移电子的数目是________。
(5)用Na2FeO4杀菌消毒的优点是还原产物具有净水作用,缺点是还原产物会对铁制水管造成腐蚀,造成腐蚀的原理有________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以甲醛和苯酚为主要原料,经下列转化可合成酚醛树脂和重要的有机合成中间体D(部分反应条件和产物已略去)

已知:R1CH2COOCH2+R2COOCH3![]() CH3OH+
CH3OH+
请回答下列问题:
(1)反应①的反应类型为___________;A的化学名称为___________。
(2)C中所含官能团的名称为___________;D的分子式为___________。
(3)反应②的化学方程式为______________________。
(4)A的下列性质中,能反映支链对苯环结构产生影响的是___________(填字母)。
a.能与氢氧化钠溶液反应
b.能使酸性高锰酸钾溶液褪色
c.向稀溶液中加入浓溴水后,产生沉淀
(5)芳香化合物E(C8H10O2)与B的水解产物互为同分异构体,1molE可与2 mol NaOH反应,其核磁共振氢谱中有3组峰且峰面积之比为3:1:1,则E有___________种可能的结构(不考虑立体异构)。
(6)以CH3OH和CH3ONa为原料(其他试剂任选),设计制备CH3COCH2 COOCH3的合成路线:CH3OH![]() ______。
______。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E 代表五种元素。请填空:
(1)A 元素基态原子的最外层有 3 个未成对电子,次外层有 2 个电子,其元素符号为_____, 电子排布图为_____,原子核外电子的运动状态有_____种。
(2)B 元素的-2 价离子和 C 元素的+1 价离子的电子层结构都与氩原子的相同,B 的原子结构 示意图为_____,B、C 所形成的化合物的电子式为_____。
(3)D 元素的+3 价离子的 3d 能级为半充满状态,D 的元素名称为________,其基态原子的所有 电子占有________个原子轨道。
(4)E 元素基态原子的 M 层为全充满状态,N 层没有成对电子,只有一个未成对电子,则 E 的基态原子的电子有 ________________个 伸 展 方 向 ,其基态原子的电子排布式 为_________________________ ,E +的外围电子排布图为_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】电解NaB(OH)4溶液制备H3BO3的原理如下图所示,下列叙述错误的是

A. M室发生的电极反应式:2H2O-4e-=O2↑+4H+
B. a、c为阴离子交换膜,b为阳离子交换膜
C. N室中:a%<b%
D. 理论上每生成1 mol H3BO3,两极室共产生标准状况下16.8 L气体
查看答案和解析>>
科目: 来源: 题型:
【题目】装置(Ⅰ)为铁镍(Fe﹣Ni)可充电电池:Fe+NiO2![]() Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是( )
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是( )

A. 闭合 K 时,X 的电极反应式为:2H++2e═H2↑
B. 给装置(Ⅰ)充电时,OH通过阴离子交换膜,移向 A 电 极
C. 给装置(Ⅰ)充电时,B 极参与反应的物质被氧化
D. 闭合 K 时,A 电极反应式为:NiO2 + 2e +2H+═Ni(OH)2
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,Fe、HCN与K2CO3可发生反应Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O。请回答下列问题:
(1)金属铁的堆积方式为___________,其配位数为___________。
(2)HCN分子的结构式为___________,写出一种与CN-互为等电子体的阴离子:___________。
(3)键角NH3___________(填“>”“<”或“=")NF3,原因是___________。
(4)K4Fe(CN)6的中心离子的核外电子排布式为___________。
(5)C、N、O、H的第一电离能由小到大的顺序为___________。
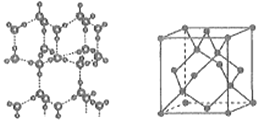
(6)冰的晶体结构模型如图所示,其晶胞结构(如图所示)与金刚石的晶胞结构相似,水分子间以氢键相连,则一个晶胞中含有___________个氢键,用NA表示阿伏加德罗常数的值,若氢键的键长为dnm,则晶体密度ρ=___________g·cm-3(用含有d、NA的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜。下列说法中正确的是
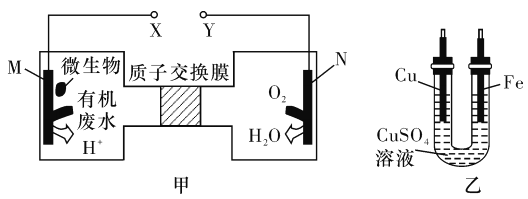
A. 铜电极应与X相连接
B. H+经过质子交换膜由右向左移动
C. 当N电极消耗0. 25 mol气体时,则铁电极增重16 g
D. M电极反应式:CO(NH2)2+H2O-6e- =CO2↑+N2↑+6H+
查看答案和解析>>
科目: 来源: 题型:
【题目】H2是一种清洁能源。在冶金、电力、材料等领域应用广泛。请回答下列问题:
(1)某科研团队利用透氧膜获得N2、H2的工作原理如图甲所示(空气中N2与O2的物质的量之比按4:1计)。上述过程中,膜I侧所得气体的物质的量之比n(H2):n(N2)=3:1,则CH4、H2O与O2反应的化学方程式为______________________。

(2)用H2和CO合成甲醇的热化学方程式为CO(g)+2H2(g) ![]() CH3OH (g) △H1。已知:CO2(g)+3H2(g)==CH3OH(g)+H2O(g) △H2=-49.0kJ·mol-1;CO(g)+H2O(g)==CO2(g)+H2(g) △H3=-41.1k J·mol-1.则△H1=___________ k J·mol-1。
CH3OH (g) △H1。已知:CO2(g)+3H2(g)==CH3OH(g)+H2O(g) △H2=-49.0kJ·mol-1;CO(g)+H2O(g)==CO2(g)+H2(g) △H3=-41.1k J·mol-1.则△H1=___________ k J·mol-1。
(3)向容积可变的密闭容器中充入1 mol CO和2.2molH2,在恒温恒压条件下发生反应CO(g)+2H2(g)![]() CH3OH(g),平衡时,CO的转化率[α(CO)]随温度、压强的变化情况如图乙所示。
CH3OH(g),平衡时,CO的转化率[α(CO)]随温度、压强的变化情况如图乙所示。

①压强:p1___________(填“>”<”或“=”)p2。
②M点时,H2的转化率为___________(计算结果精确到0.1%),该反应的平衡常数Kp=___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③不同温度下,该反应的平衡常数的对数值(lgK)如图丙所示,其中,A点为506K时平衡常数的对数值,则B、C、D、E四点中能正确表示该反应的lgK与温度(T)的关系的是___________。
(4)H2还原NO的反应为2NO(g)+2H2(g)![]() N2(g)+2H2O(1),实验测得反应速率的表达式为v=kcm(NO)·cn(H2)(k是速率常数,只与温度有关)
N2(g)+2H2O(1),实验测得反应速率的表达式为v=kcm(NO)·cn(H2)(k是速率常数,只与温度有关)
①某温度下,反应速率与反应物浓度的变化关系如下表所示。
编号 | c(H2)/(mol/L) | c(NO)/(mol/L) | v/(mol/Lmin) |
1 | 0.10 | 0.10 | 0.414k |
2 | 0.10 | 0.20 | 1.656k |
3 | 0.50 | 0.10 | 2.070k |
由表中数据可知,m=___________,n=___________。
②上述反应分两步进行:i.2NO(g)+H2(g)==N2(g)+H2O2(1)(慢反应);ii.H2O2(1)+H2(g)==2H2O(1)(快反应)。下列叙述正确的是___________(填字母)
A.H2O2是该反应的催化剂
B.反应i的活化能较高
C.总反应速率由反应ii的速率决定
D.反应i中NO和H2的碰撞仅部分有效
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:pKa=lgKa,25℃时,H2SeO3 的 pKa1=1.34, pKa2=7.34。用 0.1molL1NaOH 溶 液滴定 20mL0.1molL1H2SeO3 溶液的滴定曲线如图所示(曲线上的数字为 pH)。下列说法不正 确的是

A. a 点所得溶液中:2c(H2SeO3)+c(SeO32)<0.1 molL1
B. b 点所得溶液中:c(H2SeO3)+c(H+)=c(SeO32)+c(OH)
C. c 点所得溶液中:c(Na+)<3c(HSeO3)
D. d 点所得溶液中:c(Na+)>c(SeO3)>c(HSeO3 )
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20.00 mL 0.100 mol·L-1 CH3COONa溶液中逐滴加入0.100 0 mol·L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是

A. 点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+)
B. 点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C. 点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-)
D. 整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com