
科目: 来源: 题型:
【题目】(1)标准状况下,33.6 L氧气的物质的量为________mol;标准状况下,2 mol氢气的体积为________L。
(2)标准状况下,6 g氢气的体积为________L;标准状况下,体积为11.2 L的CO2的质量为________g。
(3)标准状况下,11.2 L氯气的分子数目是________;标准状况下,1.204×1023个氧气分子的体积是________L。
(4)标准状况下,某气体的密度为1.25 g·L-1,则其摩尔质量为________g·mol-1。
(5)实验室用H2O2和MnO2制备O2,2H2O2![]() 2H2O+O2↑,现有34 g H2O2,可制得O2在标准状况下的体积是__________。
2H2O+O2↑,现有34 g H2O2,可制得O2在标准状况下的体积是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实可以用勒夏特列原理解释的是
A. 高锰酸钾溶液与草酸发生化学反应刚开始缓慢,随后反应迅速加快
B. 实验室采用排饱和食盐水的方法收集氯气(Cl2+H2O![]() HCl+HClO)
HCl+HClO)
C. 500 ℃左右的温度比室温更有利于合成氮反应N2(g)+ 3H2 (g)![]() 2NH3(g) △H<0
2NH3(g) △H<0
D. FeCl3+3KSCN![]() Fe(SCN)3+3KCl, 增大KCl的浓度则溶液的颜色变浅
Fe(SCN)3+3KCl, 增大KCl的浓度则溶液的颜色变浅
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
A.80 g硝酸铵中含有氮原子数为NA
B.0.1 molN5+离子中所含的电子数为3.4NA
C.1 mol甲烷和NA个甲烷分子的质量相等
D.16 g氧气和16 g臭氧所含的原子数均为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于可逆反应:A(g)+3B(g) ![]() 2C(g) △H <0,下列叙述正确的
2C(g) △H <0,下列叙述正确的
A. 增大反应物的浓度,可以提高活化分子百分数,所以 v(正)会先增大后减小
B. 升高温度可以提高活化分子的能量所以v(正)、v(逆)都增大,但v(正)增的更大
C. 采用催化剂,可以提高活化分子百分数,所以会引起v(正)、v(逆)同时增大且增大的倍数相同
D. 减小压强可以降低单位体积内活化分子的数目,所以v(正)减小、v(逆)增大
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下有以下四种气体:①6.72L CH4 ②3.01×1023 HCl分子③13.6g H2S ④0.2mol NH3。下列对四种气体的关系从小到大表示不正确的是( )
A.物质的量:④<①<③<②B.体积:④<①<②<③
C.质量:④<①<③<②D.氢原子个数:②<④<③<①
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A–。已知25 ℃时,HA的Ka=6.25×10–5,H2CO3的Ka1=4.17×10–7,Ka2=4.90×10–11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A–。已知25 ℃时,HA的Ka=6.25×10–5,H2CO3的Ka1=4.17×10–7,Ka2=4.90×10–11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)
A. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B. 提高CO2充气压力,饮料中c(A–)不变
C. 当pH为5.0时,饮料中![]() =0.16
=0.16
D. 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(![]() )+c(
)+c(![]() )+c(OH–)–c(HA)
)+c(OH–)–c(HA)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是( )
A. 已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含74.0 g Ca(OH)2的稀溶液与稀硫酸完全中和,放出57.3 kJ的热量
B. 已知N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ·mol-1,将足量的N2(g)和H2(g)置于密闭的容器中充分反应生成1mol NH3(g),放出46.2kJ的热量
2NH3(g) △H=-92.4kJ·mol-1,将足量的N2(g)和H2(g)置于密闭的容器中充分反应生成1mol NH3(g),放出46.2kJ的热量
C. 2gH2完全燃烧生成液态水放出285.8 kJ热量,则表示氢气燃烧的热化学方程式为:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ
D. 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+1/2O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知有机物分子中的碳碳双键发生臭氧氧化反应: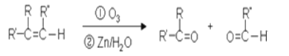 ,有机物A的结构简式为
,有机物A的结构简式为 ,G的分子式为C7H12O,以下A~H均为有机物,其转化关系如下:
,G的分子式为C7H12O,以下A~H均为有机物,其转化关系如下:

(1)下列说法正确的是 ______ 。(填字母序号)
A.C的官能团为羧基
B.1molA最多可以和2molNaOH反应
C.C可以发生氧化反应、取代反应和加成反应
D.![]() 可以发生消去反应
可以发生消去反应
(2)F的结构简式为____________ ,由F到G的反应类型为___________ 。
(3)反应①的作用是__________________ ,合适的试剂a为____________。
(4)同时满足下列条件的A的一种同分异构体的结构简式______________________。
Ⅰ.与A具有相同的官能团;Ⅱ.属于苯的邻二取代物;Ⅲ.能使FeCl3溶液显色;Ⅳ.核磁共振氢谱分析,分子中有8种不同化学环境的氢原子。
(5)H与G分子具有相同的碳原子数目,且1molH能与足量的新制银氨溶液反应生成4mol单质银。写出H与足量的新制银氨溶液反应的化学方程式__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)基态B原子的电子排布图为________________________,其第一电离能比Be___________(填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为___________ (标出配位键),其中心原子的杂化方式为________,写出[BH4]-的一种阳离子等电子体_______。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________(以n表示硼原子的个数)。

(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有_________。

(5)三氯化硼的熔点比氯化镁的熔点低,原因是_______________________。
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为_______;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伽德罗常数为NA,则镁的摩尔质量的计算式是________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了如图的实验装置.B中盛有饱和碳酸氢钠溶液,目的是除去二氧化碳中混有的氯化氢气体,E为收集氧气装置.

(1)写出装置A中发生反应的化学方程式____________。
(2)C中盛有____________,目的是_____________。
(3)写出装置D中发生反应的化学方程式__________。
(4)指出装置E的错误_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com