
科目: 来源: 题型:
【题目】G是合成药物的中间体,其制备路线如下(A为芳香烃):

已知:①R-CN![]() R-COOH
R-COOH
②![]()
![]()
![]()
回答下列问题:
(1)G的名称是_________;E中官能团的名称为___________。
(2)B→C的反应试剂是_______ ;E→F的反应类型是_______。
(3)C→D反应的化学方程式为________________。
(4)G能通过缩聚反应得到H,有G→H反应的化学方程式为________________。
(5)I是G的同系物,满足下列条件的I的同分异构体有_______种(不考虑立体异构)。
① I相对分子质量比G大14 ② 苯环上含3个取代基
(6)结合以上合成路线及相关信息,设计由苯制备苯酚的合成路线________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是常见的四种有机物的比例模型示意图。下列说法正确的是( )

A. 甲能使酸性高锰酸钾溶液褪色
B. 乙可与溴水发生取代反应使溴水褪色
C. 丙在铁作催化剂条件下与溴水发生取代反应
D. 丁在浓硫酸、加热条件下可与乙酸发生取代反应
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为_____________,G的原子结构示意图是__________________________。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为_________,所含化学键类型为___________,向甲中滴加足量水时发生反应的化学方程式是____________________________。
(3)E、F、G三种元素形成的简单离子,半径由大到小的顺序是__________。(用离子符号表示)
(4)用BA4、D2和EDA的水溶液组成燃料电池,电极材料为多孔惰性金属电极。在a极通入BA4气体,b极通入D2气体,则a极是该电池的________极,正极的电极反应式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
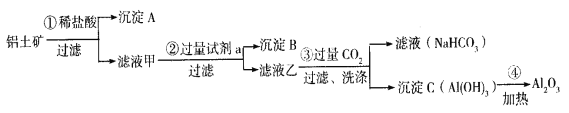
①沉淀 A、B的成分分别是____________、____________;步骤②中的试剂a是_________;(以上均填化学式)。
②试写出步骤③中发生反应的离子方式______________、________________;
③简述检验所得滤液甲中存在Fe3+的操作方法:________________________。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:

已知:在pH为4~5时,Fe3+几乎完全转化为Fe(OH)3沉淀,Cu2+却不反应。
①氧化剂最好选用__________(填编号)。
A.KMnO4 B.HNO3 C.Cl2
②写出“酸溶”时主要的离子方程式__________________________
③从滤液经过结晶得到氯化铜晶体的方法是_________(按实验先后顺序选填编号)。
A. 过滤 B. 蒸发至干 C. 冷却结晶 D. 蒸发浓缩
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列关于![]() 的
的![]() 溶液的叙述正确的是( )
溶液的叙述正确的是( )
A.该溶液中由![]() 电离出的
电离出的![]()
B.与等体积![]() 的
的![]() 溶液混合,所得溶液呈中性
溶液混合,所得溶液呈中性
C.该溶液中离子浓度大小关系:![]()
D.滴加![]() 溶液至
溶液至![]() 时,溶液
时,溶液![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气在工业上有着重要的用途,某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝(无水AlCl3遇潮湿空气即产生大量白雾),可用下列装置制备。

(1) 装置B中盛放__________溶液,其作用是_________;F中的是______溶液,其作用是_____________。
(2)装置A实验开始前,应先_________,接下来的操作依次是_____________(填序号)。
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
(3)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为﹣59℃,液体为红色;Cl2沸点为﹣34℃,液态为黄绿色。
①设计最简单的实验验证Cl2中含有ClO2:收集一试管气体,盖上胶塞,放入冰水混合物中,若____________,则说明Cl2中含有ClO2 。
②将过硫酸钠(Na2S2O8)液加入亚氯酸钠(NaClO2)中可制备ClO2,NaClO2中Cl元素的化合价是___________,该反应中氧化剂和还原剂的物质的量之比为________。
③将ClO2通入MnSO4溶液,溶液中可检测到Cl-,同时有黑色MnO2沉淀生成。该反应的离子方程式为: ___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.氢氧燃料电池放电时可以将化学能全部转化为电能
B. 铜锌硫酸原电池工作时,电子从锌电极经电解液流向铜电极
铜锌硫酸原电池工作时,电子从锌电极经电解液流向铜电极
C.将3mol H2与1mol N2混合于密闭容器中充分反应可生成2molNH3,转移电子数目为6NA
D.手机上用的锂离子电池充电时将电能转化为化学能
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示为某种胃药的核心合成反应部分过程:
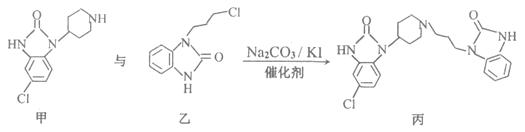
下列说法正确的是( )
A.甲中的两个![]() 键的活性相同B.乙所有原子在同一平面上
键的活性相同B.乙所有原子在同一平面上
C.丙的分子式![]() D.该反应生成丙的原子利用率小于100%
D.该反应生成丙的原子利用率小于100%
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)亚磷酸(H3PO3)为二元弱酸。 H3PO3中P元素的化合价为______,其在元素周期表的位置是__________,H3PO3与过量NaOH溶液反应的离子方程式为___________________。
(2)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图所示,化合物X可借助傅里叶红外光谱图确定。


①在图示的转化中,被还原的元素是_______________,X的化学式为________________。
②SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com