
科目: 来源: 题型:
【题目】下列用来表示物质变化的化学用语中,正确的是( )
A. Al2(SO4)3溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH-![]() Al(OH)3
Al(OH)3
B. 以KOH溶液为电解质溶液的氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH-
C. 测0.1mol/L氨水的pH为11:NH3·H2O![]() NH4++OH-
NH4++OH-
D. 钢铁发生吸氧腐蚀的正极反应式:Fe-2e-=Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A. 该反应的化学方程式为3B+4D6A+2C
B. 反应进行到1s时,v(A)=v(D)
C. 反应进行到6s时,各物质的反应速率相等
D. 反应进行到6s时,B的平均反应速率为0.05mol/(Ls)
查看答案和解析>>
科目: 来源: 题型:
【题目】3 H2(g) + N2(g) ![]() 2NH3(g) 反应过程中的能量变化如下图,有关说法错误的是( )
2NH3(g) 反应过程中的能量变化如下图,有关说法错误的是( )

A. 图中C表示生成物NH3(g)的总能量
B. 断裂3molH—H和1molN≡N所吸收的总能量大于形成6molN—H所释放的总能量
C. 逆反应的活化能E(逆)=E+△H
D. 3 H2(g) + N2(g)![]() 2NH3(g) △H< 0
2NH3(g) △H< 0
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。


①上述装置中D电极应连接肼燃料电池的____极(填“A”或“B”),该电解池中离子交换膜为_____离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为____________
③当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(2)利用下图丙装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于_______处。若X为锌,开关K置于M处,该电化学防护法称为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向25mL 0.12mol/LAgNO3溶液中逐滴加入浓度为2%的氨水,先出现沉淀,继续滴加沉淀溶解。该过程中加入氨水的体积V与溶液中lg[c(H+)/c(OH-)]的关系如图所示。已知e点时溶液迅速由浑浊变得澄清,且此时溶液中c(Ag+)与c(NH3)均约为2×10-3 mol/L。下列叙述不正确的是

A. a点溶液呈酸性的原因是AgNO3水解
B. b点溶液中:c(Ag+)+c[Ag(NH3)2+]<c(NO3-)
C. cd段加入的氨水主要用于沉淀的生成和溶解
D. 由e点可知,反应Ag++2NH3![]() [Ag(NH3)2]+平衡常数的数量级为105
[Ag(NH3)2]+平衡常数的数量级为105
查看答案和解析>>
科目: 来源: 题型:
【题目】用如下图所示的装置进行电解,通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。

(1)E为电源的________极,Fe为电解池的_______极。
(2)A中发生反应的化学方程式为_____________________。
(3)在B中观察到的现象是____________________。
(4)Pt电极的电极反应式为____________________。如电路中有0.2 mol电子发生转移,D端得到气体的体积是________(标准状况)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有X、Y、Z、T、U五种短周期元素。X、Y、Z 三元素在周期表中的位置如图所示,三元素的原子序数之和是 41。X 和 T 的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物。U 单质在 Z 单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红。
X | |
Y | Z |
(1)各元素的符号是 X______,Y______,Z______。
(2)Y 原子的结构示意图为_______。
(3)用电子式表示 Y 与 T 组成的化合物的形成过程:______。
(4)YX2 和 U2Y 反应的化学方程式为______, 其中氧化剂是______,被氧化的元素是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】铈(Ce)是一种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、 Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:
(1)湿法空气氧化法回收铈的部分流程如下:

已知:CeO2不溶于稀盐酸,也不溶于NaOH溶液。
滤渣的成分是________,反应②的离子方程式是________。
(2)干法空气氧化法回收铈是把Ce(OH)3被空气氧化成Ce(OH)4,氧化过程中发生的化学反应方程式为________。两种制备Ge(OH)4的数据如下表:
干法空气氧化法 | 氧化温度/℃ | 氧化率/% | 氧化时间/h |
暴露空气中 | 110120 | 90 | 18 |
在对流空气氧化炉中 | 110120 | 99 | 8 |
在对流空气氧化炉中大大缩短氧化时间的原因是________。
(3)利用电解方法也可以实现铈的回收。
①在酸性条件下电解Ce2O3 (如图):阳极电极反应式为______,离子交换膜为______ (填“阴”或“阳”)离子交换膜。
②电解产物Ce(SO4)2是重要的氧化剂,将其配成标准溶液,在酸性条件下能测定工业盐中NaNO2的含量,写出发生反应的离子方程式_______。

查看答案和解析>>
科目: 来源: 题型:
【题目】CH4超干重整CO2技术可得到富含CO的化工原料。回答下列问题:
(1)CH4超干重整CO2的催化转化如图所示:
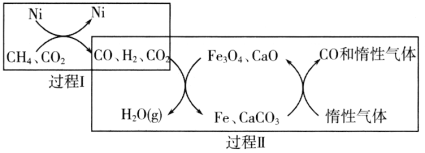
①已知相关反应的能量变化如图所示:

过程Ⅰ的热化学方程式为________。
②关于上述过程Ⅱ的说法不正确的是________(填序号)。
a.实现了含碳物质与含氢物质的分离
b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应
d.Fe3O4、CaO为催化剂,降低了反应的ΔH
③其他条件不变,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应CH4(g)+CO2(g)=2CO(g)+2H2(g)进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态________(填“是”或“不是”)平衡状态;b点CH4的转化率高于c点,原因是________。
(2)在一刚性密闭容器中,CH4和CO2的分压分别为20kPa、25kPa,加入Ni/α-Al2O3催化剂并加热至1123K使其发生反应CH4(g)+CO2(g)=2CO(g)+2H2(g)。

①研究表明CO的生成速率υ(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,某时刻测得p(CO)=20kPa,则p(CO2)=________kPa,υ(CO)=________mol·g-1·s-1。
②达到平衡后测得体系压强是起始时的1.8倍,则该反应的平衡常数的计算式为Kp=________(kPa)2。(用各物质的分压代替物质的量浓度计算)
(3)CH4超干重整CO2得到的CO经偶联反应可制得草酸(H2C2O4)。常温下,向某浓度的草酸溶液中加入一定浓度的NaOH溶液,所得溶液中![]() ,则此时溶液的pH=________。(已知常温下H2C2O4的Ka1=6×10-2,Ka2=6×10-5,lg6=0.8)
,则此时溶液的pH=________。(已知常温下H2C2O4的Ka1=6×10-2,Ka2=6×10-5,lg6=0.8)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列曲线分别表示元素某种性质与核电荷数的关系(Z为核电荷数,Y 为元素的有关性质),把与下面的元素有关性质相符合的曲线的标号填入相应括号中。
a  b
b c
c d
d e
e
(1)ⅡA 族元素的最外层电子数______
(2)ⅦA 族元素氢化物的沸点______
(3)O2-、F-、Na+、Mg2+、Al3+的离子半径______
(4)第三周期元素的最高化合价______
(5)第二周期元素 Be、B、C、N、O 的原子半径______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com