
科目: 来源: 题型:
【题目】下列化学用语表达不正确的是( )
①丙烷的球棍模型 ②丙烯的结构简式为CH3CHCH2
②丙烯的结构简式为CH3CHCH2
③某有机物的名称是2,3-二甲基戊烷 ④![]() 与C8H6互为同分异构体
与C8H6互为同分异构体
A. ①②B. ②③C. ②④D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A. 3g 3He含有的中子数为1NA
B. 1 L 0.1 mol·L1磷酸钠溶液含有的![]() 数目为0.1NA
数目为0.1NA
C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在容积为2L的密闭容器中进行反应:aN(g)![]() bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
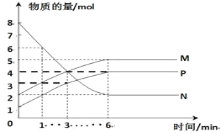
(1)反应化学方程式中各物质的系数比为a:b:c=______。
(2)1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:_____。
(3)下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗amolN,同时消耗bmolM
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有一个电子,但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能由大到小的顺序是:________________(填元素符号),e的价层电子轨道示意图为__________________________________, e的焰色反应为亮绿色,请用原子结构的知识解释原因_____________________________
(2)a和b、c、d、e形成的二元共价化合物有很多种,其中有一分子呈三角锥形,该分子的中心原子的杂化方式为__________;其中有两种分子,既含有极性共价键、又含有非极性共价键的化合物是_____________________(填化学式).
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的两种酸是_____;请从物质结构与性质的关系解释,这两种酸酸性强弱的原因是______________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
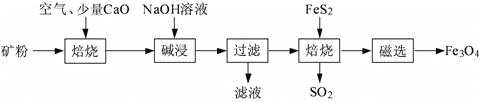
(1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为:___________________。
(2)“过滤”得到的滤渣中含有大量的Fe2O3。
①不添加CaO的矿粉焙烧时,其中FeS2转化为Fe2O3时发生的化学方程式:____________。
②添加质量分数为1%CaO后,硫元素最终转化为______________。(填化学式)
(3)向“过滤”得到的滤液中通入过量CO2,含铝元素的物质发生转化的离子方程式为_____________。
(4)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(Fe2O3)∶n(FeS2)=_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】M、R、X、Y、Z为原子序数依次增大的短周期主族元素,M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,Y和M形成的一种化合物是引起酸雨的主要大气污染物,X的原子核外有3个单电子。请回答下列问题:
(1)R基态原子的电子排布式是______________,X、Y、Z电负性由小到大的顺序是_______(填元素符号)
(2)Y的氢化物在乙醇中的溶解度小于M的氢化物,其原因是______________
(3)在 H2O分子中,H﹣O﹣H的键角是_________,H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角________填“大、小、相等”),原因为________________________________
(4)Y与M形成的YM3分子的空间构型是____________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下离子中的若干种:NH4+、Ba2+、Fe2+、Cl-、NO3-、CO32- 、SO42-.某同学收集了该地区的雾霾,经必要的预处理后得到试样溶液,设计并完成如下实验:

试回答下列问题:
(1)实验①中加入稀盐酸后,有无色气体A生成,溶液B依然澄清,且溶液中阴离子种类不变,据此可知原溶液中一定不含__________。(填离子符号)
(2)实验①中发生反应的离子方程式为__________________________________________。
(3)实验②中逐滴加入碳酸氢钠溶液,立即有气泡产生,一段时间后又有沉淀出现,这时的离子方程式为_______________________________________________ 。
(4)气体F的成分为______________。(填化学式)
(5)根据实验③现象该同学认为原溶液中一定含有SO42-,有其他同学认为其结论不合理,又进行了后续实验 ④,最终确认原溶液中含有SO42-,试写出实验④可行的操作方法及现象________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E、W是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E4+与氩原子的核外电子排布相同。W是第四周期d区原子序数最大的元素。请回答下列问题:
(1)填元素名称, C:________写出E的价层电子排布式_________,W在周期表中的位置:___________________
第二周期基态原子未成对电子数与W相同且电负性最小的元素是________(填元素符号).
(2)W(BD)n为无色挥发性剧毒液体,熔点﹣25℃,沸点43℃.不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,W(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________,BD分子的结构式是________
(3)3﹣氯﹣2﹣丁氨酸的结构简式为:![]() ,一个该有机物分子中含有_____个手性碳原子.
,一个该有机物分子中含有_____个手性碳原子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com