
科目: 来源: 题型:
【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO32- |
实验I :取少量该试液进行如下实验。
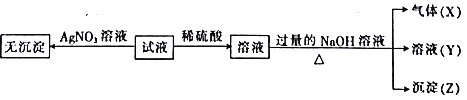
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液,向该溶液中滴加1 mol L-l的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
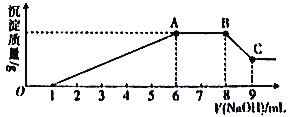
回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有___________种,沉淀Z的化学式____________。
(2)检验气体X的方法是______________________;
(3)写出实验Ⅱ的图象中BC段对应的离子方程式:_____________________________。
(4)A点对应的固体质量为__________g。
(5)通过实验I可以确定该溶液中一定存在的阴离子是_______________,推算该溶液中阴离子的浓度为_________mol L-l,检验该阴离子的方法是:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,则这个碳原子被称为“手性碳原子”,新型纤维酸类降脂药克利贝特可由物质X在一定条件下反应制得:
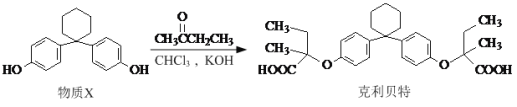
下列有关叙述正确的是
A. 克利贝特的分子式为C28H34O6
B. B.物质X分子中所有碳原子可能位于同一平面内
C. 用NaOH溶液可以鉴别物质X和克利贝特
D. 物质X中无手性碳原子,克利贝特中有两个手性碳原子
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ:用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2 MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:

实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
② | 20 mL 0.2 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
(1)该实验探究的是_________________________________因素对化学反应速率的影响。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________ mol·L-1(假设混合溶液的体积为50 mL)。
(3)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:
①产物Mn2+是反应的催化剂,②_______________________________
Ⅱ:当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)该反应的化学方程式为___________________________________
(2)在恒温恒容密闭容器中,判断上述反应达到平衡状态的依据是________________
a.体系压强不再改变 b.H2的浓度不再改变
c.气体的密度不随时间改变 d.单位时间内消耗H2和CO2的物质的量之比为3∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】茶多酚具有抗氧化作用和抗衰老、降血脂等一系列很好的药理功能,其结构简式如下图,关于茶多酚的下列说法正确的数目有( )

①1mol茶多酚与浓溴水发生加成反应最多消耗6molBr2
②1mol茶多酚与足量的Na2CO3溶液反应放出4molCO2
③1mol茶多酚与足量的NaOH溶液反应最多消耗10molNaOH
④能发生氧化、取代、加成、缩聚反应
⑤已知茶多酚易溶于水,是因为能与水分子之间形成氢键
⑥能使酸性KMnO4溶液褪色
A. 2个B. 3个C. 4个D. 5个
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种新型药物,具有血管扩张活性的选择性β1肾上腺素受体拮抗剂,用于合成该药物的中间体G的部分流程如下:
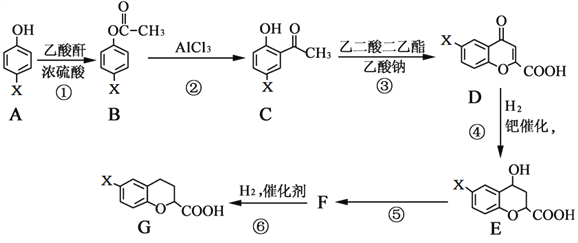
已知:乙酸酐的结构简式为:![]()
请回答下列问题:
(1)G物质中的含氧官能团的名称是________、________。
(2)反应A→B的化学方程式为_________________________________________。
(3)上述④、⑤变化过程的反应类型分别是_______________、______________。
(4)有机物F的结构简式为______________________。
(5)写出满足下列条件的C的同分异构体的结构简式:___________、___________。
Ⅰ. 苯环上只有两种取代基。
Ⅱ. 分子中只有4种不同化学环境的氢。
Ⅲ. 能与NaHCO3反应生成CO2。
(6)根据已有知识并结合相关信息,补充完成以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备![]() 的合成路线流程图(无机试剂任选)。部分合成路线流程图如下:
的合成路线流程图(无机试剂任选)。部分合成路线流程图如下:

请完成合成路线_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述不正确的是
A. 2,3,3,4—四甲基戊烷的一氯代物有3种
B. 分子式为C3H2Cl6的有机物,其同分异构体(不考虑立体异构)共有4种
C. 甲烷与氯气的混合气体在光照条件下反应生成的有机化合物均无同分异构体
D. 结构简式为H3C![]() CH3的有机物,属于芳香族化合物的同分异构体有2种
CH3的有机物,属于芳香族化合物的同分异构体有2种
查看答案和解析>>
科目: 来源: 题型:
【题目】已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_______________________。
(2)砷与氢元素可形成化合物砷化氢,该化合物的空间构型为_____________,其中砷原子的杂化方式为__________。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式________。
(4)已知由元素砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中砷原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式____________;
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定铝原子在三维空间中堆积方式________________(已知NA=6.02×1023,1pm=10-10cm,4053=6.64×107);晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=______pm.(只列出计算式即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】研究含碳化合物的结构与性质,对生产、科研等具有重要意义。
(1)某同学画出基态碳原子的核外电子排布图:![]() ,该电子排布图违背了__;CH3+、-CH3、CH3-都是重要的有机反应中间体。CH3+、CH3-的空间构型分别为___、____。
,该电子排布图违背了__;CH3+、-CH3、CH3-都是重要的有机反应中间体。CH3+、CH3-的空间构型分别为___、____。
(2)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。
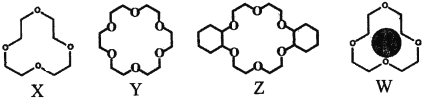
①Li+与X的空腔大小相近,恰好能进入到X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图)。基态锂离子核外能量最高的电子所处能层符号为___________;
②冠醚Y能与K+形成稳定结构,但不能与Li+形成稳定结构。理由是___________。
③烯烃难溶于水,被KMnO4水溶液氧化的效果较差。若烯烃中溶入冠醚Z,氧化效果明显提升。
i.水分子中氧的杂化轨道的空间构型是___________,H-O键键角___________(填“>”“<”或“=”)109°28′
ii.已知:冠醚Z与KMnO4可以发生下图所示的变化。加入冠醚Z后,烯烃的氧化效果明显提升的原因是___________。
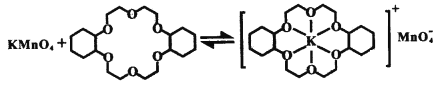
查看答案和解析>>
科目: 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示;下列描述错误的是:

A. 淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B. 以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C. 步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
D. 用SO2水溶液吸收Br2的离子反应方程式为:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】Co、Ni的化合物在生产生活中有着广泛的应用。
(1)Co元素在周期表中的位置是4周期________族。基态Co原子的简化电子排布式为_________。
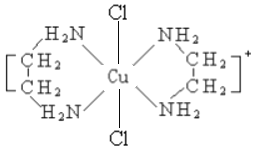
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下左图所示,中心离子的配位数为_______,配合物晶体中可能存在的作用力有___________。
A 离子键 B 极性共价键 C 非极性共价键 D 配位键 E 氢键
(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NiXO晶体中x值为![]() ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
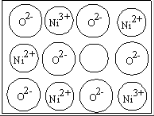
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列, Ni2+填充其中(如图),己知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____g(用a、NA表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com