
科目: 来源: 题型:
【题目】已知:① R-NO2![]() R-NH2;
R-NH2;
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯为原料制备某些化合物的转化关系图:
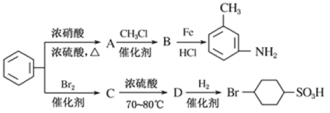
(1)A 转化为B 的化学方程式是____________________________;
(2)在“![]() ”的所有反应中属于取代反应的是______________(填字母),属于加成反应的是__________________(填字母);C 转化为D 的化学方程式是_________________;
”的所有反应中属于取代反应的是______________(填字母),属于加成反应的是__________________(填字母);C 转化为D 的化学方程式是_________________;
(3)B 中苯环上的一氯代物有_______________种同分异构体。
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)亚氯酸钠(NaClO2)是重要漂白剂。探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按右图装置进行制取。
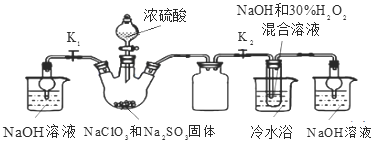
A B C D E
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,38-60℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)用50%双氧水配制30%的H2O2溶液,需要的玻璃仪器除玻璃棒、胶头滴管、烧杯外,还需要_____(填仪器名称);装置C的作用是_____________________。
(2)B中产生ClO2的化学方程式______________________________________。
(3)装置D中反应生成NaClO2的化学方程式为____________________________ 。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是_________,检验该离子的方法是___________________________。
(4)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②______________;③______________;④______________;得到成品。
(5)如果撤去D中的冷水浴,可能导致产品中混有的杂质是______________;
实验Ⅱ:样品杂质分析与纯度测定
(6)测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液。
取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①确认滴定终点的现象是__________________________________________________。
②所称取的样品中NaClO2的物质的量为______________mol(用含c、V的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列各烷烃的分子式。
(1)烷烃A在同温同压下蒸气的密度是氢气的36倍________。
(2)烷烃B的分子中含有200个氢原子________。
(3)1 L烷烃D的蒸气完全燃烧时,生成同温同压下15 L水蒸气________。
(4)0.01 mol烷烃E完全燃烧时,消耗标准状况下的氧气2.464 L________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为不同化学元素组成的化合物示意图,以下说法不正确的是 ( )
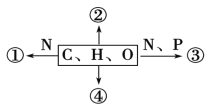
A. 若①为某种具有催化作用的化合物,则①的初步水解产物为多肽,彻底水解产物为氨基酸
B. 若②大量积累于皮下和内脏器官周围,则②为脂肪
C. 若③为构成细胞膜基本骨架的分子,则③为磷脂
D. 若④在低血糖时分解以补充血糖,则④可能是肌糖原和肝糖原
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)相对分子质量为70的烯烃的分子式为________;若该烯烃与足量的H2加成后能生成含3个甲基的烷烃,则该烯烃可能的结构简式为____________。
(2)有机物A的结构简式为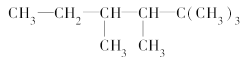
①若A是单烯烃与氢气加成后的产物,则该单烯烃可能有________种结构;
②若A是炔烃与氢气加成的产物,则此炔烃可能有________种结构。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知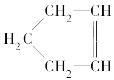 可简写为
可简写为![]() 。降冰片烯的分子结构可表示为
。降冰片烯的分子结构可表示为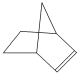 。
。
(1)降冰片烯属于________。
A.环烃 B.不饱和烃
C.烷烃 D.芳香烃
(2)下列对降冰片烯的性质的说法不正确的是________。
A.它可使酸性KMnO4溶液退色
B.它能使溴的四氯化碳溶液退色
C.它能溶于水
D.它燃烧时可发出明亮的火焰
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如下图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。
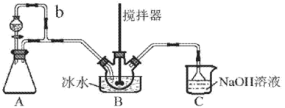
已知:NOSO4H 遇水分解,但溶于浓硫酸而不分解。
(1)装置A 利用 Na2SO3 和硫酸制取 SO2
①A 中反应的化学方程式为___________________________;
②导管 b 的作用是_____________________;
(2)装置C 的主要作用是 (用离子方程式表示)_____________________;
(3)该实验装置存在可能导致 NOSO4H 产量降低的缺陷是___________________________;
(4)测定亚硝酰硫酸NOSO4H 的纯度:准确称取 1.380g 产品放入 250mL 的碘量瓶中,加入 0.1000mol·L-1、60.00mL 的 KMnO4 溶液和10mL25%H2SO4 溶液,摇匀。然后将 0.2500mol·L-1 草酸钠(Na2C2O4)溶液滴入碘量瓶中,消耗草酸钠溶液的体积为 20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:_______![]() + ______
+ ______![]() +_______=_____________Mn2++____CO2↑+ _______H2O
+_______=_____________Mn2++____CO2↑+ _______H2O
②亚硝酰硫酸的纯度=__________(精确到 0.1%)(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列填空:
(一)下列 8 组物质或粒子:
①14N 和 14C ②16O 和 18O ③氰酸铵(NH4CNO)与尿素[CO(NH2)2] ④足球烯(C60)和金刚石 ⑤CH3CH2CH2CH3 和 CH(CH3)3 ⑥CH3CH2CH3 和 CH3(CH2)2CH3 ⑦ ![]() 和
和 ![]() ⑧
⑧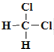 和
和![]()
(1)互为同素异形体的是__________(填编号,下同);
(2)互为同位素的是________________;
(3)互为同系物的是___________;
(4)互为同分异构体的是________________。
(二)有下列几种晶体:
A、水晶 B、冰醋酸 C、白磷 D、金刚石 E、晶体氩 F、干冰 G、氟化钠 H、过氧化钠
(1)属于原子晶体的化合物是__________________(填序号,下同);
(2)含有共价键的离子晶体是________________________;
(3)受热融化时需要克服共价键的晶体是_________________________;
(4)写出下列物质的电子式:过氧化钠_____________,二氧化碳________________。
(三)某烷烃的结构简式为:
(1)用系统命名法命名该烃:__________________________;
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构可能有 ________种(不包括立体异构,下同);
(3)若该烷烃是由炔烃加氢得到的,则原快烃的结构有_________________种;
(4)该烷烃在光照条件下与氯气反应,生成的一氧代烷最多有____________种。
(四)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。 当把 0.4mol 液态肼和0.8mol H2O2 混合反应,生成氮气和水蒸气,放出 256.7KJ 的热量(相当于 25℃、101 kPa 下测得的热量)。
①反应的热化学方程式为________________________________;
②已知 H2O(1)=H2O(g) ΔH=+44kJ/mol。
则 16g 液态肼与液态双氧水反应生成液态水时放出的热量是_________________kJ;
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的A、B 混合于 2L 的密闭容器中,发生下列反应:3A(g)+B(g) xC(g) +2D(g),经2min 后测得D 的浓度为 0.5mol·L-1,c(A)∶c(B)=3∶5,以 C 表示的平均速率 v(C)=0.25mol·L-1·min-1,下列说法正确的是( )
A.该反应方程式中,x=2B.2 min 时,A 的转化率为 50%
C.2 min 时,A 的物质的量为 0.75molD.反应速率 v(B)=0.25 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中A为278g/mol。B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀(图中部分反应物和生成物没有列出)。

(1)写出A、G、L的化学式A______________:G: _______________,L:______________。
(2)反应②的化学方程式 ________________________________________________。
(3)写出反应M→L的离子方程式为________________________________________。
(4)若将O敞口久置,变质过程中的现象为___________________________________,发生的化学方程式为__________________________________________________。
(5)向M溶液中投入与M等物质的量的Na2O2,反应的离子方程式是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com