
科目: 来源: 题型:
【题目】下列化学反应方程式不正确的是
A.用Cl2与石灰制取漂白粉:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
B.工业上用焦碳与石英砂制粗硅:SiO2+C![]() Si+CO2
Si+CO2
C.高温下铁与水蒸汽反应:3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
D.小苏打溶液与少量石灰水反应:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室回收废水中苯酚的过程如图所示。下列分析错误的是( )
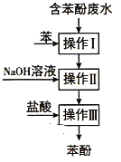
A. 操作Ⅰ中苯作萃取剂,多次萃取后检验是否萃取干净可选择三氯化铁溶液
B. 苯酚钠是离子化合物,在苯中的溶解度比在水中的小
C. 通过操作Ⅱ苯可循环使用, 三步操作均需要分液漏斗,
D. 操作中苯酚碰到皮肤,需用NaOH溶液清洗后,再用大量水不断冲洗
查看答案和解析>>
科目: 来源: 题型:
【题目】反应A(g)+ 3B(g)![]() 2C(g) + 2D(g)在四种不同情况下的反应速率分别为①v(A)= 0.15 mol/(L·s)②v(B)=0.6 mol/(L·s) ③v(C)=0.5 mol/(L·s)④v(D)=0.45 mol/(L·s)。下列表示该反应进行由快到慢的顺序正确的是( )
2C(g) + 2D(g)在四种不同情况下的反应速率分别为①v(A)= 0.15 mol/(L·s)②v(B)=0.6 mol/(L·s) ③v(C)=0.5 mol/(L·s)④v(D)=0.45 mol/(L·s)。下列表示该反应进行由快到慢的顺序正确的是( )
A.②③④①B.④③②①C.③④②①D.②④③①
查看答案和解析>>
科目: 来源: 题型:
【题目】铋为第五周期VA族元素,利用湿法冶金从辉铋矿(含Bi2S3、Bi、Bi2O3等)提取金属铋的工艺流程如下图所示:
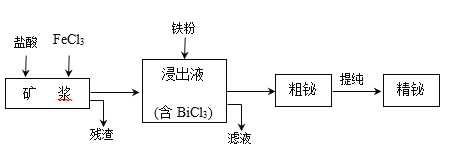
已知:BiCl3水解的离子方程式为:BiCl3+H2O![]() BiOCl+2H++2Cl。
BiOCl+2H++2Cl。
(1)矿浆浸出时加入盐酸的作用是____。
(2)浸出时,Bi溶于FeCl3溶液的化学方程式为____。
(3)残渣中含有一种单质,该单质是_______。
(4)滤液的主要溶质是(化学式)_____,该物质可在工艺中转化为循环利用的原料,转化的反应方程式为____。
(5)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,银元素以______(填化学式)进入残渣中。
(6)粗铋电解精炼时应放在_______极。
(7)某温度下饱和的Ag2S溶液中,银离子的浓度为10-4mol/L,且Ag2S的KSP=5.8×10-39,则此溶液中硫离子的浓度为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中药狼把草的成分之一M具有清炎杀菌作用,M的结构如图所示,下列叙述正确的是( )
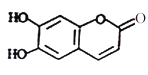
A. M的相对分子质量是180
B. 1molM最多能与4molH2发生反应
C. M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H5O5Na3
D. 1molM与足量NaHCO3反应能生成2molCO2
查看答案和解析>>
科目: 来源: 题型:
【题目】葡萄糖酸亚铁(C6H11O7) 2Fe是常用的补铁剂,易溶于水。用下图装置制备 FeCO3,提取出的 FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:

Ⅰ.(1)如何检验 A 装置的气密性?____。
(2)B中加入药品Na2CO3,要使A中制得的FeSO4溶液进入B中发生反应,实验开始时,应打开分液漏斗的活塞、______,关闭_____,一段时间后,关闭_______,打开_____(填旋塞的编号)。
(3)将制得的碳酸亚铁悬浊液过滤、洗涤。如何证明沉淀已经洗涤干净_________。
(4)将葡萄糖酸与碳酸亚铁混合,反应的化学方程式为(有机物用分子式表示)_____。
(5)从环境保护的角度分析,该装置存在不足之处,请写出改正措施__________。
Ⅱ.某补铁剂的主要成分是硫酸亚铁,用氧化还原滴定法可测定该补铁剂中铁元素的含量,实验的主要步骤如下:
①取10片补铁剂样品,溶解除去不溶物(不损耗铁元素),并配成100mL待测溶液。
②量取20.00mL待测液于锥形瓶中。
③用cmol·L1的酸性KMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积,重复两次实验,平均消耗KMnO4溶液体积为VmL。
(6)上述实验中应该用稀硫酸酸化KMnO4溶液,如果用硝酸对KMnO4溶液进行酸化,对测定结果的影响是_____(填“偏大”“偏小”或“无影响”)。滴定终点的实验现象为_____。
(7)每片补铁剂含铁元素的质量为________________g(用代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】第 VIII 族元素,跟主族元素的金属相比,它们有熔、沸点高、硬度高、密度大等特点,并有良好的延展性和高导电、导热性。下列有关它们及其化合物的结构与性质,请填写:
(1)在[Ni(NH3)6]2+中,Ni2+与NH3之间形成的化学键称为________,提供孤对电子的成键原子是________。
(2)①Co元素形成CoCl3·4NH3(绿色)和CoCl3·4NH3(紫色)各1mol,分别与足量硝酸银溶液反应,都得到1molAgCl沉淀。两种配合物中配合离子的配位数都是________,CoCl3·4NH3(绿色)和CoCl3·4NH3(紫色)的组成相同而颜色不同的原因是________。
②Co(OH)2为两性氢氧化物,在浓的强碱溶液中可以形成[Co(OH)4]2。写出Co(OH)2酸式电离的电离方程式__________。
(3)与 Co 属于同周期同族的过渡元素A,其基态原子排布中有四个未成对电子。
①由此元素可构成固体X,区别X为晶体或非晶体的方法为______________。
②A可与CO反应生成A(CO) 5 ,常压下熔点为-20.3℃,沸点为103.6℃,该晶体类型是______________。
③A3+与SCN不仅能以1:3的个数比配合,还可以其它个数比配合。若 A3+与SCN以1:4 的个数比配合,则ACl3与KSCN在水溶液中发生反应的化学方程式可表示为_______。
④A 可与另两种元素B、C构成某种化合物,B、C的外围电子排布分别为3d104s1、3s23p4,其晶胞如图所示,则其化学式为_________。
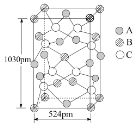
该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d=__________g﹒cm3。(保留两位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】A~G七种物质的转化关系如图所示(部分反应物、产物和反应条件未标出)。其中,A、B为中学化学常见的金属单质,C是淡黄色固体,D既能与强酸溶液反应,又能与强碱溶液反应,F溶液中加入AgNO3溶液产生不溶于稀硝酸的白色沉淀,E和G焰色反应均呈黄色。①、④均为燃烧反应。
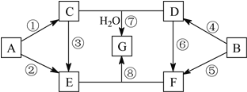
请回答下列问题:
(1)D的化学式____________,G的化学式____________。
(2)按要求写出下列反应的方程式:
③的化学方程式:___________________,
B与E的溶液反应的离子方程式:________________。
(3)将E的溶液逐滴加入到F的溶液中至过量,其现象是_____,总反应的离子方程式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图,CPAE是蜂胶的主要活性成分,也可由咖啡酸合成.下列说法不正确的是

A.咖啡酸分子中所有碳原子可能处在同一个平面上
B.1molCPAE与足量的溴水反应,最多消耗3molBr2
C.1mol苯乙醇在O2中完全燃烧,需消耗10molO2
D.1molCPAE与足量的NaOH溶液反应,最多消耗3molNaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】实验法是化学重要的研究物质性质的基本方法。某化学研究小组进行了如下实验,请回答问题。
(1)用脱脂棉包住过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,看到脱脂棉剧烈燃烧起来。
①由上述实验现象所得到的有关过氧化钠跟水反应的结论是:第一,有氧气生成;第二,____________。Na2O2跟水的反应中,水在反应中的作用是________。
a.氧化剂 b.还原剂
c.既是氧化剂,又是还原剂 d.既不是氧化剂,又不是还原剂
②该研究小组拟用如图所示装置(气密性良好)证明上述结论,用以验证第二条结论的实验操作及现象是:____________。
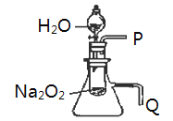
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体SO2。甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中有Fe2+,应选用的试剂编号为_____。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
写出相应的离子方程式:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com