
科目: 来源: 题型:
【题目】环氧树脂因其具有良好的机械性能、绝缘性能以及与各种材料的粘结性能,已广泛应用于涂料和胶黏剂等领域。下面是制备一种新型环氧树脂G的合成路线:


已知以下信息:

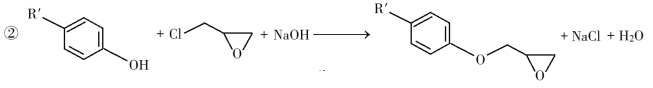
 回答下列问题:
回答下列问题:
(1)A是一种烯烃,化学名称为__________,C中官能团的名称为__________、__________。
(2)由B生成C的反应类型为__________。
(3)由C生成D的反应方程式为__________。
(4)E的结构简式为__________。
(5)E的二氯代物有多种同分异构体,请写出其中能同时满足以下条件的芳香化合物的结构简式__________、__________。
①能发生银镜反应;②核磁共振氢谱有三组峰,且峰面积比为3∶2∶1。
(6)假设化合物D、F和NaOH恰好完全反应生成1 mol单一聚合度的G,若生成的NaCl和H2O的总质量为765g,则G的n值理论上应等于__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为_______,其沸点比NH3的_______(填“高”或“低”),其判断理由是_________________________。
(2)Fe成为阳离子时首先失去______轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为______________________。
(3)比较离子半径:F__________O2(填“大于”等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。
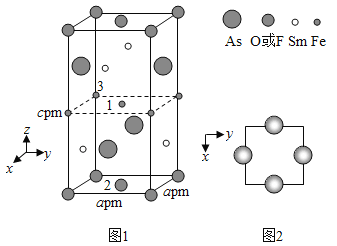
图中F和O2共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为____________,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=________g·cm3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ),则原子2和3的坐标分别为__________、__________。
),则原子2和3的坐标分别为__________、__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来流行喝苹果醋。苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等作用的保健食品。苹果酸(α羟基丁二酸)是这种饮料的主要酸性物质,其结构如下图所示:

下列相关说法正确的是( )
A. 苹果酸在一定条件下能发生消去反应
B. 苹果酸在一定条件下能催化氧化生成醛
C. 苹果酸在一定条件下能发生加聚反应生成高分子化合物
D. 1 mol苹果酸与NaHCO3溶液反应最多消耗3 mol NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)下列说法正确的是
A. 按系统命名法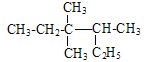 的名称为3,3-二甲基-2-乙基戊烷
的名称为3,3-二甲基-2-乙基戊烷
B. 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
C. 分子式为C5H12O的醇共有8 种,其中能催化氧化成醛的同分异构体有3 种
D. 聚乙烯( PE)和聚氯乙烯( PVC)的单体都是不饱和烃,这些单体均能使溴水褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料,它们的结构简式如下所示:
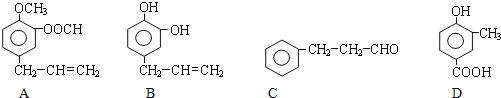
请回答下列问题:
(1)用A、B、C、D填空:
①既能使FeCl3溶液显色又能和NaHCO3溶液反应放出气体的有__________。
②能发生银镜反应的有__________。
(2)1molB最多能与_____molBr2发生反应,C中所含官能团的名称为________;
(3)按下图C经一步反应可生成E,E是B的同分异构体.则反应①属于____________反应

E到F转化过程中除用到催化剂外,还用到一种试剂G是_________(写结构简式)
(4)写出反应①的化学方程式:________;反应②的化学方程式:_________。
(5)同时符合下列两项要求的D的同分异构体有4种:
①化合物是1,2-二取代苯;
②苯环上的两个取代基分别为羟基和含有-COO-结构的基团。其中两种(G和H)结构简式如下图所示,请补充另外两种。

____________、______________
查看答案和解析>>
科目: 来源: 题型:
【题目】Q、R、X、Y、Z五种元素的原子序数依次递增。
已知:①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布为msnmpn;
③Q、X原子p能级的电子数分别为2和4。请回答下列问题:
(1)Z2+的核外电子排布式是___;基态Q原子的价电子排布图为_____。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是____(填字母)。
a.稳定性:甲>乙 b.沸点:甲<乙
(3)Q、R、X三种元素的第一电离能数值由小至大的顺序为_____(用元素符号作答)。
(4)五种元素中,电负性最大的非金属元素是___,电负性最小的非金属元素是___。(用元素符号作答)。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)金刚石、晶体硅、碳化硅,属于____晶体,其熔化时克服的微粒间的作用力是______。
(2)HF、HBr、HI形成的晶体,沸点由高到低的顺序为:_______________。
(3)NH3易液化,解释原因:_______,NH3分子的空间构型为____________。
(4)MgO的熔点比CaO的高,其原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ![]() 利用下图装置验证同主族元素非金属性的变化规律。
利用下图装置验证同主族元素非金属性的变化规律。
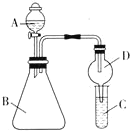
(1)若要证明非金属性:Cl>I,A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气![]() ,C中加淀粉碘化钾溶液,观察到C溶液中的现象是__________,即可证明。可用__________溶液吸收尾气。
,C中加淀粉碘化钾溶液,观察到C溶液中的现象是__________,即可证明。可用__________溶液吸收尾气。
(2)若要证明非金属性:C>Si,则在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,观察到C中溶液的现象是__________,即可证明。但有的同学认为盐酸具有挥发性,应用__________溶液除去。
Ⅱ![]() 利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
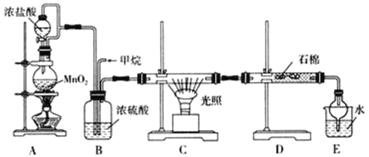
(1)A中制取氯气反应的化学方程式是_______________。
(2)D装置中的石棉上吸附着潮湿的KI粉末,其作用是__________。
(3)E装置的作用是_________(填序号)。
A.收集气体 B. 吸收氯气 C.吸收氯化氢
(4)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是__________。
(5) 将1molCH4与Cl2发生取代,测得4种有机取代物的物质的量相等,则消耗的氯气的物质的量是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)Fe(CO)5中铁的化合价为0,写出铁原子的简化的基态电子排布式______,Fe在周期表中第______周期______族,属于_______区。
(2)已知Fe(CO)5常温下呈液态,熔点为﹣20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体为________(填晶体类型)。
(3)金属铁单质的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。
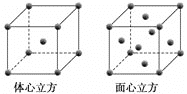
体心立方晶胞和面心立方晶胞中实际含有的铁原子个数之比为________;Fe原子配位数之比为____。若两种晶体中最邻近的铁原子间距离相同,则体心立方晶胞和面心立方晶胞密度之比为_______。
(4)已知:Y原子最高价氧化物对应水化物的酸性最强。铜与Y形成化合物的晶胞如图所示(黑点代表铜原子,空心圆代表Y原子)。
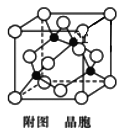
①该晶体的化学式为________。(用元素符号表示)
②已知该晶体的密度为ρ g/cm3,阿伏加德罗常数为NA,则该晶胞边长为______nm(只写计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家从化肥厂生产的(NH4)2SO4中检出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42- 和N4H44+ 两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子,N4分子不能被植物吸收。请回答下列问题:

(1)下列相关说法中,正确的是________(填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 molπ键
c.白磷的沸点比N4高,是因为P-P键键能比N-N键能大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
(2)叠氮化物是研究较早的含全氮阴离子的化合物,如:氢叠氮酸(HN3)、叠氮化钠(NaN3)等。根据等电子体理论写出N3- 的电子式_______;叠氮化物能形成多种配合物,在[Co(N3)(NH3)5]SO4,其中钴显 ____ 价,它的配体是 __________
(3)六方相氮化硼晶体内B-N键数与硼原子数之比为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com