
科目: 来源: 题型:
【题目】根据合成氨反应的能量变化示意图,下列有关说法正确的是( )
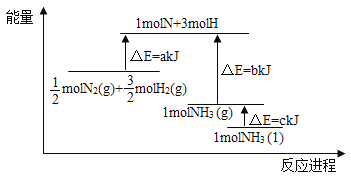
A. 若合成氨反应使用催化剂,反应放出的热量增多
B. 断裂0.5moIN2(g)和1.5molH2(g)中所有的化学键释放akJ热量
C. 2NH3(l)= N2(g)+3H2(g) △H=2(b+c-a) kJ/mol
D. N2(g)+3H2(g)=2NH3(g) △H=-2(a-b)kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】氮循环是生态系统物质循环的重要组成部分,人类活动影响了氮循环中的物质转化,如图所示。下列说法中,不正确的是

A.固氮过程中,发生了氧化还原反应
B.硝化过程需要有氧化剂参与
C.反硝化过程有助于稳定N2在大气中的含量
D.同化过程,氮元素从有机物转移至无机物
查看答案和解析>>
科目: 来源: 题型:
【题目】煤矸石是采煤过程和洗煤过程中排放的固体废物,其主要成分是Al2O3、SiO2,此外还含有FeO、Fe2O3等杂质。煤矸石经处理后,可用于制备铵明矾等。
已知:i.SiO2不与硫酸反应;Al2O3能与H2SO4反应。
ii.Fe3+、Fe2+、Al3+开始沉淀、完全沉淀的pH如表所示。
Fe2+ | Fe3+ | Al3+ | |
开始沉淀的pH | 6.3 | 1.5 | 3.4 |
完全沉淀的pH | 8.3 | 2.8 | 4.7 |
iii.NH4Al(SO4)2·12H2O的摩尔质量为453g·mol-1。
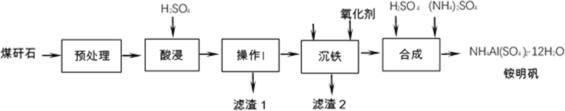
(1)酸浸过程中,Fe2O3与硫酸反应的离子方程式为___________
(2)下列说法中,正确的是___________(填字母)。
a.预处理时,粉碎煤矸石有利于提高酸浸反应速率 b.操作I是过滤 c.滤渣1中一定含有硅元素
(3)沉铁过程中,加入氧化剂的作用是___________
(4)制备过程中,若需检验滤渣1中含有![]() ,实验方案为:取少量滤渣1的洗涤液,向其中加入___________(填试剂和现象),说明其中含有
,实验方案为:取少量滤渣1的洗涤液,向其中加入___________(填试剂和现象),说明其中含有![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验,请回答下列问题:
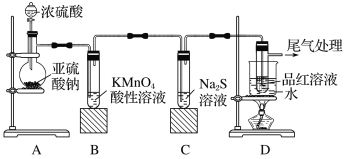
(1)装置A中盛放亚硫酸钠的仪器名称是__。
(2)实验过程中,装置B中发生的现象是__,说明SO2具有的性质是__。
(3)装置B中发生反应的离子方程式为__。
(4)尾气可采用__溶液吸收,离子方程式为:__。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:①Fe+H2SO4(稀)=FeSO4+H2↑;②Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。试回答下列问题:
CuSO4+2H2O+SO2↑;③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。试回答下列问题:
(1)当反应①转移3mol电子时,产生氢气的体积(标准状况)__L。
(2)反应②中__作氧化剂,__是氧化产物。
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是__。
(4)用单线桥法表示反应②电子转移的方向和数目__(在化学方程式上标出):Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑。
CuSO4+2H2O+SO2↑。
(5)反应③中氧化产物与还原产物的物质的量之比为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列10种物质①熔融的氢氧化钠②蔗糖③纯净的盐酸④金属钠⑤硫酸⑥二氧化硫⑦硫粉⑧偏铝酸钠溶液⑨酒精溶液⑩液氨(注意:下面前三问的答案请填序号!)
(1)属于电解质的有__。
(2)属于非电解质的有__。
(3)上述状态下的电解质能导电的有__。
(4)偏铝酸钠溶液中通足量二氧化碳反应的离子方程式:__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
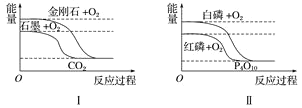
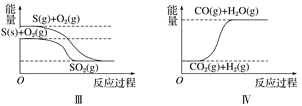
据此判断下列说法中正确的是 ( )
A. 白磷比红磷稳定
B. 石墨转变为金刚石是吸热反应
C. S(g)+O2(g)=SO2(g) ΔH1 S(s)+O2(g)=SO2(g) ΔH2 则ΔH1>ΔH2
D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目: 来源: 题型:
【题目】镁、铝的混合物共0.2mol,溶于200mL4mol·L-1的盐酸溶液中,然后再滴加2 mol·L-1的NaOH 溶液。若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示。请回答下列问题:
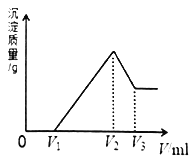
(1)当V1=160mL时,则金属粉末中m(Al)=_____________mol。
(2)V2~V3段发生反应的离子方程式为____________________________。
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则加入NaOH 溶液的体积V(NaOH)=____________mL。
(4)若镁、铝的混合物仍为0.2mol,其中镁粉的物质的量分数为a,改用200mL4 mol·L-1的硫酸溶解此混合物后,再加入840mL 2 mol·L-1的NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫和氮及其化合物在生产生活中应用广泛。请回答:
(1)已知反应:3NO2+H2O=2HNO3+NO,该反应中的氧化剂与还原剂的质量比为_____。
(2)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是____________。
A. 氨气易液化,液氨可作制冷剂 B. 可用排水法收集氨气
C. 氨气是一种无色无味的气体 D. 向氨水中滴加酚酞,溶液变红
(3)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为______________________________。
(4)实验室用金属铜和稀硝酸制取NO的离子方程式为_____________。
(5)汽车尾气常含有NO、NO2、CO等,会污染空气。在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式为__________________________。
(6)19.2 g铜投入100 mL 14 mol/L浓HNO3溶液中,充分反应后无固体剩余,收集到标准状况下气体8.96 L(气体为NO、NO2),向反应后的溶液中加入______mL 10 mol/L NaOH溶液才能使Cu2+完全沉淀。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO、CO2是化石燃料燃烧的主要产物。
(1)将含0.02mol CO2和0.01 mol CO的混合气体通入有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,充分反应后,固体质量增加_____g。
(2)已知:2CO(g)+O2(g)==2CO2(g) △H=-566.0kJ/mol,键能Eo-o=499.0kJ/mol。则反应:CO(g)+O2(g)![]() CO2(g)+O(g)的△H=_________kJ/mol。
CO2(g)+O(g)的△H=_________kJ/mol。
(3)在某密闭容器中发生反应:2CO2(g)![]() 2CO(g)+O2(g),1molCO2在不同温度下的平衡分解量如图所示。
2CO(g)+O2(g),1molCO2在不同温度下的平衡分解量如图所示。

①恒温恒容条件下,能表示该可逆反应达到平衡状态的有___(填字母)。
A.CO的体积分数保持不变 B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内,消耗CO的浓度等于生成CO2的浓度
②分析上图,若1500℃时反应达到平衡状态,且容器体积为1L,则此时反应的平衡常数K=___(计算结果保留1位小数)。
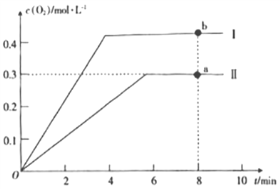
③向2L的恒容密闭容器中充入2molCO2(g),发生反应: 2CO2(g)![]() 2CO(g)+O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II所示。图中曲线I表示相对于曲线II仅改变一种反应条件后,c(O2)随时间的变化,则改变的条件是____;a、b两点用CO浓度变化表示的净反应速率关系为va(CO)____(填“>”“<”或“=”)vb(CO)。
2CO(g)+O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II所示。图中曲线I表示相对于曲线II仅改变一种反应条件后,c(O2)随时间的变化,则改变的条件是____;a、b两点用CO浓度变化表示的净反应速率关系为va(CO)____(填“>”“<”或“=”)vb(CO)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com