
科目: 来源: 题型:
【题目】已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,下列关于X、Y、Z、W四种元素的描述,不正确的是( )
A. 原子半径:X>Y>Z>WB. 原子序数:Y>X>Z>W
C. 原子最外层电子数:Z>W>Y>XD. 金属性:X>Y,还原性:W2->Z-
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是重要的化工原料,可用于制备丙烯、氢气等。
(1)MTO法由甲醇制备丙烯时的反应原理是:甲醇先脱水生成二甲醚,然后二甲醚与甲醇的平衡混合物脱水转化为含丙烯较多的低聚烯烃。某温度下,在密闭容器中加入CH3OH气体,发生脱水反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
物质 | CH3OH | CH3OCH3 | H2O |
5min浓度(mol·L-1) | 0.44 | 0.6 | 0.6 |
10min浓度mol·L-1) | 0.04 | 0.8 | 0.8 |
15min浓度(molL-1) | 0.04 | 0.8 | 0.8 |
该温度下,反应的平衡常数数值是___,CH3OH的平衡转化率是___。
(2)利用甲醇水蒸气重整制氢法是获得氢气的重要方法。反应原理如下:
反应i(主反应):CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)△H=+49kJmol-1
CO2(g)+3H2(g)△H=+49kJmol-1
反应ii(副反应):H2(g)+CO2(g)![]() CO(g)+H2O(g)△H=+41kJmol-1
CO(g)+H2O(g)△H=+41kJmol-1
①温度高于300℃则会同时发生CH3OH转化为CO和H2的副反应,该反应的热化学方程式是___。
②反应中,经常使用催化剂提高化学反应速率,但催化剂对反应具有选择性。一定条件下,测得CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。

从图中可知,反应的适宜温度为___,随着温度的升高,催化剂对___(填“反应i”或“反应ii”)的选择性越低。
③TiO2纳米电极电化学还原法可将副产物CO2在酸性水溶液中电解生成甲醇,生成甲醇的电极反应式是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物的结构简式为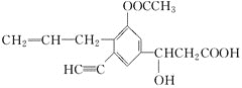 ,分析其结构,并回答下列问题:
,分析其结构,并回答下列问题:
(1)写出其分子式:____________________________________________。
(2)其中含有____个不饱和碳原子,分子中有____个双键。
(3)分子中的极性键有__________(写出2种即可)。
(4)分子中的饱和碳原子有______个,一定与苯环处于同一平面的碳原子有______个。
(5)分子中C—C===O键角约为__________,H—C≡C键角约为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,X、Y、Z、P分别为构成生物大分子的基本单位,请回答下列问题:

(1)Ⅰ在小麦种子中主要是指________,其单体X为_________是细胞生命活动所需的主要能源物质。
(2)物质Ⅲ是_______,其元素组成有___________等。
(3)在细胞中含量最高的有机物是___________(填字母),它能与双缩脲试发生作用,产生_____色反应。(4)物质Y是___________,组成Ⅱ的Y有4种,Y的种类与组成它的_________种类有关。
(5)细胞内良好的储能物质是_______,它属于脂质,脂质还有两类物质,其中________是细胞膜及细胞器膜等的重要成分,而固醇包括胆固醇、________和______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
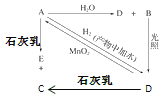
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+H2O(离子方程式):_____________;
A+石灰乳(化学方程式):______________;
E露置在空气中的第1个化学方程式:___________。
(3)漂白粉的有效成分是________(化学名称),保存漂白粉的方法__________、______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】吡唑类化合物是重要的医用中间体,如图是吡唑类物质L的合成路线。
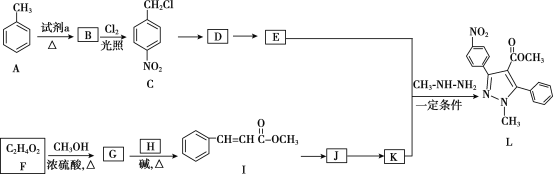
已知:R1—CHO+R2CH2—COOR3![]()
R1—CHO+R2NH2![]() R1—CH=N—R2
R1—CH=N—R2
(1)试剂a是__。
(2)C生成D的反应类型是__。
(3)D生成E的化学方程式是___。
(4)生成G的化学方程式是__。
(5)H的结构简式是__。
(6)写出符合下列条件的I的同分异构体的结构简式__。
a.是反式结构
b.能发生银镜反应
c.苯环上的一氯代物有2种
d.1mol该有机物能与2mol氢氧化钠反应
(7)K的分子式是C10H8O2,K的结构简式是__。
(8)以2-甲基丙烯和乙酸为原料,选用必要的无机试剂,合成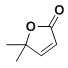 ,写出合成路线__(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线__(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验。
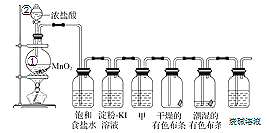
请按要求回答下列问题:
(1)仪器②的名称___________,①中反应的离子方程式__________
(2)浓盐酸的作用_______、______________,饱和食盐水的作用__________
(3)淀粉KI溶液中观察到的现象是______________,反应的离子方程式为________。
(4)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放的是________(填名称)。
(5)Cl2与烧碱溶液反应制取84消毒液的化学方程式为________。
(6)该兴趣小组用0.2mol 二氧化锰与足量的浓盐酸制备氯气,则理论上最多可制得氯气的质量是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】碲(Te)元素在元素周期表中位于第ⅥA族,其単质是重要的工业原料。工业上可用电解法从铜阳极泥(主要成分是Cu2Te、含Ag、Au等杂质)中提取单质碲,歩驟如下:
①将铜阳极泥在空气中焙烧使碲转化为TeO2;
②用NaOH溶液碱浸;
③以石墨为电极电解②所得溶液获得Te。
已知:TeO2微溶于水,易与较浓的强酸、强碱反应
下列说法不正确的是( )
A.Cu2Te中,Te的化合价是-2
B.歩骤②中,碱浸的子离方程式是:TeO2+2OH-=TeO32-+H2O
C.歩骤③中,阴极上发生反应的电极方程式是:TeO32-+4e-+6H+=Te+3H2O
D.在阳极区溶液中检验出有TeO42-存在,可能原因是阳极生成的氧气氧化TeO32-得到TeO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃下,水中碳酸化合物的三种微粒占总浓度的百分比随pH变化如图所示。25℃时,向10mL0.1molL-lNa2CO3溶液中逐滴加入0.1molL-1稀盐酸,下列说法正确的是( )

A.0.1molL-lNa2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B.溶液pH=8.3时,c(Na+)=c(C1-)
C.溶液pH=7时,加入盐酸体枳大于10mL
D.溶液pH=6时的导电能力强于pH=11时的导电能力
查看答案和解析>>
科目: 来源: 题型:
【题目】无机物转化题。请根据下列物质之间的转化回答下列问题:
Na![]() Na2O2
Na2O2![]() NaOH
NaOH![]() Na2CO3
Na2CO3
(1)写出第①步反应的化学方程式并用双线桥法标出该反应的电子转移方向及数目________
(2)第②步反应的化学方程式_________,若将第②步反应所得产物称取40克,配制成1L的溶液,其物质的量浓度是________, 再将所配的溶液加水稀释到2L,其物质的量浓度是______________。
(3)第③步反应的离子方程式_______,上述①②③反应中属于氧化还原反应的是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com