
科目: 来源: 题型:
【题目】如图是H2 和Cl2 反应生成HCl的能量变化示意图,由图可知( )
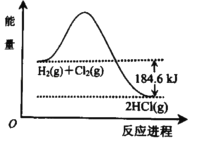
A. 反应物的能量总和小于生成物的能量
B. 生成1molHCl(g)需吸收92.3kJ的能量
C. H2(g)+Cl2(g)=2HCl(g)△H=﹣184.6 kJmol﹣1
D. H2(g)+Cl2(g)=2HCl(g)△H=﹣184.6 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式的书写及评价,均合理的是
选项 | 离子方程式 | 评价 |
A | 用铜电极电解饱和KCl溶液:2H2O+2Cl- | 正确:Cl-的失电子能力比OH-强 |
B | 向CuSO4溶液中通入过量的H2S气体:Cu2++H2S=CuS↓+2H+ | 错误:H2S的酸性比H2SO4弱 |
C | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO3- +OH- ═BaCO3↓+H2O | 错误:Ba2+与HCO3-系数比应为1:2 |
D | 过量SO2通入到NaClO溶液中:SO2+ClO- +H2O= HClO+HSO3- | 正确:H2SO3的酸性比HClO强 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA代表阿伏加德罗常数,下列说法中正确的是( )
A.18g水中含有的氢原子数目为NA
B.1 mol氩气分子所含的原子数目为2NA
C.106g碳酸钠中含有的钠离子为2NA
D.含0.5 mol HNO3的硝酸溶液中含有的氧原子为1.5 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】在粗食盐中除泥沙外,还含Na2SO4、MgCl2、CaCl2等杂质,工业制精盐除杂时,常常加入过量的除杂剂,现提供下列试剂:a.NaOH溶液;b.盐酸;c.BaCl2溶液;d.Na2CO3溶液,则加入试剂和操作不正确的是( )
A.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
B.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
C.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
D.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )

A. 原子半径的大小顺序为:r(W)>r(Y)>r(Z)
B. 元素W的最高价氧化物对应的水化物是强酸
C. 元素Y和元素Z的最高正化合价相同
D. 气态氢化物的稳定性:X<Y<Z<W
查看答案和解析>>
科目: 来源: 题型:
【题目】为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
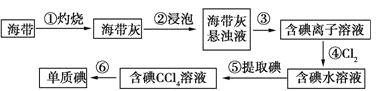
已知步骤④中反应的化学方程式是Cl2+2KI=2KCl+I2。请填写下列空白:
(1)步骤③的操作名称是___________。
(2)选用四氯化碳从碘水中萃取碘的原因是
①碘易溶于四氯化碳而难溶于水②_________③四氯化碳与水互不反应
(3)从碘水溶液中提取碘,要求从分液漏斗上口倒出水层,还可以选用下列________(填字母)物质作为萃取剂。
a.酒精 b.苯(密度比水小) c.氯化钠溶液 d.二硫化碳(密度比水大)
查看答案和解析>>
科目: 来源: 题型:
【题目】三草酸合铁酸钾K3[Fe(C2O4)3]xH2O晶体是一种亮绿色的晶体,是制备负载型活性铁催化剂的主要原料,也是一种有机反应良好的催化剂。已知M(K3[Fe(C2O4)3])=437g/mol。本实验以(NH4)2Fe(SO4)26H2O(硫酸亚铁铵晶体)为原料,加入草酸(H2C2O4)制得草酸亚铁(FeC2O4)后,在过量的草酸根(C2O42-)部分实验过程如下:
![]()
(1)在沉淀A中加入饱和K2C2O4溶液,并用40℃左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌。此过程需保持温度在40℃左右,可能的原因是:______
(2)某兴趣小组为知道晶体中x的数值,称取1.637g纯三草酸合铁酸钾(K3[Fe(C2O4)3]xH2O)晶体配成 100ml 溶液,取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4,用浓度为 0.05000molL-1的KMnO4标准溶液进行滴定。其中,最合理的是______(选填 a、b)。由如图KMnO4滴定前后数据,可求得x=______。
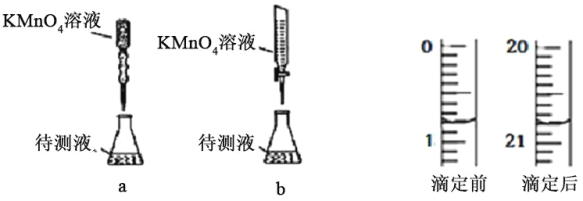
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数值。如图表示N2O在Pt2O+表面与CO反应转化成无害气体的过程。下列说法正确的是

A.N2O转化成无害气体时的催化剂是Pt2O2+
B.每1mol Pt2O+转化为Pt2O2+得电子数为3NA
C.将生成的CO2通人含大量SiO32-、Na+、Cl-的溶液中,无明显现象
D.1g CO2 、N2O的混合气体中含有电子数为0.5NA
查看答案和解析>>
科目: 来源: 题型:
【题目】以含锂电解铝废渣(主要含 AlF3、 NaF、LiF、CaO ) 和浓硫酸为原料,制备电池级碳酸锂,同时得副产品冰晶石,其工艺流程如下:

已知LiOH易溶于水,Li2CO3微溶于水。回答下列问题:
(1)电解铝废渣与浓硫酸反应产生的气体化学式为 ___________。滤渣2的主要成分是(写化学式)_________。
(2)碱解反应中, 同时得到气体和沉淀反应的离子方程式为_____________。
(3)一般地说 K>105 时,该反应进行得就基本完全了。苛化反应中存在如下平衡:Li2CO3(s)+Ca2+(aq)2Li+(aq)+ CaCO3(s)通过计算说明该反应是否进行完全________(已知Ksp(Li2CO3) = 8.64×10-4、Ksp(CaCO3) = 2.5×10-9)。
(4)碳化反应后的溶液得到Li2CO3的具体实验操作有:加热浓缩、______、______、干燥。
(5)上述流程得到副产品冰晶石的化学方程式为__________。
(6)Li2CO3是制备金属锂的重要原料, 一种制备金属锂的新方法获得国家发明专利,其装置如图所示:

工作时电极 C 应连接电源的______极,阳极的电极反应式为__________ 。该方法设计的 A 区能避免熔融碳酸锂对设备的腐蚀和因________逸出对环境的污染。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D为短周期元素,请根据下表信息回答问题。
元素 | A | B | C | D |
性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
(1)B在元素周期表的位置:___;B气态氢化物的电子式___。
(2)C的最高价氧化物分别与强酸、强碱反应的离子方程式为___、___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com