
科目: 来源: 题型:
【题目】(1)同温同压下,同体积的SO2与SO3质量之比为________,氧原子个数之比为________。
(2)在标准状况下,14g某气体的体积为11.2L,则该气体的相对分子质量是______________。
(3)在溶液中0.2 mol MnO4- 恰好能使0.5 mol SO32-离子完全氧化为SO42-,则Mn元素被还原后的化合价是________(填选项)。
A. +2 B. +3 C. +4 D. +5
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物A能使溴水褪色,E能与NaHCO3反应,且标准状况下1molE与足量Na反应能产生11.2L气体。A的一系列反应如图(部分反应条件及产物略去):
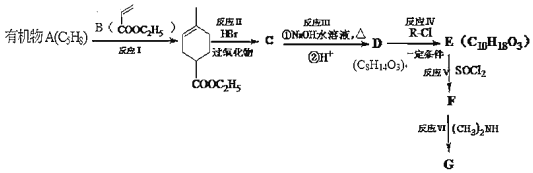
已知:(1)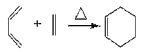
(2)![]()
![]()
![]()
(3)RCOOH![]() RCOCl
RCOCl ![]() RCON(CH3)2
RCON(CH3)2
回答下列问题:
(1)D的结构简式为______
(2)下列说法不正确的是______
A.有机物E中的官能团是羧基和酯基 B.有机物C的分子式为C10H17O2Br
C.反应Ⅲ、Ⅳ、Ⅴ、Ⅵ均属于取代反应 D.1mol有机物E最多可消耗2mol NaOH
(3)写出F→G反应的化学方程式______
(4)写出C5H9NO2满足下列条件的2种链状同分异构体的结构简式。
①红外光谱检测表明分子中含有醛基;②1H-NMR谱显示分子中有3种氢原子。______,______
(5)请设计以有机物A为原料合成(![]() )的合成路线______(用流程图表示,无机试剂任选)。
)的合成路线______(用流程图表示,无机试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19g/cm3
质量分数:36.5%
(1)该浓盐酸中HCl的物质的量浓度为______molL-1。
(2)某学生欲用上述浓盐酸和蒸馏水配480mL物质的量浓度为0.200molL-1的稀盐酸。
①配制稀盐酸时,应选用容量瓶的规格是_______mL。
②该学生需要用取___mL上述浓盐酸进行配制。
③若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)
量取浓盐酸时俯视刻度线_____,定容时仰视刻度线_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】(一)工业上,在Cu2O/ZnO 作催化剂的条件下发生反应:CO(g)+2H2(g)CH3OH(g) △H
(1)已知:CH3OH(l)=CH3OH(g) △H=+35.2kJmol-1,根据表:
物质 | H2(g) | CO(g) | CH3OH(l) |
燃烧热/kJmol-1 | -285.8 | -283.0 | -726.5 |
反应CO(g)+2H2(g)CH3OH(g) △H=______kJmol-1
(2)向2L恒容密闭容器中通入1mol CO(g)和2mol H2(g),发生反应合成甲醇,反应过程中n(CH3OH)与时间(t)及温度的关系如图1所示。在500℃恒压条件下,请在图1中画出反应体系中n(CH3OH)与时间(t)变化总趋势图。
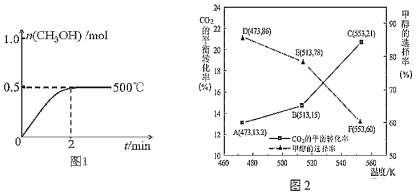 ____________
____________
(二)甲醇还可用CO2与H2在催化剂CZZA(普通铜基催化剂)作用下合成,相关反应如下:
反应ⅠCO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1=-49.2kJmol-1
反应ⅡCO2(g)+H2(g)CO(g)+H2O(g) △H2=41.2kJmol-1
(3)以CZZA/rGO为催化剂,在一定条件下,将1mol CO2与3mol H2通入恒容密闭容器中进行反应I和反应II,CO2的平衡转化率和甲醇的选择率(甲醇的选择率:转化的CO2中生成甲醇的物质的量分数)随温度的变化趋势如图2所示:
①在553K时,反应体系内CO的物质的量为______ mol
②随着温度的升高,CO2的平衡转化率增加但甲醇的选择率降低,请分析其原因:______
(三)(4)如图为氯碱工业的装置示意图,a端进入的物质为______,工业上还可以利用该装置,以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可制备四甲基氢氧化铵[(CH3)4NOH],则收集到(CH3)4NOH的区域是______(填a、b、c或d),
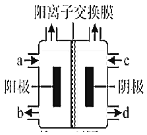
查看答案和解析>>
科目: 来源: 题型:
【题目】商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1000℃左右冶炼,可能涉及的反应有:
①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O;
2CuO+CO2↑+H2O;
②2CuO+C![]() 2Cu+CO2↑;
2Cu+CO2↑;
③CuO+CO![]() Cu+CO2;
Cu+CO2;
④CO2+C![]() 2CO。
2CO。
(1)从四种基本反应类型来看,①②④的反应类型分别为①___________,②___________,④___________。
(2)反应③中,____________发生氧化反应,__________发生还原反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质转化在给定条件下能实现的是
A.FeS2![]() SO3
SO3![]() H2SO4
H2SO4
B.NaCl(aq)![]() Na
Na![]() Na2O2
Na2O2
C.Fe![]() FeSO4(aq)
FeSO4(aq)![]() Fe(OH)2
Fe(OH)2![]() Fe2O3
Fe2O3
D.Fe2O3![]() FeCl3(aq)
FeCl3(aq)![]() Fe
Fe
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离于方程式正确的是
A. 向氯化铝溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
B. 浓盐酸与MnO2反应制取Cl2:MnO2+4HCl(浓) ![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
C. 酸性条件下,碘化钾溶液露置于空气中变质:4H++4I-+O2=2I2+2H2O
D. 向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:HCO3-+OH-=CO32-+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸合铁酸钾晶体Kx[Fe(C2O4)y]·3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程。
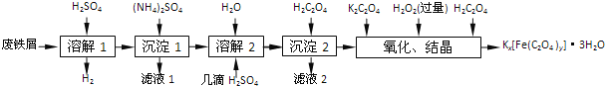
已知:(NH4)2SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
温度/℃ | 10 | 20 | 30 | 40 | 50 |
(NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
FeSO4·7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | ― |
(NH4)2SO4·FeSO4·6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)废铁屑在进行“溶解1”前,需用在5% Na2CO3溶液中加热数分钟,并洗涤干净。Na2CO3溶液的作用是________。
(2)“溶解1”应保证铁屑稍过量,其目的是___________。“溶解2”加“几滴H2SO4”的作用是________。
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、________、过滤、用乙醇洗涤、干燥。用乙醇洗涤的目的是____________。
(4)“沉淀”时得到的FeC2O4·2H2O沉淀需用水洗涤干净。检验沉淀是否洗涤干净的方法是_______。
(5)“结晶”应将溶液放在黑暗处等待晶体的析出,这样操作的原因是__________。
(6)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤[备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250 mL待测液。
步骤2:用移液管移取25.00 mL待测液于锥形瓶中,加入稀H2SO4酸化,_________,C2O42-转化为CO2被除去。
步骤3:向步骤2所得溶液中______________。
步骤4:用c mol·L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应与四种基本类型反应的关系如下图所示,则下列化学反应属于阴影部分的是( )
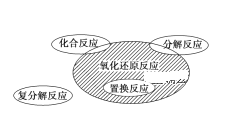
A.CO + CuO ![]() CO2 + Cu
CO2 + Cu
B.Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑
C.Fe+H2SO4=FeSO4+H2↑
D.N2+3H2 ![]() 2NH3
2NH3
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)某液体化合物X2Y4,常用做火箭燃料。16g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)==X2(g)+2Y2O(l)。冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:
①反应前O2的体积V(O2)为________。
②X2的摩尔质量为________________。
③Y元素的名称是________________。
(2)取1.43 g Na2CO3·xH2O溶于水配成50mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,共消耗盐酸20.0mL,并收集到112mLCO2(标准状况下)。
①稀盐酸物质的量浓度为________________mol·L-1
②Na2CO3·xH2O的摩尔质量为__________ g·mol-1
③x=________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com