
科目: 来源: 题型:
【题目】在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N—N键的键能为160kJ·mol-1(N2的键能为942kJ·mol-1),晶体片段结构如右图所示。又发现利用N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是( )

A. 按键型分类,该晶体中含有非极性共价键
B. 含N5+离子的化合物中既有离子键又有共价键
C. 高聚氮与N2、N3、N5、N5+、N60互为同素异形体
D. 这种固体的可能潜在应用是烈性炸药或高能材料
查看答案和解析>>
科目: 来源: 题型:
【题目】为了监测某烟道气中的NOx的含量,选用如下采样和检测方法。

I.采样步骤
①检验系统气密性;②加热器将烟道气加热至140℃;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用是___。采样步骤②加热烟道气的目的是___。
C中填充的干燥剂最好的选择是___(选填编号)。
a.碱石灰 b.无水CuSO4 c.P2O5
(2)用实验室常用仪器组装一套装置,其作用与D(装有碱液)相同,在虚线框中画出该装置的示意图,标明气体的流向及试剂___。

Ⅱ.NOx含量的测定
将一定量的气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3-,然后加入过量的FeSO4标准溶液,充分反应后,再用K2Cr2O7标准溶液滴定剩余的Fe2+。
(3)NO被H2O2氧化为NO3-的离子方程式是___。滴定操作使用的玻璃仪器主要有___。
(4)滴定过程中发生下列反应:3Fe2++NO3+4H+=NO↑+3Fe3++2H2O、Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O。判断下列情况对NOx含量测定结果的影响(填“偏高”、“偏低”或“无影响”):若缺少采样步骤③,会使测试结果___;若FeSO4标准溶液部分变质,会使测定结果___。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应的应用比较广泛。阅读下面的材料,结合相关化学知识回答下列问题。黑火药主要是硝酸钾、硫磺、木炭三者粉末的混合物,在点燃条件下,其化学反应式主要为:2KNO3+S+3C=N2↑+3CO2↑+K2S
(1)在黑火药燃烧的反应中,氧化剂为___;
(2)该反应被氧化的元素是___;
(3)该反应的氧化产物是___;
(4)KNO3中N元素的化合价是___;
(5)根据化学反应式分析,一个硫原子参与反应时转移___个电子;
(6)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。用双线桥表示反应的电子转移方向和数目:___。
(7)已知存在下列反应:①ClO3-+5Cl-+6H+ =3Cl2+3H2O ②2Fe2++Cl2=2Fe3++2 Cl-。则ClO3-、Fe3+、Cl2三种微粒氧化能力由强到弱的顺序是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合溶液中逐渐通入CO2气体至过量,生成沉淀的物质的量(n)和通入CO2气体的(V) 的关系如图所示,试回答:

(1)0到a点之间的反应的离子方程式__________
(2)a到b点之间的反应的离子方程式__________
(3)b点之后的反应的离子方程式______________
(4)c 点CO2的体积__________mL(同温同压下)。
(5) 混合溶液中Ba(OH)2和NaOH 的物质的量之比为__________
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可由氢气、氮气合成氨气,溶于水形成氨水。一定温度下,向2L固定体积的密闭容器中加入N2(g)和H2(g),发生反应:N2(g)+3H2(g)![]() 2NH3(g)+Q(Q>0),NH3物质的量随时间的变化如图所示。
2NH3(g)+Q(Q>0),NH3物质的量随时间的变化如图所示。
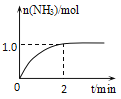
(1)0~2min内的平均反应速率v(H2)=___。
(2)该温度下,反应的平衡常数表达式K=___。
其平衡常数K与温度T的关系如下表:
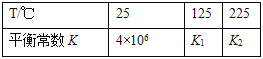
试判断K1___K2(填写“>”、“=”或“<”)。
(3)能说明该合成氨反应已达到平衡状态的是___(选填编号)。
a.3v(N2)=v(H2)
b.容器内压强保持不变
c.混合气体的密度保持不变
d.25℃时,测得容器中c(NH3)=0.2mol·L-1,c(H2)=c(N2)=0.01mol·L-1
常温下,某同学将盐酸与氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH如表。
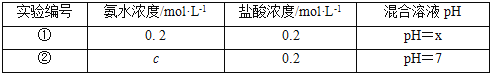
请回答:
(4)①中所得混合溶液,pH___7(填“>”、“<”或“=”);②中c__0.2(填“>”、“<”或“=”),所得混合溶液中各离子浓度大小关系为___。
(5)请你设计一个能证明一水合氨是弱电解质的简要方案___。
查看答案和解析>>
科目: 来源: 题型:
【题目】用VSEPR模型预测下列分子或离子的立体结构,其中正确的是 ( )
A. H2O与BeCl2为角形(V形) B. CS2与SO2为直线形
C. SO3与CO![]() 为平面三角形 D. BF3与PCl3为三角锥形
为平面三角形 D. BF3与PCl3为三角锥形
查看答案和解析>>
科目: 来源: 题型:
【题目】原子序数小于36的X、Y、Z、W四种元素,X基态原子的最外层电子数是其内层电子数的2倍,Y基态原子的2p原子轨道上有3个未成对电子,Z是地壳中含量最多的元素,W的原子序数为24。
(1)W基态原子的核外电子排布式为___________,元素X、Y、Z的第一电离能由大到小的顺序为___________(用元素符号表达);
(2)与XYZ-互为等电子体的化学式为___________;
(3)1molHYZ3分子中含有σ键的数目为___________;
(4)YH3极易溶于水的主要原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)质量数为37的氯原子符号为_______。
(2)S2-的结构示意图为______。
(3)氮原子的电子式为______,N2的电子式为______,NH4+的电子式为_________
(4)磷原子的核外电子排布式为______,其价电子排布式为_____,其价电子排布图为_____。
(5)含有半满p轨道的最轻原子的核外电子排布式为_______,元素名称为_______;
(6)最活泼的非金属元素原子的核外电子排布式为_______,元素名称为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硒是动物和人体所必需的微量元素之一,在周期表中信息如图所示。完成下列填空:

(1)Se元素在周期表中的位置为___。表中78.96的意义为__。Se原子最外层电子排布的轨道表示式为___。
(2)从原子结构角度解释硫的非金属性大于硒___。
(3)硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种___(选填“极性、或非极性”)分子,其空间结构为___型。
(4)工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式___。理论上该反应每转移1mol电子,可得到SeO2的质量为___g,得到SO2在标准状况下的体积为___ L。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(1)用双线桥表示出电子转移的方向和数目__,题干中反应改写成离子方程式是___。
(2)电解食盐水的过程中,氧化产物是___。
(3)电解食盐水要求对粗食盐水进行精制,以除去租食盐水中含有的泥沙和SO42-、Ca2+,Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式:___,___。
(4)请配平以下化学方程式:__Al+__NaNO3+__NaOH=__NaAlO2+__N2↑+__H2O。若反应过程中转移5mol电子,则生成标准状况下N2的体积为___L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com