
科目: 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. 加入催化剂有利于氨的合成
D. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将2molSO2和1molO2充入一固定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) △H=-197kJ/mol,当达到化学平衡时,下列说法中正确的是
2SO3(g) △H=-197kJ/mol,当达到化学平衡时,下列说法中正确的是
A.SO2和SO3共2mol B.生成 SO32mol
C.放出197kJ热量 D.含氧原子共8mo1
查看答案和解析>>
科目: 来源: 题型:
【题目】目前,世界上生产的镁有60%来自海水,其生产流程图如下:
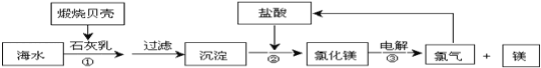
(1)贝壳的主要化学成分为_________(写化学式)。
(2)写出反应②的离子方程式:_____________。
(3)根据流程图可知,可循环利用的物质是__________。
(4)Mg与CO2反应时,有白色粉末并有黑色固体生成。请写出Mg与CO2反应的化学方程式,并用双线桥标出电子转移的方向与数目________。氧化剂是___________,氧化产物是_________。
(5)Na比Mg和Al要活泼,将Na投入到Fe2(SO4)3溶液中会发生剧烈的化学反应,其离子方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个体积为1 L的密闭容器中发生某化学反应:2A(g)![]() B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800° C,实验Ⅲ在950°C。B、C的起始浓度都为0,反应物A的浓度(mol L-1)随时间(min)的变化如图所示。试回答下列问题:
B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800° C,实验Ⅲ在950°C。B、C的起始浓度都为0,反应物A的浓度(mol L-1)随时间(min)的变化如图所示。试回答下列问题:

(1)在实验Ⅰ中,反应在2040 min内A的平均反应速率为________mol L-1min-1。实验Ⅱ和实验Ⅰ相比,可能隐含的反应条件是____________。
(2)该反应的ΔH___________0,其判断理由是_____________。
(3)实验Ⅰ第40 min末,若降低反应温度,达到新的平衡后,A的浓度不可能为________(填序号)。
A.0.35 mol·L1 B.0.4 mol·L1 C.0.7 mol·L1 D.0.8 mol·L1
(4)若反应在800°C进行,在该1 L的密闭容器中加入1 mol A、0.2 mol He,达到平衡时A的转化率应____________。
A.等于86% B.等于50% C.小于50% D.在50%86%
查看答案和解析>>
科目: 来源: 题型:
【题目】能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式:
①2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1;
②H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1;
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1;
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1;
⑤CO2(g)+2H2O(g)===2CH4(g)+2O2(g) ΔH=+890 kJ·mol-1
回答下列问题:
(1)上述反应中属于吸热反应的___________________________________________。
(2)H2的燃烧热为_______________________________________________________。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s)+H2O(g)===H2(g)+CO(g) ΔH=a kJ·mol-1;则a=________;
查看答案和解析>>
科目: 来源: 题型:
【题目】A(C2H2)是基本有机化工原料。由A制备聚乙烯醇缩丁醛和顺式异戊二烯的合成路线(部分反应条件略去)如下所示:

回答下列问题:
(1)A的名称是_______,B含有的官能团是_______________。
(2)①的反应类型是____________,⑦的反应类型是________________。
(3)C和D的结构简式分别为______________、_________________。
(4)异戊二烯分子中最多有________个原子共平面,顺式聚异戊二烯的结构简式为___________。
(5)写出与A具有相同官能团的异戊二烯的所有同分异构体__________(填结构简式)。
(6)参照异戊二烯的上述合成路线,设计一条由A和乙醛为起始原料制备1,3-丁二烯的合成路线___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知以下信息:①1 mol N2的共价键断裂吸收946 kJ的能量;1 mol H2的共价键断裂吸收436 kJ的能量;形成1 mol NH3中的化学键释放1 173 kJ的能量。②将一定量的N2和H2投入一密闭容器中,在一定条件下进行反应,测得有关数据如下:
N2(mol·L-1) | H2(mol·L-1) | NH3(mol·L-1) | |
起始时 | 3 | 3 | 0 |
2s末 | 2.6 | 1.8 | 0.8 |
根据以上相关数据回答问题:
(1)用H2表示该反应2 s内的平均反应速率为________
(2)______(填“能”或“不能”)确认该反应2 s末已达化学平衡状态。
(3)写出该反应的化学方程式:
________________________________________________________________________。
(4)氮气和氢气生成氨气的过程______(填“释放”或“吸收”)能量。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将amol氮气与bmol氢气的混合气体通入一个固定容积的密闭容器中,发生反应N2(g)+3H2(g) ![]() 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,则a值为________。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中氨气体积分数为25%,平衡时氨气的物质的量为________。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同)n始∶n平=______。
(4)原气体中a∶b=________。
(5)达到平衡时混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知2A2(g)+B2(g)![]() 2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
(1)a___(填“>”“=”或“<”)b。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将___(填“增大”“减小”或“不变”)。
(3)若在原来的容器中只加入2 mol C,500 ℃时充分反应达到平衡后,吸收热量c kJ,C的浓度___(填“>”“=”或“<”)w mol·L-1。
(4)能说明该反应已经达到平衡状态的是___。
a.v(C)=2v(B2) b.容器内压强保持不变c.v逆(A2)=2v正(B2)d.容器内气体的密度保持不变
(5)使该反应的反应速率增大,且平衡向正反应方向移动的操作是___。
a.及时分离出C气体b.适当升高温度c.增大B2的浓度 d.选择高效的催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】某氮肥厂氨氮废水中的氮元素多以NH4+和NH3![]() H2O的形式存在,该废水的处理流程如下:
H2O的形式存在,该废水的处理流程如下:
![]()
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:____________。
②用化学平衡原理解释通空气的目的:__________。
(2) 过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
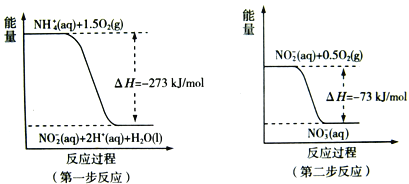
①第一步反应是_________反应(选题“放热”或“吸热”),判断依据是__________。
②1mol NH4+(aq)全部氧化成![]() 的热化学方程式是______________。
的热化学方程式是______________。
(3) 过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗![]() 转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是__________。
转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com