
科目: 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
I.已知某些化学键的键能数据如下
化学键 | C=O | C—O | C—H | H—H | O—H |
键能/kJ·mol-1 | 745 | 351 | 415 | 436 | 462 |
则CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH = __________ kJ·mol-1
CH3OH(g) + H2O(g) ΔH = __________ kJ·mol-1
II.将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(l)
CH3OCH3(g) + 3H2O(l)
(1)该反应化学平衡常数表达式K = __________。
(2)已知在某压强下,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图所示:

①该反应的ΔH __________ 0(填“>"或“<”)。
②若温度不变,减小反应投料比[n(H2)/n(CO2)],K值将____(填“增大”、“减小”或“不变”)。
(3)某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,下列物理量不再发生变化时,能说明反应达到平衡状态的是__________。
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比
(4)某温度下,在体积可变的密闭容器中,改变起始时加入各物质的量,在不同的压强下,平衡时CH3OCH3(g)的物质的量如下表所示:
P1 | P2 | P3 | |
I.2.0 mol CO2 6.0 mol H2 | 0.10 mol | 0.04 mol | 0.02 mol |
II.1.0 mol CO22 | X1 | Y1 | Z1 |
III.1.0 mol CH3OCH3 3.0 mol H2O | X2 | Y2 | Z2 |
①P1 __________ P3(填“>”“<”或“=”);
②P2下,III中CH3OCH3的平衡转化率为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)0.5molCH4含_________个电子。
(2)下列物质既能导电,又属于电解质的是_______ 。
A NaCl溶液 B铁丝 C稀硫酸 D熔融的氢氧化钠 E 盐酸 F 硫酸
(3)同温同压下,甲容器中HCl气体和乙容器中的NH3所含原子个数相等,则甲乙两容器的体积之比为________。
(4)现配制500ml 0.3mol/L稀硫酸溶液,需用量筒量取质量分数为49%,密度为1.5g/cm3的浓硫酸 _________ml。
(5)①20℃、101kPa下,1g氢气和14g氮气的体积相同;
②常温常压下,16g氧气和臭氧的混合气体中含有的质子数为8NA
③0.1L 0.5mol/LCH3CH2OH溶液中含有氢原子数为0.3NA
④常温常压下,28gCO的体积大于22.4L;
⑤分子总数相等的NO2和CO2,所含氧原子数均为2NA。
以上说法正确的是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
方法一:Fe2O3 + KNO3 + KOH===== K2FeO4 + KNO2 + H2O (未配平)
方法二:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+ 5H2O
(1)配平方法一的化学方程式___,再用双线桥标明电子转移的方向和数目___:
___Fe2O3 +___KNO3 +___KOH == ___ K2FeO4 +___ KNO2 +___ H2O
(2)方法二中的还原产物为_________ (写化学式),将方法二的化学方程式改写为离子方程式 ________ ,根据反应方程式,氧化性:KClO ________ K2FeO4(填“>”、“<”或“=”);
(3)利用方法二制备K2FeO4,若有0.5mol K2FeO4生成,转移的电子数为___________ ;
(4)在酸性溶液中,某反应的反应物和生成物有KBiO3、K2SO4、H2SO4、MnSO4、H2O、Bi2(SO4)3 和一种未知物质M。
①已知MnSO4在反应中失去电子,则该反应的氧化剂是________;
②已知该反应中被氧化的元素与被还原的元素的物质的量之比为2:5,则M的化学式为______;
③写出该反应的离子反应方程式________;
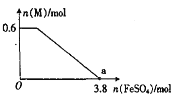
④某同学向上述反应后的溶液中逐滴加入FeSO4溶液,测得溶液中M的物质的量与FeSO4的物质的量之间的关系如图所示。已知氧化性:Fe3+>Bi3+,且a点时溶液中含Fe3+、Mn2+,则原反应体系中,起始加入的KBiO3的物质的量为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】结构决定性质,有机化合物的结构也是研究有机物性质的基础。
(1)烷基是烷烃失去一个或若干氢原子后剩下的电中性的原子团,请在方框内写出甲基的电子式_______。

(2)有一类有机物,它的一卤代物只有一种,如![]() 、
、![]() 等。请写出另外两种满足该条件烷烃的结构简式,并用系统命名法命名。
等。请写出另外两种满足该条件烷烃的结构简式,并用系统命名法命名。
结构简式 | _______ | _______ |
系统命名 | _______ | _______ |
(3)烷烃都是由共价键形成的有机物,若用I表示一个烷烃分子中的共价键数,n表示该烷烃的碳原子数,则丙烷(![]() )的共价键数
)的共价键数![]() ____________﹔若某烷烃的共价键数
____________﹔若某烷烃的共价键数![]() ,则
,则![]() ____________。
____________。
(4)烃的结构主要由碳原子的连接顺序决定,因此我们常通过键线式来表示烃的结构,其中每个端点和拐角都代表一个碳,每个碳原子连接的氢原子都不表示出来。A、B、C分别表示三种物质的空间立体结构:
A. 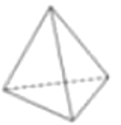 B.
B.  C.
C. 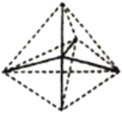
①上述结构中的C不可能是烃,理由是______________________________。
②B分子的分子式是__________________,其一氯代物共有____________种。
③在结构A的每两个碳原子之间插入一个![]() 原子团,可以形成金刚烷的结构,写出金刚烷的分子式__________________。
原子团,可以形成金刚烷的结构,写出金刚烷的分子式__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中分别是两种烃的结构模型:
A.  B.
B. 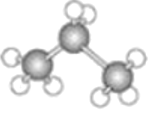
请回答下列问题:
(1)A、B两种模型分别是有机物的____________模型和____________模型。
(2)模型A可以表示分子中原子的相对位置和相对大小,以下物质的空间结构可以用模型A表示的是______。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)已知:模型B表示某烃M的结构。该烃与氯气反应生成另一有机物N,且M和N的式量相差34.5。
①写出M的结构简式:__________________。
②N的可能结构有______种。若N的分子中有2种不同化学环境的氢原子,则该过程的化学方程式是______________________________,此反应的类型是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨对人类的生产生活具有重要影响。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是____________。
②氨催化氧化生成一氧化氮反应的化学方程式是___________。
(2)氨的定量检测。水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:
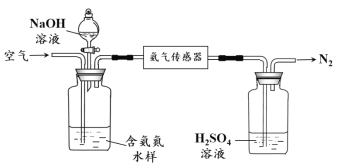
① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用:_______________。
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol,则水样中氨氮(以氨气计)含量为________mg·L-1。
(3)氨的转化与去除。 微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。
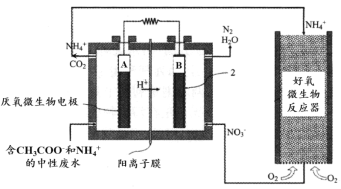
已知A、B两极生成CO2和N2的物质的量之比为5 : 2,写出A极的电极反应式:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,纵轴表示导电能力,横轴表示所加溶液的量,下列说法正确的是( )
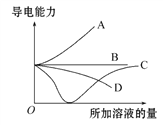
A. 曲线A表示NaOH溶液中滴加稀盐酸
B. 曲线B表示CH3COOH溶液中滴加KOH溶液
C. 曲线C表示Ba(OH)2溶液中滴加稀硫酸
D. 曲线D表示Cu(OH)2悬浊液中滴加HNO3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( )
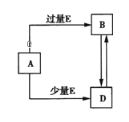
A. A、B、D可能是钠及其化合物 B. A、B、D可能是镁及其化合物
C. A、B、D可能是铝及其化合物 D. A、B、D可能是非金属及其化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应能用勒夏特列原理解释的是
A. 加入催化剂有利于氨的合成
B. 煅烧粉碎的黄铁矿矿石有利于SO2的生成
C. 硫酸生产中用98%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3
D. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表是学习化学的重要工具。回答下列问题:
(1)硅元素最外层有______种能量不同的电子,有______种运动状态不同的电子,写出其最外层电子的电子排布式__________________。
(2)![]() 的空间构型和
的空间构型和![]() 相同,写出
相同,写出![]() 的电子式:__________________。
的电子式:__________________。
(3)部分短周期元素化合价与原子序数的关系可用图示表示。

①元素X在元素周期表中的位置是__________________。
②写出元素Y和Z的最高价氧化物对应水化物反应的离子方程式:______________________________。
③第三周期主族元素中非金属性最强的两种元素是____________和____________(填元素符号),用一个化学方程式说明这两种元素非金属性的相对强弱:______________________________。
(4)第三同期元素的原子所形成的简单离子中:还原性最弱的阴离子是____________;氧化性最强的阳离子是____________。
(5)写出两种W的含氧酸的化学式____________、____________,设计一种实验方案比较两种酸的酸性强弱,写出反应的化学方程式:________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com