
科目: 来源: 题型:
【题目】磺酰氯(SO2Cl2)在医药、染料行业有重要用途,也可用于制备表面活性剂。沸点为69.2℃,遇水水解,剧烈反应生成两种强酸。学习小组在实验室用SO2和Cl2在活性炭作用下,制备SO2Cl2并测定产品纯度,设计如图实验如图1(夹持装置略去)。请回答下列问题:
Ⅰ.SO2的制备
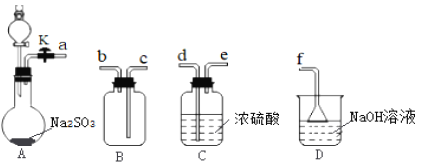
(1)欲收集一瓶干燥的SO2,装置中气流方向合理的连接顺序为____(填小写字母)。
(2)A装置分液漏斗中装的是70%的硫酸溶液,A中反应的化学方程式为____。
Ⅱ.SO2Cl2的制备和纯度的测定
将上述收集到的SO2充入注射器h中,用图2装置制备SO2Cl2。

(3)仪器e的名称为____,b中试剂的名称为____。
(4)f的作用是____。
(5)取反应后的产品4.0g,配成200mL溶液;取出20.00mL,用0.5000mol ·L-1NaOH溶液滴定;达到滴定终点时消耗标准液的体积为20.00mL(杂质不参加反应)。
①产品加水配成溶液时发生的反应为____。
②SO2Cl2的质量分数为____。(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室常用的部分仪器,请回答下列问题

(1)序号为⑧和⑩的仪器名称分别为__________、__________。
(2)在分液操作中,必须用到上述仪器中的________(填序号)。
(3)能作反应仪器且可直接加热的仪器上述中的___________(填名称)。
(4)在配制一定物质的量浓度的溶液时,需要用到的仪器是___________(填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】第19届亚洲运动会将于2022年在杭州举行,杭州的空气与水质量的提高越来越成为人们关注的问题。其中,烟气中的NOx与水中总氮含量(包括有机氮及NO3-、NO2-、NH4+等无机氮)都必须脱除(即脱硝)后才能排放。请回答下列问题:
I.空气的脱硝处理:
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1= -890.3.kJ· mol-1
N2(g)+O2(g)=2NO(g) ΔH2= +180.kJ· mol-1
(1)CH4可用于脱硝,其化学方程式为CH4(g)+4NO(g)![]() CO2(g)+2N2(g)+2H2O(l),ΔH=____kJ· mol-1。在恒温,恒容的密闭容器中通入2mol CH4和4mol NO,下列说法正确的是____。
CO2(g)+2N2(g)+2H2O(l),ΔH=____kJ· mol-1。在恒温,恒容的密闭容器中通入2mol CH4和4mol NO,下列说法正确的是____。
A.甲烷过量,可将NO完全转化为N2
B.从反应开始到平衡的过程中,NO的转化率一直增大
C.反应过程中,容器中的压强保持不变
D.平衡后,再通入一定量的甲烷,正反应速率增大
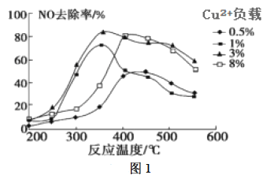
(2)C2H4也可用于烟气脱硝。为研究温度、催化剂中Cu2+负载量对其NO去除率的影响,控制其他条件一定,实验结果如图1所示。为达到最高的NO去除率,应选择的反应温度和Cu2+负载量分别是____。

II.水的脱硝处理:
(3)水中的含氮物质在好氧硝化菌的作用下有如下反应:
2NH4+(aq)+3O2(g)=2NO2-(aq)+4H+(aq)+2H2O(l)(快反应)
2NO2-(aq)+O2(g)=2NO3-(aq)(慢反应)
20℃时含氮废水(以NH4+)的NH4+的浓度随DO(水体中溶解氧)浓度的变化曲线如图2所示,在图2上画出20℃时NO2-的浓度随DO的变化趋势图。_______
(4)研究表明,用电解法除去氨氮废水(反应中视为NH4+)有很高的脱氮(转化为N2)效率,写出该过程中阳极的电极反应式____。
查看答案和解析>>
科目: 来源: 题型:
【题目】发射“神舟七号”载人飞船的是我国自行研制的“长征一号D”运载火箭。该火箭的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:![]() ,下列叙述错误的是( )
,下列叙述错误的是( )
A. 此反应是氧化还原反应
B. 反应瞬间产生大量高温气体,推动火箭飞行
C. 在此反应中![]() 作还原剂
作还原剂
D. R的分子式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,X在周期表中原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。各物质之间的转化关系如图,部分生成物省略。

请回答下列问题:
(1)写出Z在周期表中的位置____,D的结构式____。
(2)写出A的化学式____。
(3)写出反应①的离子方程式____。
(4)为了获得氯化铜晶体,需要将B溶液在HCl氛围中蒸发结晶,原因是____。
(5)将F溶于稀硝酸,溶液变成蓝色,并放出无色气体。写出该反应的化学方程式____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学用如图所示装置进行铜与浓硫酸的反应,并探究产物的性质 (夹持装置已略去)。

(1)试管①中反应的化学方程式是______;
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是______;
若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有______性。
(3)试管③中的试剂为NaOH溶液,其作用是______,反应的离子方程式是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol,若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为______ 个。
(2)该气体若溶于1L水中(不考虑反应),设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为______ mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。

(1)写出下列各物质的化学式:X:______A:______C:______F:______。
(2)写出下列变化的化学方程式:
X![]() :______;
:______;
C→E:______;
F→G:______;
(3)检验X中阳离子的方法:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关有机物结构和性质的说法错误的是
A. 分子式为C5H10O2且能与 NaHCO3反应放出气体的结构共有4种
B. 石油是混合物,可通过分馏得到汽油、煤油等纯净物
C. 苯甲酸(![]() )分子中所有原子可能位于同一平面
)分子中所有原子可能位于同一平面
D. 1mol盐酸美西律( )最多可与3 mol H2发生加成
)最多可与3 mol H2发生加成
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)“水玻璃”中溶质的化学式为____,乙二醇的结构简式为____。
(2)AlCl3熔沸点较低,熔融状态不导电,则其晶体类型为____晶体。
(3)浓硝酸需避光保存在棕色试剂瓶的原因是____。(用化学方程式解释)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com