
科目: 来源: 题型:
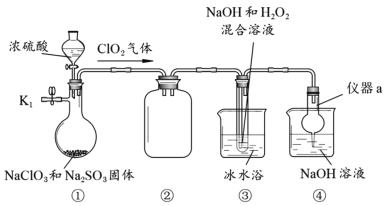
【题目】NaClO2是一种高效的杀菌消毒剂,也常用来漂白织物等。用下列装置探究NaClO2的制备。
完成下列填空:
(1)仪器a的名称为__________,装置②的作用是________________。
(2)检查装置气密性的方法是________________________________________________。
(3)关闭K1,从分液漏斗中加入一定量浓硫酸,装置③中生成NaClO2的化学方程式为2ClO2+2NaOH+H2O2→2NaClO2+2H2O+O2↑,该反应的氧化产物是_____________。
(4)实验完成后,为防止装置中残留的有毒气体污染空气,可以进行的操作是:打开止水夹K1,____________________________________________。
(5)从装置③的溶液中获得NaClO2晶体的主要操作有减压蒸发浓缩、________________、过滤洗涤、干燥等。
(6)晶体以NaClO2·3H2O的形式存在,已知:NaClO2·3H2O![]() NaCl+O2↑+3H2O↑。为测定所得固体中NaClO2·3H2O的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为a g,灼烧恒重后,得到固体b g。则晶体中NaClO2·3H2O的质量分数是__________。
NaCl+O2↑+3H2O↑。为测定所得固体中NaClO2·3H2O的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为a g,灼烧恒重后,得到固体b g。则晶体中NaClO2·3H2O的质量分数是__________。
若发生副反应4[NaClO2·3H2O]![]() 2NaCl+2NaClO3+O2↑+12H2O↑,则实验测得的值会__________。(选填“偏大”、“偏小”或“不变”)
2NaCl+2NaClO3+O2↑+12H2O↑,则实验测得的值会__________。(选填“偏大”、“偏小”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
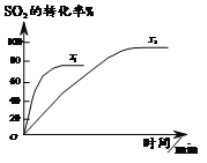
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g),如图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g),如图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
完成下列填空:
(1)T1__________(选填“>”“<”或“=”)T2,判断依据是_______________;该反应为___________(选填“放”或“吸”)热反应,判断依据是__________。
(2)下表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率。
投料比 | ① | ② | ③ | ④ |
SO2平衡转化率/% | 97.1 | 96.8 | 95.8 | 90.0 |
②对应的投料比为_____。投料比为8:10时,平衡混合气体中SO3体积分数为______。
(3)在相同温度下:2NO(g)+O2(g)![]() 2NO2(g) K1=a;NO2(g)+SO2(g)
2NO2(g) K1=a;NO2(g)+SO2(g)![]() SO3(g)+NO(g) K2=b;则2SO2(g)+O2(g)
SO3(g)+NO(g) K2=b;则2SO2(g)+O2(g)![]() 2SO3(g) 的平衡常数K=__________(用a、b表示)。
2SO3(g) 的平衡常数K=__________(用a、b表示)。
(4)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如下:

吸收池中发生反应的离子方程式是________;NaHSO3溶液呈弱酸性,NaHSO3溶液中离子浓度由大到小排序为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“类推思维”是化学解题中常用的思维方法,类推的结论最终要经过实践的检验,才能决定其正确与否。下列类推结论中正确的是
A.钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
B.铝在空气中生成氧化膜保护内层金属;铁在空气中生成氧化膜也保护内层金属
C.Al(OH)3、Cu(OH)2受热易分解;Fe(OH)3受热也易分解
D.Fe与CuSO4溶液反应能置换Cu;Na与CuSO4溶液反应也能置换Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 银锌纽扣电池的放电反应:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其中Ag2O作正极,发生还原反应
B. 通过构成原电池,能将反应的化学能全部转化为电能
C. 如图原电池中,电池工作时,SO42-移向电池的正极
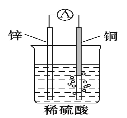
D. 构成原电池的两个电极必须是活泼性不同的两种金属
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。它的制备方法如 下图所示,下列说法正确的是
![]()
A.步骤①的化学方程式为:SiO2+C![]() Si+CO2↑
Si+CO2↑
B.步骤①、②、③中每生成或反应1molSi,转移2mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.单晶硅是电子工业中重要的半导体材料,也能用于制作太阳能电池
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4与Cl2生成CH3Cl的反应过程,中间态物质的能量关系见下图。有关说法错误的是
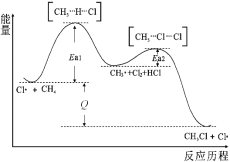
A.Cl·是由Cl2在光照下化学键断裂生成的,该过程可表示为:![]()
B.反应过程一定无CH3CH3的生成
C.图中的反应热Q>0,其大小与Ea1、Ea2无关
D.CH4转化为CH3Cl的过程,C-H键发生了断裂
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列各溶液中,所给离子一定能大量共存的是
A.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
B.小苏打溶液:K+、SO42-、Cl-、H+
C.与铝反应产生H2的溶液中:Na+、K+、CO32-、Cl-
D.室温下,强酸性溶液中:Na+、Fe3+、NO3-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】锌锰碱性干电池是依据原电池原理制成的化学电源。电池中负极与电解质溶液接触直接反应会降低电池的能量转化效率,称为自放电现象。


下列关于原电池和干电池的说法不正确的是
A. 两者正极材料不同
B. MnO2的放电产物可能是KMnO4
C. 两者负极反应式均为Zn失电子
D. 原电池中Zn与稀H2SO4存在自放电现象
查看答案和解析>>
科目: 来源: 题型:
【题目】每年10月23日上午6:02到晚上6:02倍誉为“摩尔日”(Mole Day),这个时间的美式写法为6:02 10/23,外观与阿伏伽德罗常数6.02×1023相似。设NA为阿伏伽德罗常数的值,下列说法正确的是
A.7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1NA
B.1L0.1mol·L-1碳酸钠溶液中含有的氧原子数为0.3NA
C.将100mL 0.1mol·L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数为0.01NA
D.将CO2通过0.1mol Na2O2时,反应共转电子数为移0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】在四个不同的密闭容器中,采用不同条件进行反应N2(g)+3H2(g)![]() 2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
A.v(N2)=0.2mol/(Ls)B.v(NH3)=0.8mol/(Lmin)
C.v(H2)=0.3mol/(Ls)D.v(H2)=1.3mol/(Lmin)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com