
����Ŀ����֪2SO2(g)+O2(g)![]() 2SO3(g)����ͼΪ��ͬ�¶ȣ�T1��T2����SO2��ת������ʱ��ı仯���ߡ�
2SO3(g)����ͼΪ��ͬ�¶ȣ�T1��T2����SO2��ת������ʱ��ı仯���ߡ�
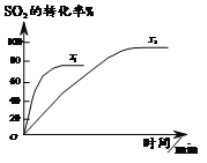
���������գ�
(1)T1__________��ѡ�>����<����=����T2���ж�������_______________���÷�ӦΪ___________��ѡ��š����������ȷ�Ӧ���ж�������__________��
(2)�±�Ϊһ���¶Ⱥ�ѹǿ�£�4��Ͷ�ϱ�[n(SO2):n(O2)]�ֱ�Ϊ2:18��4:15��7:11��8:10ʱSO2��ƽ��ת���ʡ�
Ͷ�ϱ� | �� | �� | �� | �� |
SO2ƽ��ת���ʣ�% | 97.1 | 96.8 | 95.8 | 90.0 |
�ڶ�Ӧ��Ͷ�ϱ�Ϊ_____��Ͷ�ϱ�Ϊ8:10ʱ��ƽ����������SO3�������Ϊ______��
(3)����ͬ�¶��£�2NO(g)+O2(g)![]() 2NO2(g) K1=a��NO2(g)+SO2(g)
2NO2(g) K1=a��NO2(g)+SO2(g)![]() SO3(g)+NO(g) K2=b����2SO2(g)+O2(g)
SO3(g)+NO(g) K2=b����2SO2(g)+O2(g)![]() 2SO3(g) ��ƽ�ⳣ��K=__________����a��b��ʾ����
2SO3(g) ��ƽ�ⳣ��K=__________����a��b��ʾ����
(4)�Ƽ�ѭ�����������᳧β���е�SO2������ת��Ϊ����Ĺ������£�

���ճ��з�����Ӧ�����ӷ���ʽ��________��NaHSO3��Һ�������ԣ�NaHSO3��Һ������Ũ���ɴ�С����Ϊ_________��
���𰸡�> �����������䣬��ͼ��֪T1��T2�ﵽƽ������ʱ��̣�˵��T1��Ӧ�ٶȿ죬����T1�¶ȸ� �� ��ͼ��֪��T1�¶ȸߣ���������ƽ��ת���ʵͣ�˵���¶�����ʱƽ�����ƣ��淴ӦΪ���ȣ�����ӦΪ���� 4:15 50% ab2 SO2+SO32-+H2O��2HSO3- c(Na+)��c(HSO3-)��c(H+)��c(SO32-)��c(OH-)
��������
��1���¶�Խ�ߣ���Ӧ����Խ�죬�ﵽ��ѧƽ���ʱ��Խ�̣��¶����ߣ�ƽ�������ȷ����ƶ���
��2��ͬһ��ѧ��Ӧ������һ�ַ�Ӧ��Ũ�ȿ������������Ӧ��ת���ʣ���������ʽ����ɵã�
��3�����ø�˹���ɵõ���Ӧ֮��Ĺ�ϵ���ɴ˼���ƽ�ⳣ����
��4�����ճ�������������Һ���������Ӧ�������������ƣ�NaHSO3��Һ�������ԣ�˵��HSO3-�ĵ������ˮ�⡣
��1���¶�Խ�ߣ���Ӧ����Խ�죬�ﵽ��ѧƽ���ʱ��Խ�̣���ͼ��֪����ͬ�����£�T1��T2�ﵽƽ������ʱ��̣�˵��T1��Ӧ�ٶȿ죬��T1��T2���¶����ߣ�ƽ�������ȷ����ƶ�����T2��T1�� SO2��ת���ʼ�С��ƽ���������ƶ�����������Ϊ���ȷ�Ӧ���ʴ�Ϊ�����������������䣬��ͼ��֪T1��T2�ﵽƽ������ʱ��̣�˵��T1��Ӧ�ٶȿ죬����T1�¶ȸߣ��ţ���ͼ��֪��T1�¶ȸߣ���������ƽ��ת���ʵͣ�˵���¶�����ʱƽ�����ƣ��淴ӦΪ���ȣ�����ӦΪ���ȣ�
��2��ͬһ��ѧ��Ӧ������һ�ַ�Ӧ��Ũ�ȿ������������Ӧ��ת���ʣ�Ͷ�ϱ�[n��SO2����n��O2��]ԽС��������Ũ��Խ��������ת����Խ�����ݢڵ�ת���ʿ�֪��Ͷ�ϱ�[n��SO2����n��O2��]Ϊ4��15��Ͷ�ϱ�[n��SO2����n��O2��]Ϊ8��10ʱ�����������ת����Ϊ90%������ʼ��������Ϊ4mol���������ʵ���Ϊ5mol�������⽨����������ʽ��

��ƽ��������������������������Ϊ![]() ��100%=50%���ʴ�Ϊ��4��15��50%��
��100%=50%���ʴ�Ϊ��4��15��50%��
��3������֪��Ӧ���α��Ϊ�٢ڣ��ɸ�˹���ɿ�֪��+����2�ɵ�2SO2(g)+O2(g)![]() 2SO3(g)����ƽ�ⳣ��K=K1��K22= ab2���ʴ�Ϊ��ab2��
2SO3(g)����ƽ�ⳣ��K=K1��K22= ab2���ʴ�Ϊ��ab2��
��4�����ճ�������������Һ���������Ӧ�������������ƣ���Ӧ�����ӷ���ʽ��SO2+SO32-+H2O=2HSO3-��NaHSO3��Һ�������ԣ�˵��HSO3-�ĵ������ˮ�⣬��NaHSO3��Һ������Ũ���ɴ�С����Ϊc(Na+)��c(HSO3-)��c(H+)��c(SO32-)��c(OH-)���ʴ�Ϊ��SO2+SO32-+H2O=2HSO3-��c(Na+)��c(HSO3-)��c(H+)��c(SO32-)��c(OH-)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ�����
(һ)���������������ʣ����� ������ ��CO2 ��H2SO4 ��Ba��OH��2 ���ɫ�������������� ��HCl ���ˮ����� ��̼��� ��CuSO4��5H2O��
(1)�������������ڵ���ʵ���__________������ţ���
(2)�����Һ���μӢߵ���Һ��������������________________________��
(3)����������������������ˮ��Һ�з�����Ӧ�������ӷ���ʽΪ��H++OH����H2O����÷�Ӧ�Ļ�ѧ����ʽΪ______________________________��
(��)(1)ij��̬�����ﻯѧʽΪRO2���ڱ�״���£�1.28 g��������������448 mL�����������Ħ������Ϊ_______��R�����ԭ������Ϊ__________��
(2)�ڱ�״���£�w L��������x��N2���ӣ����ӵ�����Ϊ____________����w��x��ʾ����
(3)���˺��ʳ��ˮ�Ժ��п����Ե�CaCl2��MgCl2��Na2SO4�����ʣ�ͨ�����¼���ʵ�鲽�裬���Ƶô�����ʳ��ˮ���ټ����Թ�����BaCl2��Һ���ڼ����Թ�����NaOH��Һ���ۼ����Թ�����Na2CO3��Һ���ܵ���ϡ�����������ݲ������ݹ��ˡ���ȷ�IJ���˳����________����д��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС������NaI��Һ��ͨ������Cl2�õ������Һ�������ú����Һ��ȡNaI���壬ʵ���������£�

��֪��Ӧ����2I��+2Cu2++![]() +H2O
+H2O![]() 2CuI��+
2CuI��+![]() +2H+��
+2H+��
�ش��������⣺
��1������ʵ������Ҫ�IJ�����������ͨ©�����ձ���_____________��
��2����Ӧ����CuI����������ԭ����ֻ��NO2���÷�Ӧ�Ļ�ѧ����ʽΪ_________________������95.5 g CuI���뷴Ӧ������Ҫ�����______________L��O2���ܽ����ɵ�NO2��ˮ����ȫת��Ϊ���ᡣ
��3��������B�к�����Ԫ�أ���ԭ������һ��Ԫ��ԭ�ӵ����ʵ���֮��Ϊ3��8������B�Ļ�ѧʽΪ_____________��
��4����Ӧ�������ɺ�ɫ�������ɫ���壬��ɫ������׳�Ϊ��������������Ӧ���Ļ�ѧ����ʽΪ______��
��5����������Cl2ͨ�뺬12 g NaI����Һ�У�һ��ʱ������Һ���ɵõ����������Ϊ_________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ĸ������ʾһ�ַ�Ӧ���������(ijЩ�����Ѿ���ȥ)�����г�����A��C��DΪ��ɫ���壬C��ʹʪ��ĺ�ɫʯ����ֽ������
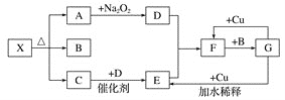
��1��д������X�Ļ�ѧʽ��__��
��2��д�����б仯�Ļ�ѧ����ʽ��
��A��D��___��
��G��E��___��
��F��G��___��
��3��ʵ��������ü��ȹ�������ķ�����ȡ����C����д����ѧ����ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и���Һ�У���������һ���ܴ����������
A.ʹ��̪��Һ������Һ��Na����Cl����SO42����Fe3��
B.С�մ���Һ��K����SO42����Cl����H��
C.������Ӧ����H2����Һ�У�Na����K����CO32����Cl��
D.�����£�ǿ������Һ�У�Na����Fe3����NO3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A. Cl2ͨ��ˮ�У�Cl2+H2O = 2H++Cl-+ClO-
B. ˫��ˮ����ϡ�����KI��Һ��H2O2��2H����2I��=I2��2H2O
C. ��ͭ���缫���CuSO4��Һ��2Cu2����2H2O![]() 2Cu��O2����4H��
2Cu��O2����4H��
D. Na2S2O3��Һ�м���ϡ���2S2O32����4H��=SO42����3S����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ����£�Fe��ˮ�����ɷ�����Ӧ��Ӧ������װ�ã��Ϳ�����ɴ˷�Ӧ��ʵ�顣

��1������A������Ϊ____________����ײ����˼�Ƭ���Ƭ����������____________��
��2��ʵ��ǰ���������װ�ý��еIJ�����_________________��ʵ�鿪ʼʱӦ�ȵ�ȼ_____����ƾ��ơ��ƾ���ơ�����
��3������Ӧ���ɵĹ�����д��ԣ�д������ˮ������Ӧ�Ļ�ѧ����ʽ__________________��
��4����д����D���ռ�β���ķ�����___________________________�����Ҫ��D����ȼβ���������Ը��������____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ǹɵ�ص����������Ѵ����ij�����Ŷ�������������̶Լ���п�̸ɵ�صķϾ���Դ���л������ã�
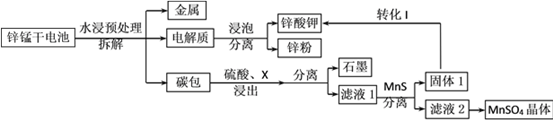
��֪����Ksp(MnS)=2.5��10��13��Ksp(ZnS)=1.6��10��24
��Mn(OH)2��ʼ����ʱpHΪ8.3,��ȫ������pHΪ9.8
�ż���п�̸ɵ������п��Ϊ��������������Ϊ����������������ҺΪ����ʡ�����ܷ�ӦΪ2MnO2+ Zn+2KOH= 2MnOOH+K2ZnO2����д����ص�������Ӧʽ_____________��
��Ϊ�����̼���Ľ���Ч�ʣ����Բ�ȡ�Ĵ�ʩ��________________________��(дһ������)
������Һ1�м���MnS��Ŀ����__________________________________________��
����֪MnSO4���ܽ��������ͼ��ʾ������Һ2������MnSO4��H2O����IJ����������ᾧ��____________________��ϴ�ӡ����¸��
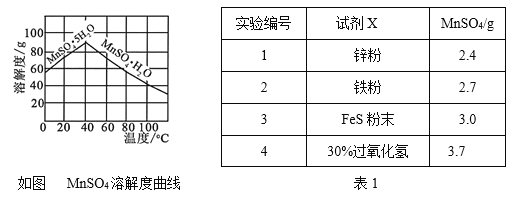
��Ϊ��ѡ���Լ�X������ͬ�����£��ֱ���3 g̼�������Ʊ�MnSO4��ʵ�飬�õ��������1����д������Լ�X��̼���е���Ҫ�ɷַ�����Ӧ�Ļ�ѧ����ʽ_____________��
�ʹ�ҵ�Ͼ�����������Һ2�м���NaHCO3��Һ���Ʊ�MnCO3����ѡ��Na2CO3��Һ��ԭ����___________________________________��
�˸ÿ���С������EDTA(�Ҷ�����������ƣ������Ӽ�дΪY2��)������ϵζ��ⶨMn2+�ڵ���еİٷֺ�������ѧ����ʽ���Ա�ʾΪMn2++Y2��=MnY��ʵ��������£�
ȷ����һ�ڵ�ص�����ƽ��Ϊ24.00g����ȫ��Ӧ�õ�200.00mL��Һ2����ȡ10.00mL��Һ2ϡ����100.00mL��ȡ20.00mL��Һ��0.0500molL��1EDTA����Һ�ζ���ƽ�����ı���Һ22.00mL����÷������MnԪ�صİٷֺ���Ϊ________��(����3λ��Ч����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��K����ͼ��ת����ϵ������D��EΪ���嵥�ʣ�A��HΪ�����������Իش�(ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ�����)��
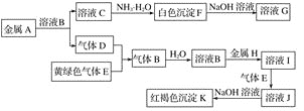
(1)д���������ʵĻ�ѧʽ��D��________�� I��______��
(2)д����C��F����Ӧ�����ӷ���ʽ��______________________________________��
(3)д����Ӧ��J��K�������ӷ���ʽ��____________________________________��
(4)����ҺI�е���NaOH��Һ���ɹ۲쵽��������______________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com