
【题目】在高温下,Fe与水蒸气可发生反应。应用下列装置,就可以完成此反应的实验。

(1)仪器A的名称为____________;其底部放了几片碎瓷片,其作用是____________。
(2)实验前必须对整套装置进行的操作是_________________;实验开始时应先点燃_____(填“酒精灯”或“酒精喷灯”)。
(3)若反应生成的固体具有磁性,写出铁与水蒸气反应的化学方程式__________________。
(4)请写出在D处收集尾气的方法:___________________________;如果要在D处点燃尾气,则必须对该气体进行____________________________________。
【答案】圆底烧瓶 防止暴沸 气密性的检验 酒精灯 3Fe+4H2O(g)![]() Fe3O4+4H2 向下排空气法 验纯
Fe3O4+4H2 向下排空气法 验纯
【解析】
⑴仪器A的名称为圆底烧瓶,加碎瓷片的作用是防止液体暴沸;
⑵有气体参与反应的装置都要检查装置的气密性,开始时防止铁粉被氧气氧化,不能先点燃酒精喷灯;
⑶铁粉和水蒸气在高温条件下生成四氧化三铁和氢气;
⑷尾气的主要成分是氢气,密度比空气的小,可以用向下排空气法收集,氢气属于易燃气体,在点燃时先要检验氢气的纯度。
⑴仪器A的名称为圆底烧瓶,加碎瓷片的作用是防止液体暴沸,故答案为:圆底烧瓶,防止暴沸;
⑵有气体参与反应的装置都要检查装置的气密性,开始时防止铁粉被氧气氧化,不能先点燃酒精喷灯,要先点燃酒精灯产生大量水蒸汽排除空气后,再点燃酒精喷灯,故答案为:气密性的检验,酒精灯;
⑶有磁性的铁的氧化物是四氧化三铁,也就是铁粉和水蒸气在高温条件下生成四氧化三铁,化学反应方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
⑷尾气的主要成分是氢气,密度比空气的小,可以用向下排空气法收集,氢气属于易燃气体,在点燃时先要检验氢气的纯度,故答案为:向下排空气法,验纯。


科目:高中化学 来源: 题型:
【题目】0.1mol某有机物的蒸气跟过量O2混合后点燃,生成13.2g CO2和5.4g H2O,该有机物跟金属反应放出H2,又能跟新制Cu(OH)2悬浊液加热时生成红色沉淀,此有机物还能跟乙酸反应生成酯类化合物.该酯类化合物的结构简式可能是( )
A. CH3CH(OCH3) CHOB. OHCCH2CH2COOCH3
C. CH3CH(OOCCH3)CHOD. OHCCH(OH) COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以粉煤灰(主要成分:Al2O3、SiO2、少量Fe2O3)为原料,制取Al2O3的部分工艺流程如下:

完成下列填空:
(1)铝原子核外有_____种不同能量的电子,最外层电子的轨道式是_____________,上述流程涉及第二周期元素的原子半径由小到大的顺序是______________________________。
(2) “除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为______________________,检验溶液中Fe3+是否除尽的方法是____________________________________________。
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。______________________
(4)上述流程可循环的物质是_______________。
(5)工业上将Al2O3溶解在熔化的冰晶石中电解获得铝,该反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
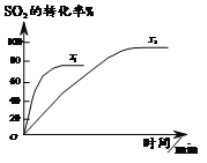
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g),如图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g),如图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
完成下列填空:
(1)T1__________(选填“>”“<”或“=”)T2,判断依据是_______________;该反应为___________(选填“放”或“吸”)热反应,判断依据是__________。
(2)下表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率。
投料比 | ① | ② | ③ | ④ |
SO2平衡转化率/% | 97.1 | 96.8 | 95.8 | 90.0 |
②对应的投料比为_____。投料比为8:10时,平衡混合气体中SO3体积分数为______。
(3)在相同温度下:2NO(g)+O2(g)![]() 2NO2(g) K1=a;NO2(g)+SO2(g)
2NO2(g) K1=a;NO2(g)+SO2(g)![]() SO3(g)+NO(g) K2=b;则2SO2(g)+O2(g)
SO3(g)+NO(g) K2=b;则2SO2(g)+O2(g)![]() 2SO3(g) 的平衡常数K=__________(用a、b表示)。
2SO3(g) 的平衡常数K=__________(用a、b表示)。
(4)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如下:

吸收池中发生反应的离子方程式是________;NaHSO3溶液呈弱酸性,NaHSO3溶液中离子浓度由大到小排序为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的四种元素X、Y、Z、W分别处于第一至第四周期,自然界中存在多种X的化合物,Y原子核外电子有6种不同的运动状态,Y与Z可形成正四面体形分子,W的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为_________。
(2)Z所在主族的四种元素分别与X形成的化合物,沸点由高到低的顺序是______(填化学式),呈现如此递变规律的原因是________________________________。
(3)Y元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为___,另一种的晶胞如图二所示,该晶胞的空间利用率为________________(保留两位有效数字)。(![]() )
)
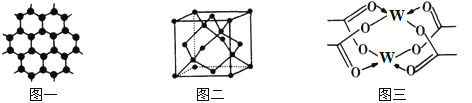
(4)W元素形成的单质,其晶体的堆积模型为___________,W的醋酸盐晶体局部结构如图三,该晶体中含有的化学键是____________(填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)向W的硫酸盐溶液中滴加过量氨水,观察到的现象是____________。请写出上述过程的离子方程式___________________________ ,___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A.7.8g Na2O2中含有的离子总数为 0.4NA
B.标准状况下,22.4L 乙醇所含的分子数为0.1NA
C.常温常压下,0.18g H2O所含的电子数为0.1NA
D.常温常压下,3.2g O2所含的氧原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A.相同温度、相同压强的O2和CO2,两种气体的分子数一定相等
B.相同体积、相同密度的N2和CO,两种气体的分子数一定相等
C.配制450mL 0.1mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8g
D.0.45 mol·L-1的NaCl溶液与0.15mol·L-1的AlCl3溶液中含有的Cl-离子数目相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯的化合物与人们的生活紧密相关。回答下列问题:
(1)高血压患者,应该减少食盐的摄入量,为了“减盐不减咸”,建议高血压患者食用低钠盐(含氯化钾30%左右的氯化钠)。我们可以通过________________(操作名称)来检验食盐中含有钾元素,得到食盐中含钾元素的实验依据是___________。
(2)瑞典化学家舍勒(Carl Wilhelm Scheele)将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首次制得了氯气。实验室用下图所示装置制取纯净的氯气。
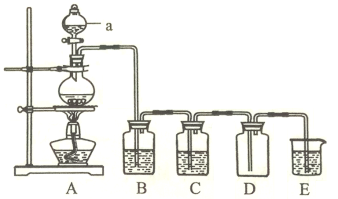
①仪器a的名称为______________。
②装置A中发生反应的离子方程式为_____________________________。
③装置B的作用是_____________,装置C中的试剂为_____________。
④装置E中发生反应的离子方程式为__________________。
⑤当有4molHCl被氧化时,产生的氯气在标准状况下的体积为__________L。
(3)漂白液(有效成分是NaClO)与洁厕灵(主要成分为盐酸)混合,也会产生Cl2,请写出该反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:
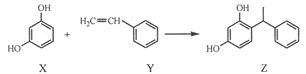
下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com