
科目: 来源: 题型:
【题目】Ⅰ.已知:①![]()
②![]()
③![]()
试据此写出一氧化碳燃烧的热化学方程式___________________________。
Ⅱ.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
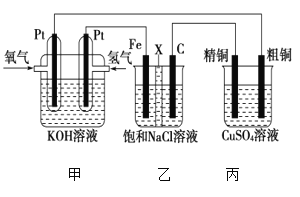
①石墨电极为________(填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,________(填“铁极”或“石墨极”)区的溶液先变红。乙池中电解总方程式为____________。
②如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将________(填“增大”“减小”或“不变”)。精铜电极上的电极反应式为______________________。
③若在标准状况下,有224 mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为________mL;丙装置中阴极析出铜的质量为________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】结构简式如图所示的有机物常用于合成药物,下列对该有机物说法不正确的是
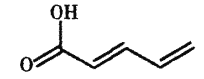
A.存在顺反异构体
B.与丙烯酸互为同系物
C.有两种官能团
D.与H2按等物质的量关系反应时,可能有3种加成产物
查看答案和解析>>
科目: 来源: 题型:
【题目】对于100mL0.5 mol·L-1Na2CO3溶液,下列有关说法正确的是( )
A.实验室配制该溶液,定容时仰视刻线,所配制溶液浓度偏大
B.该溶液稀释10倍后,c(Na+)=0.05 mol·L-1
C.从该溶液中取出10mL,所取溶液中溶质的物质的量浓度为0.05 mol·L-1
D.该溶液中含有Na2CO3的质量为5.3g
查看答案和解析>>
科目: 来源: 题型:
【题目】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
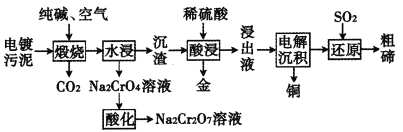
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2![]() 2CuO+TeO2。
2CuO+TeO2。
(1)Te元素在元素周期表中的位置为______________其基态原子的电子占据的最高能层符号为________。
(2)煅烧时,Cr2O3发生反应的化学方程式为__________________。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有________(填化学式)。电解沉积过程中析出单质铜的电极为_________极。
(4)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:
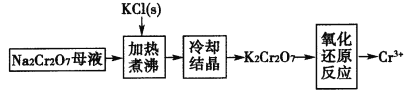
通过冷却结晶能析出大量K2Cr2O7的原因是______________。
(5)测定产品中K2Cr2O7含量的方法如下:称取试样2.50 g配成250 mL溶液,取25.00 mL于锥形瓶中,加入足量稀硫酸和几滴指示剂,用0.1000 mol·L-1(NH4)2Fe(SO4)2标准液进行滴定。滴定过程中发生反应的离子方程式为____________________。
若三次实验消耗(NH4)2Fe(SO4)2标准液的体积平均为25.00 mL,则所得产品中K2Cr2O7的纯度为________%(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】浓硫酸和铜在加热时反应,生成SO2气体的体积为3.36L(标准状况下)。已知:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。试计算:(写出计算过程)
CuSO4+SO2↑+2H2O。试计算:(写出计算过程)
(1)SO2气体的物质的量是多少?___
(2)参加反应的硫酸的物质的量是多少?___
(3)将生成的硫酸铜配制成500mL溶液,则该溶液中溶质的物质的量浓度是多少?___
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用18.4molL-1的浓硫酸来配制480mL0.2molL-1的稀硫酸。可供选用的仪器有:①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有___(选填序号),还缺少的仪器有(写仪器名称)___。
(2)需要用量筒量取上述浓硫酸的体积为___mL,量取浓硫酸时应选用___(选填①10mL②50mL③100mL)规格的量筒。
(3)实验中两次用到玻璃棒,其作用分别是:___、___。
(4)下列对容量瓶及其使用方法的描述中正确的是___。
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.配制溶液时,把量好的浓硫酸小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
D.使用前要检查容量瓶是否漏水
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有___(填序号)
①未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,仰视刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的量是高中化学计算的核心:
(1)相同物质的量的NH3和H2S的质量比___,分子个数比为___,同温同压下的体积比__,所含氢原子的个数比为____.
(2)现有m g某气体,它的一个分子由四原子构成,它的摩尔质量为M g/mol.设阿伏伽德罗常数为NA,则:
①该气体的物质的量为____mol.
②该气体中所含的原子总数为____个.
③该气体在标准状况下的体积为___L.
查看答案和解析>>
科目: 来源: 题型:
【题目】关于Na2CO3与NaHCO3的性质判断正确的是( )
A.常温下溶解度:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
D.与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目: 来源: 题型:
【题目】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是 ( )。

A. a为CH4,b为CO2
B. ![]() 向负极移动
向负极移动
C. 此电池在常温时也能工作
D. 正极电极反应式为O2+2CO2+4e-===2![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com