
【题目】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
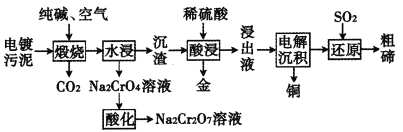
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2![]() 2CuO+TeO2。
2CuO+TeO2。
(1)Te元素在元素周期表中的位置为______________其基态原子的电子占据的最高能层符号为________。
(2)煅烧时,Cr2O3发生反应的化学方程式为__________________。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有________(填化学式)。电解沉积过程中析出单质铜的电极为_________极。
(4)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:
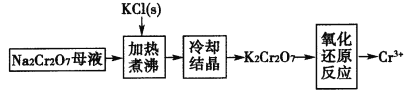
通过冷却结晶能析出大量K2Cr2O7的原因是______________。
(5)测定产品中K2Cr2O7含量的方法如下:称取试样2.50 g配成250 mL溶液,取25.00 mL于锥形瓶中,加入足量稀硫酸和几滴指示剂,用0.1000 mol·L-1(NH4)2Fe(SO4)2标准液进行滴定。滴定过程中发生反应的离子方程式为____________________。
若三次实验消耗(NH4)2Fe(SO4)2标准液的体积平均为25.00 mL,则所得产品中K2Cr2O7的纯度为________%(保留三位有效数字)。
【答案】第五周期ⅥA族 O 2Cr2O3+3O2+4Na2CO3![]() 4Na2CrO4+4CO2 CuSO4 阴 低温条件下,K2Cr2O7的溶解度在整个体系中最小,且K2Cr2O7的溶解度随温度的降低而显著减小 Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O 49.0
4Na2CrO4+4CO2 CuSO4 阴 低温条件下,K2Cr2O7的溶解度在整个体系中最小,且K2Cr2O7的溶解度随温度的降低而显著减小 Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O 49.0
【解析】
某种电镀污泥中主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜、粗碲等,根据流程图,煅烧时Cu2Te发生的反应为Cu2Te+2O2![]() 2CuO+TeO2,Cr2O3与纯碱和空气中的氧气反应生成Na2CrO4,Na2CrO4酸化后生成Na2Cr2O7溶液;沉渣中主要含有CuO、TeO2以及少量的金(Au),用稀硫酸溶解后,浸出液中主要含有铜离子和TeOSO4,电解后铜离子放电生成铜,溶液中含有TeOSO4,TeOSO4与二氧化硫发生氧化还原反应生成粗碲,据此分析解答。
2CuO+TeO2,Cr2O3与纯碱和空气中的氧气反应生成Na2CrO4,Na2CrO4酸化后生成Na2Cr2O7溶液;沉渣中主要含有CuO、TeO2以及少量的金(Au),用稀硫酸溶解后,浸出液中主要含有铜离子和TeOSO4,电解后铜离子放电生成铜,溶液中含有TeOSO4,TeOSO4与二氧化硫发生氧化还原反应生成粗碲,据此分析解答。
(1)Te是52号元素,原子核外电子排布为2、8、18、18、6,可见Te元素在元素周期表中的位置为第五周期第VIA族,最高能层为第5能层,故其基态原子的电子占据的最高能层符号为O;
(2)煅烧时,Cr2O3与O2及Na2CO3发生反应产生Na2CrO4和CO2,反应的化学方程式为:2Cr2O3+3O2+4Na2CO3![]() 4Na2CrO4+4CO2;
4Na2CrO4+4CO2;
(3)根据上述分析,浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有CuSO4,Cu2+转化为铜单质,发生还原反应,电解沉积过程中析出单质铜的电极为阴极;
(4)在低温条件下K2Cr2O7的溶解度在整个体系中最小,且K2Cr2O7的溶解度随温度的降低而显著减小,因此通过冷却结晶能析出大量K2Cr2O7;
(5)氧化还原滴定过程中发生Fe2+与Cr2O72-的反应,其中Cr2O72-被还原为Cr3+,Fe2+被氧化为Fe3+,根据电子守恒、电荷守恒及原子守恒,可得该反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
反应中消耗Fe2+的物质的量n(Fe2+)=c·V=0.1000 mol·L-1×0.025 L=0.0025 mol,根据方程式Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O可知n(Cr2O72-)=![]() n(Fe2+)=
n(Fe2+)=![]() mol,则所得样品中K2Cr2O7的纯度=
mol,则所得样品中K2Cr2O7的纯度=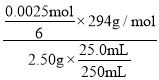 ×100%=49.0%。
×100%=49.0%。


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】已知反应①CO(g)+CuO(s)![]() CO2(g)+Cu(s)和反应②H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②H2(g)+CuO(s)![]() Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A. 反应①的平衡常数K1=c(CO2).c(Cu)/c(CO).c(CuO)
B. 反应③的平衡常数K=K1/K2
C. 对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值
D. 对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500 ℃条件下,在恒容密闭容器中,充入1 mol NO2存在如下平衡:2NO2(g) ![]() N2O4(g)。平衡后,向容器内再充入1 mol NO2,下列说法正确的是
N2O4(g)。平衡后,向容器内再充入1 mol NO2,下列说法正确的是
A. 平衡向正反应方向移动 B. 平衡常数K增大
C. NO2的转化率变小 D. 容器内气体颜色先变深后变浅,最后比原来还要浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里也可以利用以下反应制取少量氯气:2KMnO4+16HCl(浓)![]() 2KCl+2MnCl2+8H2O+5Cl2↑,关于该反应的说法正确的是( )
2KCl+2MnCl2+8H2O+5Cl2↑,关于该反应的说法正确的是( )
A.KMnO4中的锰元素被氧化
B.Cl2既是氧化产物,又是还原产物
C.HCl在反应中只做还原剂
D.每生成1molCl2转移电子的物质的量为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是 ( )。

A. a为CH4,b为CO2
B. ![]() 向负极移动
向负极移动
C. 此电池在常温时也能工作
D. 正极电极反应式为O2+2CO2+4e-===2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Z是合成某药物的中间体,其合成原理如下:
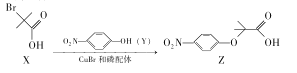
下列说法正确的是.
A.用NaHCO3溶液可以鉴别X和ZB.X、Y、Z都能发生取代反应
C.X分子所有碳原子可能共平面D.与X具有相同官能团的同分异构体还有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=+b kJ/mol
B. C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
C. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-2b kJ/mol
D. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-4b kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验室制氯气的说法中错误的是( )
A.该反应是一个氧化还原反应,其中二氧化锰是氧化剂
B.每生成1mol氯气,就要转移2mol电子
C.该反应的离子方程式为MnO2+4H++4Cl-![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.该方法是瑞典化学家舍勒最先发现的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示不同化学元素所组成的化合物,以下说法不正确的是

A. 若图中①为某种多聚体的单体,则①最可能是氨基酸
B. 若②存在于皮下和内脏器官周围等部位,则②是脂肪
C. ③一定是核酸或是组成核酸的单体核苷酸
D. 若④是参与构成植物细胞壁的一种多糖,则④最可能是纤维素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com