
科目: 来源: 题型:
【题目】在实验室用自来水制取蒸馏水的实验中,下列说法正确的是( )
A.蒸馏烧瓶中加满自来水并放入几粒沸石
B.冷凝水应该是下进上出,与蒸气的流向相反
C.开始蒸馏时,应该先加热,再通冷凝水
D.蒸馏完毕时,应该先停止通冷凝水再撤酒精灯
查看答案和解析>>
科目: 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是 ( )

A. 按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B. 图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C. 铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D. 图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为硫酸,其正极反应式为____________________,负极反应式为___________________;若在常温下转移2mol电子,可产生水质量为_________g。
(2)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=3mol·L—1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到1.12L(标准状况)气体。此时氢氧燃料电池中消耗H2的质量是_______,混合溶液中NaOH的物质的量浓度是__________mol·L-1。
(3)已知可逆反应:AsO43-+2I-+2H+![]() AsO33-+I2+H2O。如图所示,C1棒和C2棒都是石墨电极。
AsO33-+I2+H2O。如图所示,C1棒和C2棒都是石墨电极。
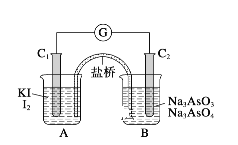
(Ⅰ)若向B中逐滴加入浓盐酸,上述反应向右进行,发现检流计指针向左偏转。
(Ⅱ)若改用向B中滴加40%的NaOH溶液,发现检流计指针与(Ⅰ)中偏转方向相反。
试回答问题:
操作(Ⅰ)中,C1棒上的反应式为_____________________________。
操作(Ⅱ)中,C2棒上的反应式为______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在下图所示装置中加入一定量的铁粉,分液漏斗中加入一定体积浓度为12 mol·L-1的硝酸,加热打开分液漏斗的活塞,使其充分反应后,
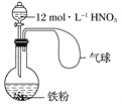
下列微粒:①![]() 、② Fe3+、③H+、④ NO、⑤ NO2,在该装置中一定大量存在的( )
、② Fe3+、③H+、④ NO、⑤ NO2,在该装置中一定大量存在的( )
A.①B.①⑤C.②④⑤D.①②③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】现有25 mL 2 mol·L-1Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家已研制出一种可替代锂电池的“可充室温Na-CO2电池”,该电池结构如图所示。电极材料为钠金属片和碳纳米管,电解液为高氯酸钠-四甘醇二甲醚。下列说法错误的是( )
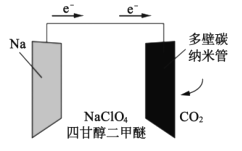
A.电池放电时钠金属片发生氧化反应
B.电池工作时,外电路流过0.01mol电子,负极材料减重0.23g
C.碳纳米管的作用主要是导电及吸附CO2,电池充电时,应该与直流电源的正极相连
D.放电时负极反应为:C+2Na2CO3-4e-=3CO2↑+4Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】某二元弱酸(简写为H2B)溶液,按下式发生一级和二级电离:
H2B![]() H++HB-
H++HB-
HB-![]() H++B2-
H++B2-
已知相同浓度时的电离度a(H2B)>>a(HB-),现有下列四种溶液:
①0.01molL-1的H2B溶液
②0.01molL-1的NaHB溶液
③0.02molL-1的HCl溶液与0.04molL-1的NaHB溶液等体积混合后的溶液
④0.02molLL-1的NaOH溶液与0.02molL-1的NaHB溶液等体积混合后的溶液
下列说法错误的是( )
A.溶液④一定显碱性B.c(H2B)最大的是③
C.c(B2-)最小的是①D.c(H+)最大的是③
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)天然气是一种清洁高效的能源,其主要成分为甲烷。
CH4的摩尔质量为_____________, 4.8 g CH4的物质的量为______________,在标准状况下的体积约为_______________,所含氢原子数为_______________。
(2)某化学兴趣小组对某矿泉水进行检测, 发现0.5 L该矿泉水中含有10.8 mg Mg2+,则Mg2+的物质的量浓度为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据原电池原理可以设计原电池,实现多种用途
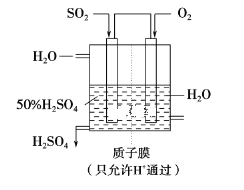
(1) 可以用如图所示装置吸收SO2并制取硫酸,写出通入SO2和O2的电极的电极反应式及反应的总方程式。
负极________________________________
正极________________________________
总反应_________________________________________。
(2) 如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。
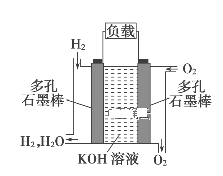
试回答下列问题:
①图中通过负载的电子流动方向________(填“向左”或“向右”)。
②写出氢氧燃料电池工作时电极反应方程式。
正极:_________________________,负极:____________________________,
③若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,
正极反应式为__________________________________________________;
负极反应式为__________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH溶液为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.右图是一个电化学过程的示意图.已知甲池的总反应式为: 2CH3OH+3O2+4KOH![]()
![]() 2K2CO3+6H2O
2K2CO3+6H2O
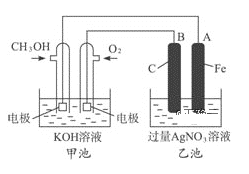
请填空:
(1)充电时:①燃料电池的正极与电源______极相连.
②阳极的电极反应式为__________________________________.
(2)放电时:负极的电极反应式为______________________________.
(3)在此过程中若完全反应,乙池中A极的质量增加324g,则甲池中理论上消耗O2______L(标准状况下).
(4)工业上用3克氢气与足量二氧化碳反应生成气态甲醇(CH3OH)和水蒸气,放出24.5千焦的热量,请写出该反应的热化学反应方程式:_________________________.
(5)用该电池为电源电解氯化镁制取金属镁,消耗甲醇1.6g,可制得金属镁______g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com