
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–±μ ω÷–’ΐ»ΖΒΡ «(ΓΓΓΓ)
A.“―÷Σ2H2(g)+O2(g)![]() 2H2O(g) ΠΛH=Θ≠483.6 kJ/molΘ§‘ρ1mol«βΤχ»Φ…’Ζ≈≥ω»»ΝΩΈΣ483.6 kJ
2H2O(g) ΠΛH=Θ≠483.6 kJ/molΘ§‘ρ1mol«βΤχ»Φ…’Ζ≈≥ω»»ΝΩΈΣ483.6 kJ
B.”…C( ·ΡΪΘ§s)![]() C(ΫπΗ’ ·Θ§s)ΓΓΠΛH=+11.9 kJΓΛmol-1Ω…÷ΣΘ§ ·ΡΪ±»ΫπΗ’ ·Έ»Ε®
C(ΫπΗ’ ·Θ§s)ΓΓΠΛH=+11.9 kJΓΛmol-1Ω…÷ΣΘ§ ·ΡΪ±»ΫπΗ’ ·Έ»Ε®
C.Ά§Έ¬Ά§―Ιœ¬Θ§H2(g)+Cl2(g)![]() 2HCl(g)‘ΎΙβ’’ΚΆΒψ»ΦΧθΦΰΒΡΠΛH≤ΜΆ§
2HCl(g)‘ΎΙβ’’ΚΆΒψ»ΦΧθΦΰΒΡΠΛH≤ΜΆ§
D.Μ·―ß±δΜ·≤Μ“ΜΕ®ΕΦΑιΥφΉ≈ΡήΝΩΒΡ±δΜ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥÷÷Α±≈πΆι(NH3ΓΛBH3)Βγ≥ΊΉΑ÷Ο»γΆΦΥυ Ψ(Έ¥Φ”»κΑ±≈πΆι÷°«ΑΘ§ΝΫΦΪ “ΡΎ“ΚΧε÷ ΝΩœύΒ»)Θ§Βγ≥ΊΖ¥”ΠΈΣNH3ΓΛBH3+3H2O=NH4BO2+4H2O(≤ΜΩΦ¬«ΤδΥϊΖ¥”ΠΒΡ”Αœλ)ΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
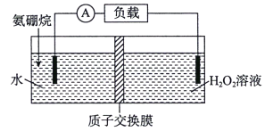
A.Α±≈πΆι÷–NΚΆBΒΡ‘”Μ·ΖΫ Ϋ≤ΜΆ§
B.Βγ≥Ί’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣH2O2+2H++2e-=2H2O
C.ΤδΥϊΧθΦΰ≤Μ±δΘ§œρH2O2»ή“Κ÷–Φ”»κ ΝΩΝρΥαΡή‘ω¥σΒγΝς«ΩΕ»
D.»τΦ”»κΒΡΑ±≈πΆι»Ϊ≤ΩΖ≈ΒγΚσΉσ”“ΝΫΦΪ “ΡΎ“ΚΧε÷ ΝΩ≤νΈΣ3.8gΘ§‘ρΒγ¬Ζ÷–ΉΣ“Τ1.2molΒγΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.Ζ÷±π‘ΎΦΉ““ΝΫ÷ß≤ύΙή÷–ΉΑ»κ1.06gNa2CO3ΚΆ0.84gNaHCO3Θ§ ‘Ιή÷–Ης”–10mLœύΆ§≈®Ε»ΒΡ―ΈΥα(»γΆΦ)Ά§ ±ΫΪΝΫΗω≤ύΙή÷–ΒΡΈο÷ »Ϊ≤ΩΒΙ»κΗςΉ‘ΒΡ ‘Ιή÷–Θ§““ΉΑ÷ΟΒΡΤχ«ρ≈ρ’ΆΥΌ¬ ¥σ
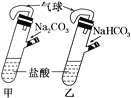
B.”Ο»γΆΦΉΑ÷ΟΩ…“‘÷Τ±Η≥ΝΒμFe(OH)2
C.»Γ…ΌΝΩFe(NO3)2 ‘―υΦ”Υ°»ήΫβΘ§Φ”œΓH2SO4ΥαΜ·Θ§ΒΈΦ”KSCN»ή“ΚΘ§»ή“Κ±δΈΣΚλ…ΪΓΘΫα¬έΘΚΗΟFe(NO3)2 ‘―υ“―Ψ≠±δ÷
D.Al(OH)3÷–Μλ”–…ΌΝΩMg(OH)2ΘΚΦ”»κΉψΝΩ…’Φν»ή“Κ≥δΖ÷Ζ¥”ΠΘ§Ιΐ¬ΥΘ§œρ¬Υ“Κ÷–Ά®»κΙΐΝΩCO2ΚσΙΐ¬Υ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
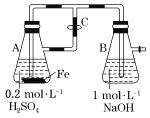
ΓΨΧβΡΩΓΩAΓΔBΓΔCΓΔDΈΣ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΒΡΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§“―÷ΣCΓΔD‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ÷°ΚΆ «AΓΔB‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ÷°ΚΆΒΡ3±ΕΘ§«“CΓΔD‘ΣΥΊ «Ά§÷ςΉε‘ΣΥΊΓΘΦΉΓΔ““ΓΔ±ϊΓΔΕΓΓΔΈλΈε÷÷Εΰ‘ΣΜ·ΚœΈοΒΡΉι≥…»γœ¬±μΘΚ

Έο÷ Φδ¥φ‘ΎΖ¥”ΠΘΚΦΉ+““ΓζΒΞ÷ B+±ϊΘΜΕΓ+ΈλΓζΒΞ÷ D(Β≠ΜΤ…ΪΙΧΧε)+±ϊΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.ΦΉΓΔ““ΓΔ±ϊΓΔΕΓΓΔΈλΨυΈΣ÷ΜΚ§ΦΪ–‘ΦϋΒΡΦΪ–‘Ζ÷Ή”
B.‘≠Ή”ΑκΨΕΘΚD>B>CΘΜΒγΗΚ–‘ΘΚB>C>D
C.Ω…”ΟΨΤΨΪœ¥Β”’≥‘Ύ»ίΤςΡΎ±Ύ…œΒΡΒΞ÷ D
D.»τ2molΦΉ”κ3mol““«ΓΚΟΖ¥”Π…ζ≥…2.5molΒΞ÷ BΘ§‘ρ““ΈΣΥΪ‘≠Ή”Ζ÷Ή”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σ»»Μ·―ßΖΫ≥Χ ΫΘΚSO2(g)+ 1/2O2(g) ![]() SO3(g) ΠΛHΘΫ®D98.32kJΘ·molΘ§‘Ύ»ίΤς÷–≥δ»κ2molSO2ΚΆ1molO2≥δΖ÷Ζ¥”ΠΘ§Ήν÷’Ζ≈≥ωΒΡ»»ΝΩΈΣΘ® Θ©
SO3(g) ΠΛHΘΫ®D98.32kJΘ·molΘ§‘Ύ»ίΤς÷–≥δ»κ2molSO2ΚΆ1molO2≥δΖ÷Ζ¥”ΠΘ§Ήν÷’Ζ≈≥ωΒΡ»»ΝΩΈΣΘ® Θ©
A. 196.64kJB. –Γ”Ύ98.32kJ
C. –Γ”Ύ196.64kJD. ¥σ”Ύ196.64kJ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”Ο50 mL 0.50 mol/LΒΡ―ΈΥα”κ50 mL 0.55 mol/LΒΡ«β―θΜ·ΡΤ»ή“Κ‘Ύ»γœ¬ΆΦΥυ ΨΒΡΉΑ÷Ο÷–Ϋχ––÷–ΚΆΖ¥”ΠΘ§Ά®Ιΐ≤βΕ®Ζ¥”ΠΙΐ≥Χ÷–ΥυΖ≈≥ωΒΡ»»ΝΩΩ…ΦΤΥψ÷–ΚΆ»»ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
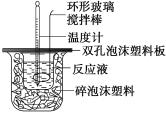
Θ®1Θ©…’±≠ΦδΧν¬ζΥι≈ίΡ≠ΥήΝœΒΡΉς”Ο «_________ΘΜ
Θ®2Θ©ΜΖ–Έ≤ΘΝßΫΝΑηΑτΡήΖώ”ΟΜΖ–ΈΧζ÷ ΫΝΑηΑτ¥ζΧφΘΩ_____Θ®ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ©Θ§Τδ‘≠“ρ «_________
Θ®3Θ© Β―ι ±«β―θΜ·ΡΤ»ή“ΚΒΡ≈®Ε»“Σ”Ο0.55 mol/LΒΡ‘≠“ρ «_________ΘΜ Β―ι÷–»τΗΡ”Ο60 mL 0.50 mol/LΒΡ―ΈΥα”κ50 mL 0.55 mol/LΒΡ«β―θΜ·ΡΤ»ή“ΚΫχ––Ζ¥”ΠΘ§”κ…œ ω Β―ιœύ±»Θ§ΥυΖ≈≥ωΒΡ»»ΝΩ_____Θ®ΧνΓΑœύȖΜρΓΑ≤Μœύ»ñȩȧ»τ Β―ι≤ΌΉςΨυ’ΐ»ΖΘ§‘ρΥυ«σ÷–ΚΆ»»________Θ®ΧνΓΑœύȖΜρΓΑ≤Μœύ»ñȩΘΜ
Θ®4Θ©“―÷Σ‘ΎœΓ»ή“Κ÷–Θ§«ΩΥαΚΆ«ΩΦνΖΔ…ζ÷–ΚΆΖ¥”Π…ζ≥…1 mol Υ° ±Θ§Ζ≈≥ω57.3 kJΒΡ»»ΝΩΘ§‘ρ…œ ωΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣΘΚ _____________ΓΘ
Θ®5Θ©ΒΙ»κNaOH»ή“ΚΒΡ’ΐ»Ζ≤ΌΉς « _________
AΘ°―Ί≤ΘΝßΑτΜΚ¬ΐΒΙ»κΓΓ BΘ°Ζ÷»ΐ¥Έ…ΌΝΩΒΙ»κ CΘ°“Μ¥Έ―ΗΥΌΒΙ»κ
Θ®6Θ©Ρ≥Ά§―ßάϊ”Ο Β―ι ΐΨίΦΤΥψ≥ωΒΡ÷–ΚΆ»»”κ57.3 kJ/mol”–ΤΪ≤νΘ§≤ζ…ζΤΪ≤νΒΡ‘≠“ρΩ…Ρή «(ΧνΉ÷ΡΗ)____________ΓΘ
aΘ° Β―ιΉΑ÷Ο±ΘΈ¬ΓΔΗτ»»–ßΙϊ≤νΘΜ
bΘ°”ΟΈ¬Ε»ΦΤ≤βΕ®NaOH»ή“ΚΤπ ΦΈ¬Ε»Κσ÷±Ϋ”≤βΕ®HCl»ή“ΚΒΡΈ¬Ε»ΘΜ
cΘ°ΝΩ»ΓNaOH»ή“ΚΒΡΧεΜΐ ±―ω ”ΕΝ ΐΘΜ
dΘ°ΒΙΆξNaOH»ή“ΚΚσΘ§ΖΔœ÷ΉΑNaOH…’±≠ΡΎ”–ΦΪ…ΌΝΩ≤–Ντ“ΚΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥–ΓΉιΡβ”ΟΥα–‘KMnO4»ή“Κ”κH2C2O4»ή“ΚΒΡΖ¥”ΠΘ®¥ΥΖ¥”ΠΈΣΖ≈»»Ζ¥”ΠΘ©ά¥ΧΫΨΩΓΑΧθΦΰΕ‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΓ±Θ§≤Δ…ηΦΤΝΥ»γœ¬ΒΡΖΫΑΗΦ«¬Φ Β―ιΫαΙϊΘ®Κω¬‘»ή“ΚΜλΚœΧεΜΐ±δΜ·Θ©ΓΘœό―Γ ‘ΦΝΚΆ“«ΤςΘΚ0.20 mol/L H2C2O4»ή“ΚΓΔ0.010 mol/L KMnO4»ή“ΚΘ®Υα–‘Θ©ΓΔ’τΝσΥ°ΓΔ ‘ΙήΓΔΝΩΆ≤ΓΔΟκ±μΓΔΚψΈ¬Υ°‘Γ≤έΓΘ
ΈοάμΝΩ ±ύΚ≈ | VΘ®0.20 mol/L H2C2O4»ή“ΚΘ©/mL | VΘ®’τΝσΥ°Θ©/mL | VΘ®0.010 mol/LΥα–‘KMnO4»ή“ΚΘ©/mL | mΘ®MnSO4Θ©/g | T/Γφ | ““ |
ΔΌ | 2.0 | 0 | 4.0 | 0 | 50 | |
ΔΎ | 2.0 | 0 | 4.0 | 0 | 25 | |
Δέ | 1.5 | a | 4.0 | 0 | 25 | |
Δή | 2.0 | 0 | 4.0 | 0.1 | 25 |