
科目: 来源: 题型:
【题目】两同学为制得纯净的Fe(OH)2,使用如图所示的装置,A管中是Fe和H2SO4,B管中是NaOH溶液:

(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是___________;
(2)同学乙:打开a,使A管中反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是___________,B中发生反应的离子方程式为____________________________________
(3)在制备纯净的Fe(OH)2实验中,一定要注意避免Fe(OH)2被氧化,一旦实验失败就会看到白色絮状沉淀逐渐变为灰绿色,最后变成红褐色,请写出这个过程的化学方程式,并用单线桥法标出电子转移的方向和数目:_________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)鉴别KCl溶液和K2CO3的试剂是___________,离子方程式为________________。
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是________,离子方程式为___________。
(3)除去Na2CO3粉末中混入的NaHCO3杂质用________方法,化学方程式为_____________。
(4)除去铁粉中混有铝粉的试剂是___________,离子方程式为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,横坐标表示通入气体或加入试剂的体积,纵坐标表示产生沉淀的质量。请把符合下列各种情况的图像字母代码分别填入题后。
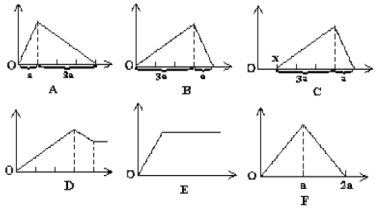
(1)向石灰水中通入二氧化碳:__________。
(2)向AlCl3溶液中加入氨水:__________。
(3)向盐酸和氯化铝的混合溶液中逐滴加入氢氧化钠溶液:__________。
(4)向NaAlO2溶液中滴加盐酸:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】侯德榜制碱法可以做到连续循环生产,其工艺流程如下图所示。完成下列填空:

(1)写出流程中主反应的化学方程式:_________。
(2)流程通过同时利用合成氨厂产生的_______来降低原料成本。副产物b的化学式为______,简述降温条件下加入原料A的作用__________。侯氏制碱法的创新之处就是对母液的循环利用,这是由于母液中含有大量的![]() 、
、![]() 、_______离子。
、_______离子。
某兴趣小组同学制定如下两个方案对含有![]() 杂质的纯碱的含量进行测定:
杂质的纯碱的含量进行测定:
方案一:用如图装置测定样品与足量稀硫酸反应生成![]() 的体积。
的体积。
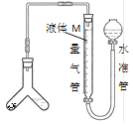
(3)为了减小实验误差,量气管中液体M的选择原则是______。若实验测得样品纯碱含量低于样品实际含量,可能的原因是_________
a ![]() 气体中含有水蒸气 b 测定气体体积时未冷却至室温
气体中含有水蒸气 b 测定气体体积时未冷却至室温
c Y型管中留有反应生成的气体 d 测定气体体积时水准管的液面高于量气管的液面
方案二:通过以下流程测定样品的含量。

(4)操作Ⅰ的名称为________,实验中,恒重的标准为________。根据以上实验过程,含有氯化钠的纯碱样品中碳酸钠的质量分数可表示为:_______。(注明你的表达式中所用的有关符号的含义)
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物N具有镇痛、消炎等药理作用,其合成路线如下:
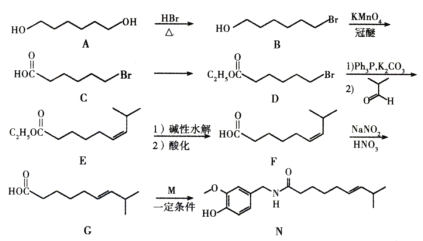
(1)A的系统命名为____________,E中官能团的名称为_____________。
(2)A→B的反应类型为____________,从反应所得液态有机混合物中提纯B的常用方法为_____________。
(3)C→D的的化学方程式为_____________。
(4)C的同分异构体W(不考虑手性异构)可发生银镜反应;且1 mol W最多与2 mol NaOH发生反应,产物之一可被氧化成二元醛。满足上述条件的W有____________种,若W的核磁共振氢谱具有四组峰,则其结构简式为_____________。
(5)参照上述合成路线,以![]() 为原料,采用如下方法制备医药中间体
为原料,采用如下方法制备医药中间体![]() 。
。
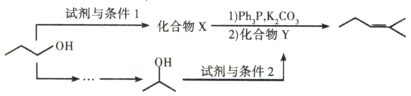
该路线中试剂条件1为____________,X的结构简式为____________;试剂与条件2为____________,Y的结构简式为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应既属于离子反应,又属于氧化还原反应的是( )
A. NaOH溶液与盐酸中和B. Zn与CuSO4 溶液的反应
C. 分解氯酸钾制氧气D. MgCl2溶液 与KOH溶液产生沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】目前铬被广泛应用于冶金、化工、铸铁及高精端科技等领域。回答下列问题:
(1)基态Cr原子价层电子的轨道表达式为_______,其核外有_______种不同能量的电子。
(2)Cr的第二电能离(ICr)和Mn的第二电离能(IMn)分别为1590.6 kJ·mol-1、1509.0 kJ·mol-1,ICr > IMn的原因是____________。
(3)过氧化铬CrO5中Cr的化合价为+6,则该分子中![]() 键、
键、![]() 键的数目之比为______。
键的数目之比为______。
(4)CrCl3的熔点(83℃)比CrF3的熔点(1100℃)低得多,这是因为___________。
(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是_______,阳离子中Cr原子的配位数为_________,ClO![]() 的立体构型为________。
的立体构型为________。

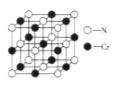
(6)氮化铬晶体的晶胞结构如图所示,Cr处在N所围成的________空隙中,如果N与Cr核间距离为apm,则氮化铬的密度计算式为__________g·cm-3(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在t℃下,某反应达到平衡,平衡常数K=c(NO)c(SO3)/c(NO2)c(SO2)。恒容时,温度升高,NO浓度减小。下列说法正确的是( )
A.该反应的焓变为正值B.恒温下增大压强,反应体系的颜色加深
C.升高温度,逆反应速率减小D.该反应化学方程式为NO+SO3![]() NO2+SO2
NO2+SO2
查看答案和解析>>
科目: 来源: 题型:
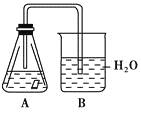
【题目】某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如图所示的装置进行实验,过一段时间后观察,下列现象不可能出现的是( )
A.B中导气管中产生气泡B.B中导气管里形成一段水柱
C.金属片剪口变红D.锌被腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是
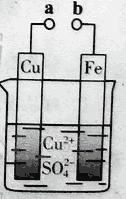
A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com