
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДгЗЯЗАДпЛЏМСжаЛиЪеЗАЃЌМШФмБмУтЖдЛЗОГЕФЮлШОЃЌгжФмНкдМБІЙѓЕФзЪдДЁЃЛиЪеЙЄвеСїГЬШчЯТЃК
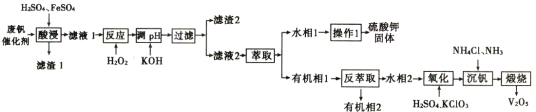
вбжЊЃКЂйЗЯЗАДпЛЏМСжаКЌгаK2SO4ЁЂV2O5ЁЂV2O4ЁЂSiO2ЁЂFe2O3ЁЂAl2O3ЕШЁЃ
ЂкЁАЫсНўЁБЪБV2O5КЭV2O4ЯШгыЯЁH2SO4ЗДгІЗжБ№ЩњГЩ![]() КЭVO2+ЁЃ
КЭVO2+ЁЃ
ЂлгаЛњнЭШЁМСнЭШЁVO2+ЕФФмСІБШнЭШЁ![]() ЕФФмСІЧПЁЃ
ЕФФмСІЧПЁЃ
ЂмШмвКжа![]() гы
гы![]() ПЩЯрЛЅзЊЛЏЃК
ПЩЯрЛЅзЊЛЏЃК![]() ЁЃ
ЁЃ
(1)ЮЊСЫЬсИпЁАЫсНўЁБаЇТЪПЩВЩШЁЕУДыЪЉЮЊ______________________ЁЃ
(2)ЁАЫсНўЁБЪБМгШыFeSO4ФПЕФЪЧ___________ЃЌFeSO4ВЮгыЗДгІЕФЛЏбЇЗНГЬЪНЮЊ__________ЁЃ
(3)ЁАТЫдќ2ЁБЕФГЩЗжЮЊ______________ЃЛЁАВйзї1ЁБЕФУћГЦЮЊ_______________ЁЃ
(4)дкЁАбѕЛЏЁБВНжшжабѕЛЏМСгыЛЙдМСЕФЮяжЪЕФжЪСПжЎБШЮЊ1ЃК6ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ_________________________________________ЁЃ
(5)tЁцЪБЃЌЁАбѕЛЏЁБКѓШмвКжаc(![]() )=0ЃЎ1molЃЏLЃЌМйЩшЁАГСЗАЁБВНжшжа
)=0ЃЎ1molЃЏLЃЌМйЩшЁАГСЗАЁБВНжшжа![]() ШЋВПзЊЛЏ
ШЋВПзЊЛЏ![]() ЃЌВЂЩњГЩNH4VO3ГСЕэЃЌЮЊЪЙГСЗАаЇТЪДяЕН95ЃЅЃЎдђДЫЪБШмвКжаc(
ЃЌВЂЩњГЩNH4VO3ГСЕэЃЌЮЊЪЙГСЗАаЇТЪДяЕН95ЃЅЃЎдђДЫЪБШмвКжаc(![]() )Ён______________ЁЃ[вбжЊtЁцЪБKsp(NH4VO3)=2ЃЎ0ЁС10Ѓ3ЃЌЗДгІЧАКѓШмвКЕФЬхЛ§БфЛЏКіТдВЛМЦ]
)Ён______________ЁЃ[вбжЊtЁцЪБKsp(NH4VO3)=2ЃЎ0ЁС10Ѓ3ЃЌЗДгІЧАКѓШмвКЕФЬхЛ§БфЛЏКіТдВЛМЦ]
(6)ШЁЁАьбЩеЁБКѓЕФV2O5бљЦЗm gНјааВтЖЈЃЌМгШызуСПЯЁСђЫсГфЗжЗДгІКѓЃЌХфГЩ250mLШмвКЁЃШЁИУШмвК25ЃЎ00mLгУbmolЃЏLВнЫсШмвКНјааЕЮЖЈЃЌЯћКФВнЫсШмвКcmLЁЃдђV2O5бљЦЗжаЗАЕФжЪСПЗжЪ§=_________ЃЅЃЌбљЦЗЕФДПЖШЁм___________ЃЅЃЌбљЦЗЕФДПЖШаЁгкИУЪ§жЕПЩФмЕФдвђЪЧ____________________________ЁЃ(вбжЊЃКЂйV2O5+2H+=2![]() +H2O Ђк2
+H2O Ђк2![]() +H2C2O4+2H+=2VO2+2CO2Ёќ+2H2O)
+H2C2O4+2H+=2VO2+2CO2Ёќ+2H2O)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИљОнЯТЭМЫљЪОЕФзЊЛЏЙиЯЕЃЌЛиД№ЯТСаЮЪЬтЃК

(1)аДГіЗДгІЂйЕФРызгЗНГЬЪНЃК______________________________________________ЃЛаДГіЗДгІЂкЕФРызгЗНГЬЪНЃК______________________ЁЃ
(2)ЭЦГіЯТСаЮяжЪЕФЛЏбЇЪНЃКE____________ЃЛI______________ЁЃ
(3)дкЩЯЪізЊЛЏЙ§ГЬжаЃЌBЁЂCЁЂFЁЂHЕФбѕЛЏФмСІгЩШѕЕНЧПЕФЫГађЮЊ______________________(аДЛЏбЇЪН)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЙЄГЇЖдЙЄвЕЩњВњюбАзЗлВњЩњЕФЗЯвКНјаазлКЯРћгУЃЌЗЯвКжаКЌгаДѓСПFeSO4ЁЂH2SO4КЭЩйСПFe2(SO4)3ЃЌПЩгУгкЩњВњбеСЯЬњКьКЭВЙбЊМСШщЫсбЧЬњЁЃЦфЩњВњЙЄвеСїГЬШчЭМЃК
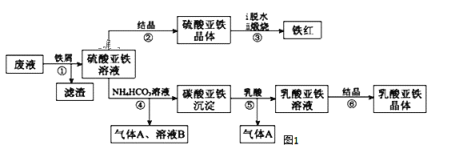
вбжЊЃКШщЫсПЩвдКЭЬМЫсИљЩњГЩЖўбѕЛЏЬМЦјЬхЁЃЧыЛиД№ЃК
ЃЈ1ЃЉВНжшЂмашПижЦЗДгІЮТЖШЕЭгк35ЁцЃЌЦфФПЕФЪЧ___ЁЃ
ЃЈ2ЃЉВНжшЂмЗДгІЕФРызгЗНГЬЪНЪЧ___ЁЃ
ЃЈ3ЃЉвбжЊЃКFeCO3(s) Fe2+(aq)+CO32-(aq)ЃЌЪдгУЦНКтвЦЖЏдРэНтЪЭВНжшЂнЩњГЩШщЫсбЧЬњЕФдвђ___ЁЃ
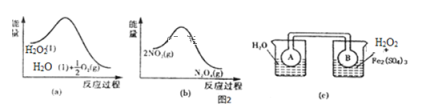
ЃЈ4ЃЉFe3+ЖдH2O2ЕФЗжНтОпгаДпЛЏзїгУЁЃРћгУШчЭМ(a)КЭ(b)жаЕФаХЯЂЃЌАДЭМ(c)зАжУ(СЌЭЈЕФAЁЂBЦПжавбГфгаNO2ЦјЬх)НјааЪЕбщЁЃПЩЙлВьЕНBЦПжаЦјЬхбеЩЋБШAЦПжаЕФ___(ЬюЁАЩюЁБЛђЁАЧГЁБ)ЃЌЦфдвђЪЧ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЕФИїЗНПђБэЪОвЛжжЗДгІЮяЛђЩњГЩЮя(ФГаЉЮяжЪвбОТдШЅ)ЃЌЦфжаГЃЮТЯТAЁЂCЁЂDЮЊЮоЩЋЦјЬхЃЌCФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЁЃ
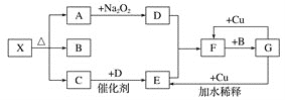
ЃЈ1ЃЉаДГіЮяжЪXЕФЛЏбЇЪНЃК__ЁЃ
ЃЈ2ЃЉаДГіЯТСаБфЛЏЕФЛЏбЇЗНГЬЪНЃК
ЂйAЁњDЃК___ЃЛ
ЂкGЁњEЃК___ЃЛ
ЂлFЁњGЃК___ЁЃ
ЃЈ3ЃЉЪЕбщЪвРяЃЌГЃгУМгШШЙЬЬхЛьКЯЮяЕФЗНЗЈжЦШЁЦјЬхCЃЌЧыаДГіЛЏбЇЗНГЬЪНЃК___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПадбЇЯАаЁзщРћгУЯТСагаЙизАжУЖдSO2ЕФаджЪМАПеЦјжаSO2ЕФКЌСПНјааЬНОПЃЈзАжУЕФЦјУмадвбМьВщЃЉЃК
(1)зАжУAжаЗДгІЕФЛЏбЇЗНГЬЪНЪЧ________ЃЎ
(2)ЕЮМгХЈСђЫсжЎЧАЃЌДђПЊЕЏЛЩМаЃЌЭЈШывЛЖЮЪБМфN2ЃЌдйЙиБеЕЏЛЩМаЃЎДЫВйзїЕФФПЕФЪЧЁЁ______ЁЃ

(3)ЪЕбщЙ§ГЬзАжУBжаУЛгаУїЯдБфЛЏЃЎЪЕбщНсЪјШЁЯТзАжУBЃЌДгжаЗжБ№ШЁЩйСПШмвКгкСНжЇНрОЛЪдЙмжаЃЌЯђЕк1жЇЪдЙмжаЕЮМгЪЪСПАБЫЎГіЯжАзЩЋГСЕэ___________ЃЈЬюЛЏбЇЪНЃЉЃЛЯђЕк2жЇЪдЙмжаЕЮМгЪЪСПаТжЦТШЫЎЃЌШдШЛГіЯжАзЩЋГСЕэЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧ______ЁЃ
(4)зАжУCжаЕФШмвКжаГіЯжЕЛЦЩЋЛызЧ,ИУЪЕбщжЄУїSO2Опга___ адЃЎ
(5)зАжУDЕФзїгУЪЧ______ЁЃ
(6)СэвЛаЁзщРћгУзАжУEНјааЪЕбщЃКSO2аджЪЪЕбщжЎКѓЃЌгУзЂЩфЦїЖдЪЕбщЪвФкПеЦјНјааШЁбљЃЎВЂЯђзАжУEжаЙВзЂШыV mLЃЈвбелЫуЮЊБъПіЯТЬхЛ§ЃЉЕФПеЦјЃЌЕБШмвКИеКУЭЪЩЋЪБЃЌЭЃжЙЪЕбщЃЎЧыМЦЫуИУПеЦјжаSO2ЕФЬхЛ§ЗжЪ§ЃЈгУКЌVЕФДњЪ§ЪНБэЪОЃЉ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТЭМЪЧвЛИіЪЕбщЪвжЦШЁТШЦјВЂвдТШЦјЮЊдСЯНјааЬиЖЈЗДгІЕФзАжУЃЈBжагаЕМЙмКЭвЛИіСЌЭЈЭтНчЕФГЄОБТЉЖЗЃЉЃК

ЃЈ1ЃЉAЪЧТШЦјЗЂЩњзАжУЃЌЦфжаЗДгІЕФЛЏбЇЗНГЬЪНЮЊ__________________________ЃЎ
ЃЈ2ЃЉЪЕбщПЊЪМЪБЃЌЯШЕуШМAДІЕФОЦОЋЕЦЃЌДђПЊа§ШћKЃЌШУCl2ГфТњећИізАжУЃЌдйЕуШМDДІОЦОЋЕЦЃЌCl2ЭЈЙ§CЦПКѓдйНјШыDЁЃDзАжУЕФгВжЪВЃСЇЙмФкЪЂгаЬПЗлЃЌЗЂЩњбѕЛЏЛЙдЗДгІЃЌЦфВњЮяЮЊCO2КЭHClЁЃЪдаДГіDжаЗДгІЕФЛЏбЇЗНГЬЪНЃК___________________ЃЛзАжУCЕФзїгУЪЧ_________________ ЁЃ
ЃЈ3ЃЉдкEДІЃЌзЯЩЋЪЏШяЪдвКЕФбеЩЋгЩзЯЩЋБфЮЊКьЩЋЃЌдйБфЮЊЮоЩЋЃЌЦфдвђЪЧ__ЁЃ
ЃЈ4ЃЉШєНЋEДІЩеБжаШмвКИФЮЊГЮЧхЪЏЛвЫЎЃЌЗДгІЙ§ГЬжаЯжЯѓЮЊ___ЁЃЃЈбЁЬюБъКХЃЉ
ЃЈAЃЉгаАзЩЋГСЕэЩњГЩЃЈBЃЉЮоУїЯдБфЛЏЃЈCЃЉЯШЩњГЩАзЩЋГСЕэЃЌЖјКѓАзЩЋГСЕэЯћЪЇ
ЃЈ5ЃЉDДІЗДгІЭъБЯКѓЃЌЙиБеа§ШћKЃЌвЦШЅОЦОЋЕЦЃЌЕЋгЩгкгрШШЕФзїгУЃЌAДІШдгаCl2ВњЩњЃЌДЫЪБBжаЕФЯжЯѓЪЧ__ЃЌBЕФзїгУЪЧ___________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊ![]() ЮЊжабЇЛЏбЇжавЛжжГЃМћЕФбЮЃЌ
ЮЊжабЇЛЏбЇжавЛжжГЃМћЕФбЮЃЌ![]() ЮЊЕЛЦЩЋЙЬЬхЃЛ
ЮЊЕЛЦЩЋЙЬЬхЃЛ![]() ЁЂ
ЁЂ![]() ЮЊГЃМћЕФН№ЪєЃЌ
ЮЊГЃМћЕФН№ЪєЃЌ![]() ЕФбѕЛЏЮяПЩзїФЭЛ№ВФСЯЃЌПЩгУЫќРДжЦдьФЭЛ№лсліКЭФЭИпЮТЪдбщвЧЦїЃЛ
ЕФбѕЛЏЮяПЩзїФЭЛ№ВФСЯЃЌПЩгУЫќРДжЦдьФЭЛ№лсліКЭФЭИпЮТЪдбщвЧЦїЃЛ![]() ЮЊЦјЬхЕЅжЪЃЌ
ЮЊЦјЬхЕЅжЪЃЌ![]() ЮЊЮоЩЋЦјЬхЃЌ
ЮЊЮоЩЋЦјЬхЃЌ![]() дкПеЦјжаЛсГіЯжКьзиЩЋЃЌИїЮяжЪЕФзЊЛЏЙиЯЕШчЯТЭМ(ВПЗжЗДгІВњЮявбТдШЅ)ЁЃ
дкПеЦјжаЛсГіЯжКьзиЩЋЃЌИїЮяжЪЕФзЊЛЏЙиЯЕШчЯТЭМ(ВПЗжЗДгІВњЮявбТдШЅ)ЁЃ
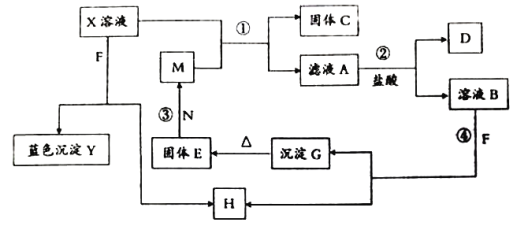
ЧыЛиД№ЯТСаЮЪЬтЃЛ
(1)![]() бѕЛЏЮяЕФЛЏбЇЪНЮЊ__________ЃЌ
бѕЛЏЮяЕФЛЏбЇЪНЮЊ__________ЃЌ![]() ЕФЕчзгЪНЮЊ_________ЁЃ
ЕФЕчзгЪНЮЊ_________ЁЃ
(2)ЗДгІЂлЕФЛЏбЇЗНГЬЪНЮЊ_________________ЁЃ
(3)дкЗДгІЂйЂкЂлЂмжаВЛЪєгкжУЛЛЗДгІЕФЪЧ________________(ЬюађКХ)ЁЃ
(4)аДГі![]() гы
гы![]() вдЕШЮяжЪЕФСПНјааЗДгІЕФРызгЗНГЬЪН________________ЁЃ
вдЕШЮяжЪЕФСПНјааЗДгІЕФРызгЗНГЬЪН________________ЁЃ
(5)![]() КЭ
КЭ![]() ЕФЛьКЯШмвКЃЌгУЪЏФЋзїЕчМЋЕчНтДЫШмвКЃЌЕБЭЈЕчвЛЖЮЪБМфКѓЃЌСНМЋОљЪеМЏЕН
ЕФЛьКЯШмвКЃЌгУЪЏФЋзїЕчМЋЕчНтДЫШмвКЃЌЕБЭЈЕчвЛЖЮЪБМфКѓЃЌСНМЋОљЪеМЏЕН![]() ЦјЬх(БъзМзДПіЯТ)ЃЌМйЖЈЕчНтКѓШмвКЬхЛ§ШдЮЊ
ЦјЬх(БъзМзДПіЯТ)ЃЌМйЖЈЕчНтКѓШмвКЬхЛ§ШдЮЊ![]() ЁЃ
ЁЃ
ЂйаДГіЕчНтЪБбєМЋЕФЕчМЋЗДгІЪН____________________ЃЛ
ЂкЕчНтКѓШмвКжа![]() ЮЊ____________________
ЮЊ____________________![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯПЩгУ![]() гы
гы![]() КЯГЩбЧЯѕѕЃТШ
КЯГЩбЧЯѕѕЃТШ![]() ЃЌПЩвдгУгкгаЛњКЯГЩЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЌПЩвдгУгкгаЛњКЯГЩЁЃЛиД№ЯТСаЮЪЬтЃК
(1)вЛЖЈЬѕМўЯТЃЌЕЊбѕЛЏЮягыаќИЁдкДѓЦјжаЕФКЃбЮСЃзгЯрЛЅзїгУЪБЛсЩњГЩбЧЯѕѕЃТШЃЌЩцМАгаЙиЗДгІЕФШШЛЏбЇЗНГЬЪНШчЯТЃК
Ђй![]()
Ђк![]()
Ђл![]()
дђ![]()
![]() __________(гУ
__________(гУ![]() ЁЂ
ЁЂ![]() БэЪО)ЁЃ
БэЪО)ЁЃ
(2)![]() ЪБЃЌдквЛУмБеШнЦїжаЗЂЩњЗДгІЃК
ЪБЃЌдквЛУмБеШнЦїжаЗЂЩњЗДгІЃК![]() ЃЌЦфе§ЗДгІЫйТЪБэДяЪН
ЃЌЦфе§ЗДгІЫйТЪБэДяЪН![]() ЁЃВтЕУе§ЗДгІЫйТЪКЭЖдгІХЈЖШЕФЪ§ОнШчБэЃК
ЁЃВтЕУе§ЗДгІЫйТЪКЭЖдгІХЈЖШЕФЪ§ОнШчБэЃК
ађКХ |
|
|
Ђй |
|
|
Ђк |
|
|
Ђл |
|
|
дђ![]() __________ДяЕНЦНКтКѓЃЌШєМѕаЁбЙЧПЃЌдђЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПНЋ__________(бЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
__________ДяЕНЦНКтКѓЃЌШєМѕаЁбЙЧПЃЌдђЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПНЋ__________(бЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
(3)![]() ЪБЃЌЯђЬхЛ§ЮЊ
ЪБЃЌЯђЬхЛ§ЮЊ![]() ЧвДјЦјбЙМЦЕФКуШнУмБеШнЦїжаЭЈШы
ЧвДјЦјбЙМЦЕФКуШнУмБеШнЦїжаЭЈШы![]() КЭ
КЭ![]() ЗЂЩњЗДгІЃК
ЗЂЩњЗДгІЃК
![]() ЁЃвбжЊЃКЗДгІЦ№ЪМКЭЦНКтЪБЮТЖШЯрЭЌЁЃ
ЁЃвбжЊЃКЗДгІЦ№ЪМКЭЦНКтЪБЮТЖШЯрЭЌЁЃ

ЂйВтЕУЗДгІЙ§ГЬжабЙЧП![]() ЫцЪБМф
ЫцЪБМф![]() ЕФБфЛЏШчЭМ1ЧњЯп
ЕФБфЛЏШчЭМ1ЧњЯп![]() ЫљЪОЃЌдђ
ЫљЪОЃЌдђ![]() __________(бЁЬюЁА>ЁБЁЂЁА<ЁБЛђЁАВЛШЗЖЈЁБ)0ЃЛШєЦфЫћЬѕМўЯрЭЌЃЌНіИФБфФГвЛЬѕМўЪБЃЌВтЕУбЙЧП
__________(бЁЬюЁА>ЁБЁЂЁА<ЁБЛђЁАВЛШЗЖЈЁБ)0ЃЛШєЦфЫћЬѕМўЯрЭЌЃЌНіИФБфФГвЛЬѕМўЪБЃЌВтЕУбЙЧП![]() ЫцЪБМф
ЫцЪБМф![]() ЕФБфЛЏШчЭМ1ЧњЯп
ЕФБфЛЏШчЭМ1ЧњЯп![]() ЫљЪОЃЌдђИФБфЕФЬѕМўЪЧ_________ЁЃ
ЫљЪОЃЌдђИФБфЕФЬѕМўЪЧ_________ЁЃ
ЂкЭМ2ЪЧСНЮЛЭЌбЇУшЛцЕФЩЯЪіЗДгІЦНКтГЃЪ§ЕФЖдЪ§жЕ![]() гыЮТЖШЕФБфЛЏЙиЯЕЭМЯѓЃЌЦфжае§ШЗЕФЧњЯпЪЧ______(бЁЬюЁАМзЁБЛђЁАввЁБ)ЃЛ
гыЮТЖШЕФБфЛЏЙиЯЕЭМЯѓЃЌЦфжае§ШЗЕФЧњЯпЪЧ______(бЁЬюЁАМзЁБЛђЁАввЁБ)ЃЛ![]() ЕФжЕЮЊ______ЁЃ
ЕФжЕЮЊ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯЭЈГЃРћгУSiO2 КЭЬМЗДгІРДжЦШЁЙшЃЌаДГіЗДгІЕФЛЏбЇЗНГЬЪН___________________ЁЃ
ЙЄвЕЩЯЛЙПЩвдРћгУУОжЦШЁЙшЃЌЗДгІЮЊ2Mg+SiO2 = 2MgO+SiЃЌЭЌЪБЛсЗЂЩњИБЗДгІЃК2Mg + Si = Mg2SiЁЃШчЭМЪЧНјааMgгыSiO2ЗДгІЕФЪЕбщзАжУЃЌЪдЛиД№ЯТСаЮЪЬтЃК

ЃЈ1ЃЉгЩгкO2КЭH2OЃЈgЃЉЕФДцдкЖдИУЪЕбщгаНЯДѓгАЯьЃЌЪЕбщжагІЭЈШыЦјЬхXзїЮЊБЃЛЄЦјЃЌЪдЙмжаЕФЙЬЬхвЉЦЗПЩбЁгУ________(ЬюађКХ)ЁЃ
aЃЎЪЏЛвЪЏЁЁЁЁЁЁbЃЎаПСЃЁЁЁЁЁЁcЃЎДПМю
ЃЈ2ЃЉЪЕбщПЊЪМЪБЃЌБиаыЯШЭЈвЛЖЮЪБМфXЦјЬхЃЌдйМгШШЗДгІЮяЃЌЦфРэгЩЪЧ ___________________________ЃЛЕБЗДгІв§ЗЂКѓЃЌвЦзпОЦОЋЕЦЃЌЗДгІФмМЬајНјааЃЌЦфдвђЪЧ______________________ЁЃ
ЃЈ3ЃЉЗДгІНсЪјКѓЃЌД§РфШДжСГЃЮТЪБЃЌЭљЗДгІКѓЕФЛьКЯЮяжаМгШыЯЁбЮЫсЃЌПЩЙлВьЕНЩСССЕФЛ№аЧЃЌВњЩњДЫЯжЯѓЕФдвђЪЧИБВњЮяMg2SiгібЮЫсбИЫйЗДгІЩњГЩSiH4ЃЈЙшЭщЃЉЦјЬхЃЌШЛКѓSiH4здШМЃЎгУЛЏбЇЗНГЬЪНБэЪОетСНИіЗДгІЂй________________________Ђк___________________ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏКЯЮяFЪЧвЛжжГЃМћЕФЛЏЙЄдСЯЃЌПЩвдЭЈЙ§вдЯТЗНЗЈКЯГЩЃК
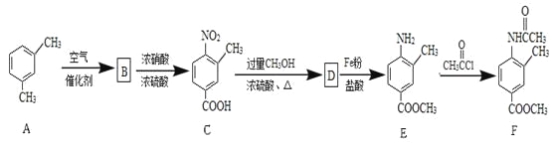
ЃЈ1ЃЉаДГіЛЏКЯЮяCжаКЌбѕЙйФмЭХЕФУћГЦЃК_________КЭ___________ЁЃ
ЃЈ2ЃЉЛЏКЯЮяBЕФНсЙЙМђЪНЮЊ___________ЃЛгЩDЁњEЕФЗДгІРраЭЪЧ___________ЁЃ
ЃЈ3ЃЉаДГіCЁњDЗДгІЕФЛЏбЇЗНГЬЪНЃК___________ЁЃ
ЃЈ4ЃЉаДГіЭЌЪБТњзуЯТСаЬѕМўЕФEЕФвЛжжЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНЃК___________ЁЃ
ЂёЃЎФмЗЂЩњвјОЕЗДгІ ЃЛ ЂђЃЎЫЎНтВњЮяжЎвЛгіFeCl3ШмвКЯдЩЋЃЛ
ЂѓЃЎЗжзгжаКЌга4жжВЛЭЌЛЏбЇЛЗОГЕФЧтЁЃ
ЃЈ5ЃЉвбжЊ![]() ЁЃЧыаДГівд
ЁЃЧыаДГівд![]() ЮЊдСЯЃЌжЦБИЛЏКЯЮя
ЮЊдСЯЃЌжЦБИЛЏКЯЮя![]() ЕФКЯГЩТЗЯпСїГЬЭМ(ЮоЛњЪдМСПЩШЮбЁ)_______________ЁЃ
ЕФКЯГЩТЗЯпСїГЬЭМ(ЮоЛњЪдМСПЩШЮбЁ)_______________ЁЃ
КЯГЩТЗЯпСїГЬЭМЪОР§ШчЯТЃК![]()
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com