
科目: 来源: 题型:
【题目】2019年3月21日是第二十七届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100![]() ,进行了三组实验,其操作和有关图像如下图所示,请回答下列问题:
,进行了三组实验,其操作和有关图像如下图所示,请回答下列问题:

(1)根据上述3组实验可以分析废水中一定不存在的阴离子是_______,一定存在的阳离子是_____。
(2)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为_______
(3) 若通过实验确定原废水中c(Na+)=0.14mol/L,试判断原废水中NO3-是否存在?_____(填“存在”“不存在”或“不确定”)。若存在,c(NO3-)=______mol/L。(若不存在或不确定则此空不填)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在化学分析中,常常需要用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。用Na2C2O4固体测定KMnO4溶液浓度的实验步骤如下:(反应原理为:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O)
步骤一:先粗配浓度约为0.15mol/L的KMnO4溶液500mL。
步骤二:准确称取Na2C2O4固体mg放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配KMnO4溶液进行滴定。记录相关数据。
步骤三:重复步骤二两到三次。计算得KMnO4溶液的物质的量浓度。
试回答下列问题:
(1)盛放KMnO4溶液的滴定管为___(填“酸式”或“碱式”)滴定管。
(2)该滴定实验滴定终点的现象是___。
(3)步骤二中滴定操作如图所示,正确的操作是___(填编号)。
A. B.
B. C.
C.
(4)若m的数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为___mol/L。
(5)若滴定完毕后读数时俯视,则实验误差会__(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学通过以下装置测定M样品(只含Fe、Al、Cu)中各成分的质量分数。取两份质量均为m g的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为V1 mL和V2 mL(已折算到标准状况下)。
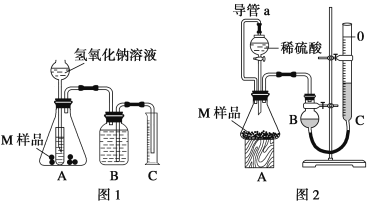
(1)写出实验1中可能发生反应的离子方程式:____________。
(2)该实验需要0.50 mol·L-1的NaOH溶液480 mL,请回答下列问题:
①配制时应用托盘天平称量______g NaOH,应选择________ ml容量瓶。
②配制NaOH溶液时,NaOH固体中含有Na2O杂质会导致所配溶液浓度________。(填“偏大”、“偏小”或“无影响”)。
(3)该实验中所用稀硫酸是用98%的浓硫酸(ρ=1.84g/cm3)配制的,则该浓硫酸的物质的量浓度是_______。
(4)对于实验2,读数时冷却至室温除视线平视外,还应进行的操作是: ___________。
(5)实验2中导管a的作用_________。
(6)M样品中铜的质量的数学表达式为(用V1和V2 表示):_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为相互串联的甲乙两个电解池,请回答:
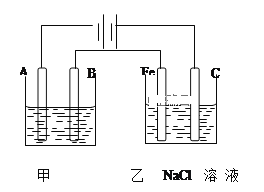
(1)甲池若为用电解原理精炼铜的装置,A极是__极,材料是___,B极电极反应方程式为___。
(2)乙池中若滴入少量酚酞试液,开始一段时间后,___极(填“Fe”或“C”)附近变红色。
(3)若乙槽阳极放出气体在标准状况下的体积为2.24L,
①甲槽阴极增重___g。
②若乙槽电解后得到碱液的物质的量浓度为2moL/L,则乙槽剩余液体体积为__mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属铜、铁、铝等在人类文明史上先后被广泛使用。回答下列问题:
(1)铜、银、金三种金属在元素周期表同族且依次相邻,因此价电子层结构相似。银原子价层电子排布式为________;金元素在周期表的位置是________。
(2)观察如下循环图可以获知FeO的晶格能为________ kJ·mol-1。

(3)氯化铝熔点194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成式为Al2Cl6,其结构式为________;气态氯化铝中存在________(填选项标号)
A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(4)石墨微观结构如下图。其中碳原子杂化类型为________。金刚石晶体中碳碳键键长为0.155nm。金刚石的熔点略低于石墨,而远高于C60的原因是________。
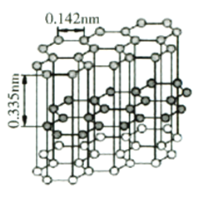
(5)设阿伏加德罗常数值为NA,则石墨的密度为________![]() (列出计算表达式)
(列出计算表达式)
查看答案和解析>>
科目: 来源: 题型:
【题目】依据电化学知识,解决下列问题:
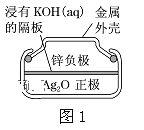
(1)图1为锌银电池,负极是Zn,正极是Ag2O,电解质是KOH。写出该电池负极电极反应式:___,电池工作时,正极区周围溶液的pH___(填“增大”、“减小”、“不变”)。
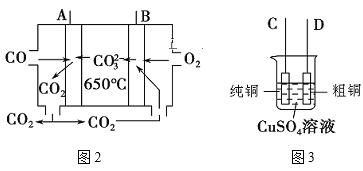
(2)图2是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,图3是粗铜精炼的装置图,现用该燃料电池为电源进行粗铜的精炼实验。
①写出A极的电极反应式:___。
②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与__极(填“C”或“D”)相连。
③当消耗标准状况下2.24LO2时,C电极的质量变化为___。
查看答案和解析>>
科目: 来源: 题型:
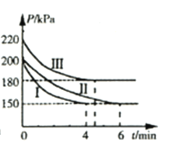
【题目】工业上用CO2和NH3合成尿素 [CO(NH2)2]。某研发小组为合成尿素进行如下实验:向5L恒容密闭容器中通入0.2molNH3和0.1molCO2,分别进行Ⅰ、Ⅱ、Ⅲ三组实验。在不同条件下发生反应:![]() ,反应体系总压强随时间的变化曲线如图所示。
,反应体系总压强随时间的变化曲线如图所示。
(1)已知:
①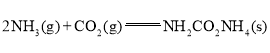
![]()
②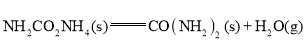
![]()
用CO2和NH3合成尿素的热化学方程式为________。
(2)Ⅰ、Ⅱ、Ⅲ三组实验中,反应温度最高的是________。(填“Ⅰ”、“Ⅱ”或“Ⅲ”)
(3)Ⅰ、Ⅲ两组实验中,NH3转化率较高的是________。(填“Ⅰ”或“Ⅲ”)
(4)若要增加实验Ⅱ的反应速率并提高NH3转化率,改变下列条件可以实现的是________(填标号)
A.增加CO2的物质的量 B.加入惰性气体使压强增大
C.升高反应的温度 D.改用2L的容器进行实验
(5)Ⅰ、Ⅱ两组实验中,反应达到平衡的时间不同,可能的原因是________。
(6)第Ⅱ组实验开始6min内NH3的平均反应速率为________![]() ,平衡常数
,平衡常数![]() ________。
________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答以下问题:
(1)写出![]() 溶液与稀硫酸反应的离子方程式___________,等物质的量的
溶液与稀硫酸反应的离子方程式___________,等物质的量的![]() 与
与![]() 固体分别与足量的硫酸反应,消耗硫酸的物质的量之比为________。
固体分别与足量的硫酸反应,消耗硫酸的物质的量之比为________。
(2)在![]() 稀
稀![]() 反应中,________是氧化剂;________是还原剂;氧化剂与还原剂的物质的量之比为__________
反应中,________是氧化剂;________是还原剂;氧化剂与还原剂的物质的量之比为__________
(3)向酸性高锰酸钾溶液中滴加硫酸亚铁,紫色逐渐褪去,写出该反应的离子方程式: _______。
(4)将![]() 的钠、镁、铝分别投入
的钠、镁、铝分别投入![]() 的硫酸溶液中,三者产生氢气的体积比是________。
的硫酸溶液中,三者产生氢气的体积比是________。
(5)等质量的Fe分别与足量的![]() 、S、
、S、![]() 反应转移电子数之比为_______;
反应转移电子数之比为_______;
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20mL0.10molL-1醋酸溶液中滴加0.10molL-1NaOH溶液,滴加过程中测得pH与NaOH溶液体积(V)的关系如图所示。下列说法正确的是( )
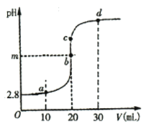
A.m=7
B.由水电离出的c(H+):a>b>c>d
C.由图可知,醋酸Ka的数量级为10-6
D.b与d之间的任意一点c都有:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素,Y与W的最高化合价之和为8,X与Z同主族,且Z的核电荷数是X的2倍。下列说法正确的是( )
A.简单气态氢化物的稳定性:X>ZB.简单离子半径:![]()
C.由X、Y组成的化合物中不含共价键D.最高价氧化物对应水化物的酸性:Z>W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com