
【题目】如图为相互串联的甲乙两个电解池,请回答:
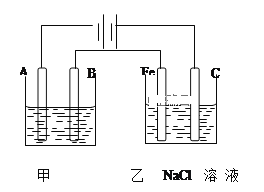
(1)甲池若为用电解原理精炼铜的装置,A极是__极,材料是___,B极电极反应方程式为___。
(2)乙池中若滴入少量酚酞试液,开始一段时间后,___极(填“Fe”或“C”)附近变红色。
(3)若乙槽阳极放出气体在标准状况下的体积为2.24L,
①甲槽阴极增重___g。
②若乙槽电解后得到碱液的物质的量浓度为2moL/L,则乙槽剩余液体体积为__mL。
【答案】阴 精铜或纯铜 Cu-2e-=Cu2+ Fe 6.4 100
【解析】
(1)甲池若为用电解原理精炼铜的装置,A极与电源负极相连,应为阴极。答案为:阴;
因为此电池是精炼铜的装置,所以阴极材料为精铜。答案为:精铜或纯铜;
B极为阳极,电极反应方程式为Cu-2e-=Cu2+。答案为:Cu-2e-=Cu2+
(2)乙池中,阴极的电极反应式为:2H2O+2e-=2OH-+H2↑;
若滴入少量酚酞试液,开始一段时间后,阴极即Fe电极附近变红色。
答案为:Fe;
(3)乙槽中阳极发生的反应为:2Cl--2e- =Cl2↑,若放出气体在标准状况下的体积为2.24L,
则失去的电子为0.2mol。
①甲槽阴极反应为Cu2++2e-=Cu,依据电子守恒,生成Cu 0.1mol,质量为6.4g。
答案6.4;
②在乙槽中,得到的碱液为NaOH,其物质的量为:
![]() ,
,
![]()
答案为:100。


科目:高中化学 来源: 题型:
【题目】下列实验操作能够达到实验目的的是( )
A.液溴易挥发,在存放液溴的试剂瓶中应加入少量水
B.实验室采用如图所示装置收集Cl2
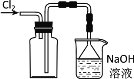
C.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤
D.用酒精萃取碘水中的碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用固体氧化物电解池(SOEC)可实现乙烷电化学脱氢制乙烯,原理示意图如图。下列说法错误的是
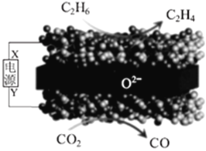
A.X电极的电势高于Y电极
B.该装置在工作过程中,O2-在固体氧化物中由下方向上方迁移
C.该过程总反应的方程式为:C2H6+CO2![]() C2H4+CO+H2O
C2H4+CO+H2O
D.阴极区发生的反应为:CO2+2e-+2H+=CO+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下pH为2的盐酸,下列叙述正确的是( )
A.将10mL该溶液稀释至100mL后,pH=4
B.向该溶液中加入等体积pH为12的氨水恰好完全中和
C.该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为1010:1
D.该溶液中由水电离出的c(H+)水×c(OH-)水=1×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.10molL-1醋酸溶液中滴加0.10molL-1NaOH溶液,滴加过程中测得pH与NaOH溶液体积(V)的关系如图所示。下列说法正确的是( )
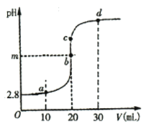
A.m=7
B.由水电离出的c(H+):a>b>c>d
C.由图可知,醋酸Ka的数量级为10-6
D.b与d之间的任意一点c都有:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知A、I为常见金属单质,B、H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
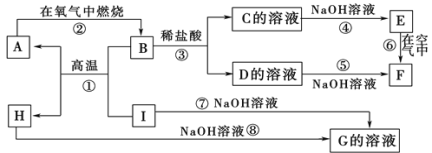
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是______,H的化学式为_______。
(2)反应③的离子方程式为 ____________,向G中通少量CO2的离子方程式为__________。
(3)反应⑥化学方程式___________。
(4)C中阳离子检验方法:______。
(5)1mol I发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准况下占______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离可达到平衡:H2O![]() H++OH–;△H>0,下列叙述正确的是
H++OH–;△H>0,下列叙述正确的是
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 将水加热,Kw增大,pH不变
C. 向水中加入少量稀硫酸,c(H+)增大,Kw不变
D. 向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol/L的盐酸滴定0.1mol/L的Na2CO3溶液25mL。测得溶液pH变化曲线如图,下列说法正确的是( )

A. b点时,c(CO32-)>c(HCO3-)>c(OH-)
B. d点时,c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C. e点时,c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
D. c→d发生的主要离子反应:H++HCO3-=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究物质的组成、结构有利于更好的理解物质的性质。

⑴图3是As4S4分子的结构,该分子中含非极性共价键的数目是_____;基态As原子的外围电子排布式是______。
⑵图1是某种晶体的晶胞,该晶体的化学式是______。
⑶图1对应物质与图3对应物质熔点较高的是______,原因是______。
⑷NaCl的熔点为801.3℃,MgO的熔点高达2800℃。MgO熔点高的原因是______。
⑸图3所示是硼酸晶体的层状结构,层内H3BO3分子通过氢键相连。H3BO3分子B原子的轨道杂化方式是______,1 mol H3BO3晶体中含有的氢键数目是_____。
⑹金刚石、晶体硅、金刚砂(SiC)的晶体类型相同,它们的熔点由高到低的顺序是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com