
科目: 来源: 题型:
【题目】草酸亚铁晶体(![]() )常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
)常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
I.纯净的草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究,小组成员采用如下装置(可重复选用)进行实验:

①E中盛装碱石灰的仪器名称为__________________。
②按照气流从左到右的方向,上述装置的接口顺序为![]() ___________尾气处理装置。
___________尾气处理装置。
③实验前先通入一段时间![]() ,其目的是________________________。
,其目的是________________________。
④实验证明气体产物中含有![]() ,依据的实验现象为_________________________________。
,依据的实验现象为_________________________________。
(2)![]() 受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,![]() 晶体受热分解的化学方程式_________________________。
晶体受热分解的化学方程式_________________________。

(3)晒制蓝图时,以![]() 溶液为显色剂,写出
溶液为显色剂,写出![]() 与
与![]() 溶液反应的化学方程式____________。
溶液反应的化学方程式____________。
Ⅱ.草酸亚铁晶体样品纯度的测定
(4)工业制得的草酸亚铁晶体中常含有![]() 杂质测定其纯度的步骤如下:
杂质测定其纯度的步骤如下:
步骤1:称取![]() 草酸亚铁晶体样品溶于稀
草酸亚铁晶体样品溶于稀![]() 中,配成
中,配成![]() 溶液;
溶液;
步骤2:取上述溶液![]() ,用
,用![]() ,标准液滴定至终点消耗标准液
,标准液滴定至终点消耗标准液![]() ;
;
步骤3:向反应后溶液中加入适量锌粉充分反应后加人适量稀![]() ,再用
,再用![]() 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液![]()
①步骤2中滴定终点的现象为_______________,,步骤3中加入锌粉的目的是__________________。
②草酸亚铁晶体样品的纯度为_________________(写出计算表达式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】照相底片定影时,常用定影液硫代硫酸钠(![]() )溶解未曝光的溴化银(
)溶解未曝光的溴化银(![]() ),生成含
),生成含![]() 的废定影液再向其中加入
的废定影液再向其中加入![]() 使
使![]() 中的银转化为
中的银转化为![]() ,使定影液再生。将
,使定影液再生。将![]() 在高温下转化为Ag,达到回收银的目的。回答下列问题:
在高温下转化为Ag,达到回收银的目的。回答下列问题:
(1)元素周期表中,铜、银、金位于同一副族相邻周期,则基态银原子的最外层电子排布式为__________________。
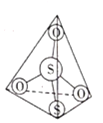
(2)![]() 离子结构如图所示,其中心硫原子的杂化方式为___________。基态S原子中,核外电子占据的最高能级的符号是__________,占据最高能级电子的电子云轮廓图为________形。
离子结构如图所示,其中心硫原子的杂化方式为___________。基态S原子中,核外电子占据的最高能级的符号是__________,占据最高能级电子的电子云轮廓图为________形。
(3)写出![]() 溶于
溶于![]() 溶液反应的离子方程式______。
溶液反应的离子方程式______。![]() 中存在的作用力有离子键、共价键、__________。
中存在的作用力有离子键、共价键、__________。
(4)在空气中灼烧![]() 生成
生成![]() 和
和![]() ,
,![]() 分子的空间构型为__________。分子中的大
分子的空间构型为__________。分子中的大![]() 键可用符号
键可用符号![]() 表示,其中m代表参与形成大
表示,其中m代表参与形成大![]() 键的原子数n代表参与形成大
键的原子数n代表参与形成大![]() 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大![]() 键可表示为
键可表示为![]() ),则
),则![]() 中的大
中的大![]() 键应表示为_________。
键应表示为_________。
(5)![]() 的键角小于
的键角小于![]() 的键角,原因是_________________。
的键角,原因是_________________。
(6)用X射线衍射法可测定阿伏加德罗常数。由金的X射线衍射图像可知金的晶胞属于面心立方晶胞。若金原子的半径为![]() ,金的密度为
,金的密度为![]() ,摩尔质量为
,摩尔质量为![]() ,列出计算阿伏加德罗常数的算式_________(用含
,列出计算阿伏加德罗常数的算式_________(用含![]() 的表达式表示)。
的表达式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机化合物9,10-二甲基菲的结构如图所示,下列关于该物质的说法正确的是

A. 该物质分子式为C16H12
B. 该物质与甲苯互为同系物
C. 该物质能与溴水发生取代反应和加成反应
D. 该物质苯环上七氯代物的同分异构体有4种
查看答案和解析>>
科目: 来源: 题型:
【题目】依据粗盐提纯的原理,除去氯化钾溶液中少量的氯化镁、硫酸镁等杂质,可选用氢氧化钡溶液、稀盐酸和碳酸钾溶液三种试剂,按如图步骤操作:
![]()
(1)A的化学式是__________,B的化学式是________,C的化学式是__________。
(2)加入过量A的目的是__________________。
(3)加入过量B的目的是____________________。
(4)加热煮沸的目的是________________________。
(5)操作Ⅰ的名称是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙_________,F__________。
(2)写出下列反应的离子方程式:
①金属A和水反应_______________。②红褐色沉淀C与物质E反应__________。
③F与黄绿色气体乙反应____________。
④实验室常用氢氧化钠吸收实验过程中的黄绿色气体乙,写出用氢氧化钠溶液吸收该气体的离子方程式___。
(3)将G溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在______之间,验证的简单方法是:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一氧化碳和氢气是重要的化工原料,常用于合成甲醇、二甲醚、甲酸甲酯等有机物。
(1)已知![]() 的燃烧热分别是
的燃烧热分别是![]() ,则甲醇与一氧化碳催化合成乙酸的热化学方程式为_____________。
,则甲醇与一氧化碳催化合成乙酸的热化学方程式为_____________。
(2)有人设想将![]() 按下列反应除去
按下列反应除去![]() ,该反应能否自发进行______________(填“是”或“否”),依据是_____________。
,该反应能否自发进行______________(填“是”或“否”),依据是_____________。
(3)向体积可变的密闭容器中投入![]() 和
和![]() ,在不同条件下发生反应:
,在不同条件下发生反应:![]() 。测得
。测得![]() 的平衡转化率随温度、压强的变化如图所示。
的平衡转化率随温度、压强的变化如图所示。
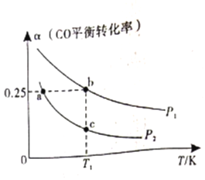
①该可逆反应的![]() __________0(填>”、“<”或“=”)。a、b、c三点对应的平衡常数
__________0(填>”、“<”或“=”)。a、b、c三点对应的平衡常数![]() 的大小关系是____________________。
的大小关系是____________________。
②在恒温恒容条件下进行该反应,能表示反应达到平衡状态的是______________(填字母)。
a. CO的体积分数保持不变
b. 容器内混合气体的密度保持不变
c.容器内混合气体的平均摩尔质量保持不变
d.单位时间内消耗CO的浓度等于生成![]() 的浓度
的浓度
(4)在催化剂作用下,![]() 时分别进行反应:
时分别进行反应:![]() ,
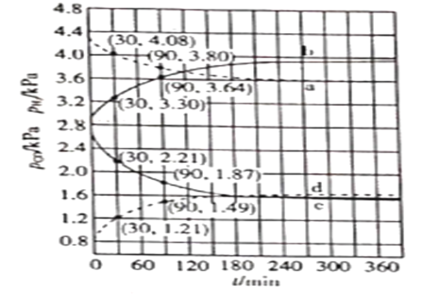
,![]() ,测得CO和
,测得CO和![]() 的分压随时间的变化关系如图所示。起始时,体系中
的分压随时间的变化关系如图所示。起始时,体系中![]() 和
和![]() 相等、
相等、![]() 和
和![]() 相等。计算曲线a的反应在
相等。计算曲线a的反应在![]() 内的平均速率
内的平均速率![]() _______
_______![]() 。
。![]() 时
时![]() 随时间变化关系的曲线是_______,
随时间变化关系的曲线是_______,![]() 时
时![]() 随时间变化关系的曲线是___________。
随时间变化关系的曲线是___________。
(5)一定条件下,![]() 与粉末状氢氧化钠反应生成甲酸钠。已知:常温时,甲酸的电离平衡常数
与粉末状氢氧化钠反应生成甲酸钠。已知:常温时,甲酸的电离平衡常数![]() 。向
。向![]() 的甲酸钠溶液中加入
的甲酸钠溶液中加入![]() 的盐酸,混合液呈__________性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为__________________。
的盐酸,混合液呈__________性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为

下列说法正确的是( )
A. 上述反应为取代反应 B. 脱氢维生素C的分子式为C6H5O6
C. 滴定时应剧烈振荡锥形瓶 D. 滴定时可用淀粉溶液作指示剂
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用一定浓度的盐酸滴定某浓度的氨水。滴定终点附近溶液的pH和导电能力的变化如图所示(利用溶液导电能力的变化可判断滴定终点,溶液总体积变化忽略不计)。下列说法错误的是( )

A.a点对应的溶液中:![]()
B.a→b过程中,![]() 不断增大
不断增大
C.c→d溶液导电性增强的主要原因是![]() 和
和![]() 增大
增大
D.根据溶液pH和导电能力的变化可判断:![]()
查看答案和解析>>
科目: 来源: 题型:
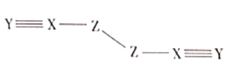
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物![]() 的结构式如图所示。下列说法错误的是( )
的结构式如图所示。下列说法错误的是( )
A.Z与W形成的化合物熔点高
B.Y与Z能形成多种化合物
C.X的氢化物的沸点一定小于Z的氢化物
D.化合物![]() 中所有原子均满足8电子稳定结构
中所有原子均满足8电子稳定结构
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下图所示的转化关系,回答下列问题:

(1)写出反应①的离子方程式:______________________________________________;写出反应②的离子方程式:______________________。
(2)推出下列物质的化学式:E____________;I______________。
(3)在上述转化过程中,B、C、F、H的氧化能力由弱到强的顺序为______________________(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com