
科目: 来源: 题型:
【题目】肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:
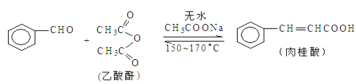 +CH3COOH
+CH3COOH
苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
溶解度(25℃,g/100g水) | 0.3 | 遇水易水解成乙酸 | 0.04 | 互溶 |
沸点(℃) | 179.6 | 138.6 | 300 | 118 |
相对分子质量 | 106 | 102 | 148 | 60 |
填空:
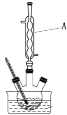
Ⅰ.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、3.6 g苯甲醛和4.2 g乙酸酐,振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
(1)仪器A的名称为________,其作用是__________。
(2)该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是(从平衡移动角度解释)_________。
(3)不能把无水CH3COONa换成CH3COONa·3H2O的原因是_________。
Ⅱ.粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:在搅拌下,向反应液中加入20 mL水
A.再慢慢加入碳酸钠溶液
B.然后进行水蒸气蒸馏(已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的)
C.待烧瓶内溶液冷却至室温,在搅拌下用加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有_______。水蒸气蒸馏除去的杂质是______。
(5)若得到的肉桂酸晶体产品不纯,应采用____方法可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸4.3 g,则该反应中的产率是____(保留小数点后一位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】非金属和金属单质以及相关化合物有着广泛的应用,回答下列相关问题:
(1)铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是______(填字母)。
a. 电子从基态跃迁到较高的激发态 b. 电子从较高的激发态跃迁到基态
c. 焰色反应的光谱属于吸收光谱 d. 焰色反应的光谱属于发射光谱
(2)In元素基态原子的价电子排布式为________。与Cu元素同周期,且基态原子有2个未成对电子的过渡元素是____(填元素符号)。
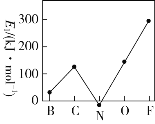
(3)第一电子亲和能(E1)是元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量。第二周期部分元素的E1变化趋势如图所示。试分析碳元素的E1较大的原因:______________。
(4)[PtCl4(NH3)2]中H-N-H键之间的夹角____(填“>”“<”或“=”)NH3分子中H-N-H键之间的夹角,原因是________________。
(5)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4。1个Fe(CO)5分子中含有σ键数目为____;已知Ni(CO)4分子为正四面体构型,下列溶剂能够溶解Ni(CO)4的是____(填字母)。
A. 四氯化碳 B.苯 C.水 D.液氨
(6)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和由3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为____。Fe3O4晶胞中有8个图示结构单元,晶体密度为5.18 g·cm-3,则该晶胞参数a=_____cm(写出计算表达式即可)。

查看答案和解析>>
科目: 来源: 题型:
【题目】某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示:

已知硝酸能将Fe2+氧化为Fe3+。回答下列问题:
(1) A可能是________________;
(2) B的化学式是______________,D的化学式是____________;
(3)滤液C中一定含有的阳离子Fe3+是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】航天员呼吸产生的CO2用下列反应处理,可实现其合理利用。反应Ⅰ:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
(1)己知H2(g)、CH4(g)的燃烧热分别为A kJ/mol、B kJ/mol, H2O(l)=H2O(g) △H =+C kJ/mol。计算反应Ⅰ的△H=_______kJ/mol。
(2)将原料气按n(CO2)∶n(H2)=1:4置于密闭容器中发生反应Ⅰ,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
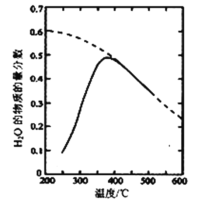
①温度过高或过低均不利于该反应的进行,原因是________。
②200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为____。(不必化简。用平衡分压代替平衡浓度计算)
(3)一种新的利用方案是Ⅱ:反应:CO2(g)+2H2(g)![]() C(s)+2H2O(g) △H
C(s)+2H2O(g) △H
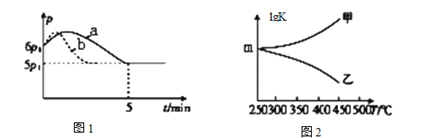
①向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol H2和0.04 mol CO2发生反应Ⅱ。若反应起始和平衡时温度相同(均为250℃),测得反应过程中压强(P)随时间(t)的变化如图1曲线a所示,则△H___ 0(填“>”“<”或“不确定”)
②若其它条件相同,仅改变某一条件时,测得其压强(P)随时间(t)的变化如图1曲线b所示,则改变的条件是_______。
③图2是甲、乙两同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是_______(填“甲”或“乙”),m值为______。
④反应Ⅱ必须在高温下才能启动,原因是______________。
(4)科学家还研究了处理CO2(g)另外的方法,利用下图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为______________。
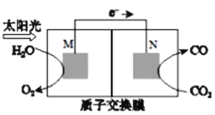
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A. c1∶c2=3∶1 B. 平衡时,Y和Z的生成速率之比为2∶3
C. X、Y的转化率不相等 D. c1的取值范围为0<c1<0.14 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】判断A(g)+B(g) ![]() C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )
A. 压强不随时间改变
B. 气体的密度不随时间改变
C. c(A)不随时间改变
D. 单位时间里生成C和D的物质的量相等
查看答案和解析>>
科目: 来源: 题型:
【题目】中国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂空气电池如下左图,电池的工作原理如下图。下列有关说法错误的是
(已知F=96500 C/mol)
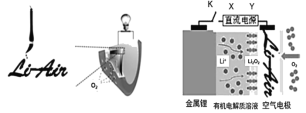
A.放电时,纸张中的纤维素作为电池的正极导电材料
B.充电时,若阳极放出1 mol O2,则有4 mol e-从X电极流出
C.放电时,理论上1 g负极材料能释放的电量约为13786 C
D.充电时,若用铅蓄电池作直流电源,则Y电极材料为PbO2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知2NO2(g) ![]() N2O4(g),在体积相同的A和B两个带活塞的玻璃容器中,如分别注入1/4容积颜色相同的NO2和Br2(气),然后将活塞同时向外拉到1/2处(快速),过一会儿可以看到
N2O4(g),在体积相同的A和B两个带活塞的玻璃容器中,如分别注入1/4容积颜色相同的NO2和Br2(气),然后将活塞同时向外拉到1/2处(快速),过一会儿可以看到
A.A中颜色比B中浅B.A中颜色比B中深
C.A、B中颜色深浅一样D.A、B中颜色都比开始时深
查看答案和解析>>
科目: 来源: 题型:
【题目】铝粉和氧化铁粉末的混合物制成的铝热剂可用于焊接钢轨。现取不同质量的该铝热剂分别和100ml同物质的量浓度的NaOH溶液反应,所取铝热剂的质量与产生气体的体积关系如下表(气体体积均在标准状况下测定):
① | ② | ③ | ④ | |
铝热剂质量/g | 5g | 10g | 15g | 20g |
气体体积/L | 2.24L | 4.48L | 6.72L | 6.72L |
试完成下列计算:
(1)NaOH溶液的物质的量浓度_______________。
(2)该铝热剂中铝的质量分数_____________
(3)20g该铝热剂发生铝热反应理论上产生铁的质量是多少?________(写出步骤)
查看答案和解析>>
科目: 来源: 题型:
【题目】对于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g) ΔH<0的化学反应下列叙述不正确的是
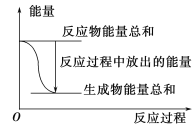
A. 反应过程中能量关系可用上图表示
B. ΔH的值与反应方程式的计量系数有关
C. 若将该反应设计成原电池,锌为负极
D. 若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com