
科目: 来源: 题型:
【题目】三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的是( )
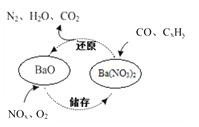
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1mol N2,转移电子数为1 mol
D.三效催化剂能有效实现汽车尾气中CO、CxHy、NOx三种成分的净化
查看答案和解析>>
科目: 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。如图是氟离子电池工作示意图,其中充电时F-从乙电极流向甲电极,下列关于该电池的说法正确的是( )
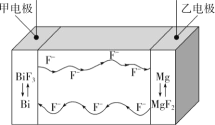
A.放电时,甲电极的电极反应式为Bi-3e-+3F-=BiF3
B.放电时,乙电极电势比甲电极高
C.充电时,导线上每通过1mole-,甲电极质量增加19g
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目: 来源: 题型:
【题目】在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.9molL-1,若不考虑反应过程中溶液体积的变化,则10s内生成硫酸铝的平均反应速率是( )
A.0.03molL-1min-1B.1.8molL-1min-1
C.1.2molL-1min-1D.0.18molL-1min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】工业是制取高铁酸钾(K2FeO4),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备Na2FeO4的主要反应为:2Fe(OH)3+3ClO﹣+4OH﹣=2FeO42﹣+3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是( )
A.湿法和干法制备中,生成1molNa2FeO4转移电子数目相同
B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小
C.干法制备的主要反应中Na2O2是氧化剂
D.K2FeO4处理水时,既能杀菌消毒,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色溶液中含有的阳离子为H+、Na+、Mg2+、Al3+、Ba2+中的一种或几种,向该溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此确定原溶液中一定含有的阳离子是
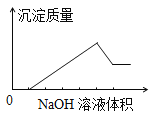
A. Mg2+、Al3+、Na+ B. H+、Mg2+、Al3+ C. H+、Ba2+、Al3+ D. Ba2+、Mg2+、Al3+
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量混合气体在密闭容器中发生如下反应![]() ;ΔH <0,达到平衡后测得A气体的浓度为0.5mol·L-1;当恒温下将密闭容器的容积扩大两倍并再次达到平衡时,测得A的浓度为0.3 mol·L-1。则下列叙述正确的是( )
;ΔH <0,达到平衡后测得A气体的浓度为0.5mol·L-1;当恒温下将密闭容器的容积扩大两倍并再次达到平衡时,测得A的浓度为0.3 mol·L-1。则下列叙述正确的是( )
A. 平衡向右移动 B. x+y>z C. B的转化率提高 D. C的体积分数增加
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:4NH3+5O2=4NO+6H2O,若反应速率分别用ν(NH3)、ν(O2)、ν(NO)、ν(H2O)[摩/(升分)]表示,则不正确的关系是( )
A.![]() ν(NH3)=ν(O2)B.
ν(NH3)=ν(O2)B.![]() ν(O2)=ν(H2O)
ν(O2)=ν(H2O)
C.![]() ν(NH3)=ν(H2O)D.
ν(NH3)=ν(H2O)D.![]() ν(O2)=ν(NO)
ν(O2)=ν(NO)
查看答案和解析>>
科目: 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如下所示。
达到平衡,正反应速率随时间变化的示意图如下所示。
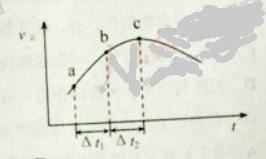
A. 反应在c 点达到平衡状态
B. 反应物浓度:![]() 点小于
点小于![]() 点
点
C. 反应物的总能量低于生成物的总能量
D. ![]() 时,SO2的转化率:
时,SO2的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目: 来源: 题型:
【题目】在硫酸铝、硫酸钾和明矾的混合溶液中,硫酸根离子的浓度为0.4mol·L-1,当加入等体积0.4mol·L-1氢氧化钾溶液时,生成的沉淀恰好完全溶解。则反应后溶液中钾离子的浓度约为( )
A.0.225mol·L-1B.0.25mol·L-1C.0.45mol·L-1D.0.9mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知水的电离方程式是H2O![]() H++ OH-。下列叙述正确的是( )
H++ OH-。下列叙述正确的是( )
A.升高温度,KW增大,pH不变
B.向水中加入少量硫酸,c(H+)增大,KW不变
C.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低
D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com