
科目: 来源: 题型:
【题目】甲醇来源丰富,有广泛的用途和广阔的应用前景,工业上可以利用CO和CO2生产甲醇,同时可以利用甲醇生产丙烯。制备甲醇,丙烯过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.0kJ/mol
CH3OH(g) △H3=-90.0kJ/mol
反应Ⅳ:3CH3OH(g)![]() C3H6(g)+3H2O(g) △H4=-31.0kJ/mol
C3H6(g)+3H2O(g) △H4=-31.0kJ/mol
回答下列问题:
(1)反应Ⅱ的ΔH2=________。
(2)反应Ⅲ能够自发进行的条件是________(填“较低温度”“较高温度”或“任何温度”),据研究该反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于保持催化剂Cu2O的量不变,原因是________(用化学方程式表示)。
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是________。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2的生成速率与CH3OH的生成速率相等
D.容器的压强不再变化
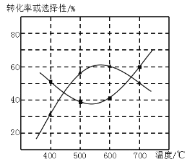
(4)甲醇生产丙烯的同时,还生成乙烯。在某催化剂作用下,2L密闭容器中加入0.5mol甲醇,经过相同时间后测得甲醇转化率及丙烯的选择性(生成丙烯的甲醇与甲醇转化量的比值)与反应温度之间的关系如图所示。计算600℃时反应甲醇生产丙烯的反应Ⅳ平衡常数________。若将容器体积压缩为1L,其他条件不变,在如图中作出甲醇平衡转化率随温度的变化曲线。________。
(5)研究表明,甲醇可由CO2在强酸性水溶液中通过电解合成,则生成甲醇的反应电极反应式:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】有的油田开采的石油中溶有一种碳氢化合物—金刚烷。金刚烷 是一种环状烃,它的结构高度对称。下图表示金刚烷,图中数字是碳原子编号。碳原子用小黑点表示,氢原子均省略,一条短线表示共用一对电子。
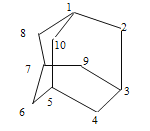
(1)编号1的碳原子上的一个氢原子被氨基(-NH2)取代后,再与盐酸反应生成盐酸盐(1—氨基金刚烷盐酸盐)是一种防治感冒的药物。推断它的化学式是__________。
(2)金刚烷是由 _____ 个六元环构成的笼形结构,其中有 _____ 个碳原子被三个环共有。
查看答案和解析>>
科目: 来源: 题型:
【题目】PT(KHC2O4·H2C2O4·2H2O,名称:四草酸钾)是一种分析试剂。室温时,H2C2O4的pKa1、pKa2分别为1.23、4.19(pKa=-lgKa)。下列说法不正确的是( )
A.0.1mol·L-1PT溶液中:c(HC2O![]() )>c(K+)>c(H2C2O4)
)>c(K+)>c(H2C2O4)
B.0.1mol·L-1PT中滴加NaOH至溶液pH=4.19:c(C2O![]() )=c(HC2O
)=c(HC2O![]() )
)
C.0.1mol·L-1PT中滴加NaOH至溶液呈中性:c(K+)>c(Na+)>c(HC2O![]() )>c(C2O
)>c(C2O![]() )
)
D.0.1mol·L-1PT与0.1mol·L-1KOH溶液等体积混合,溶液中水的电离程度比纯水的大
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上除去电石渣浆(含CaO)上清液中的S2-,并制取石膏(CaSO42H2O)的常用流程如图:
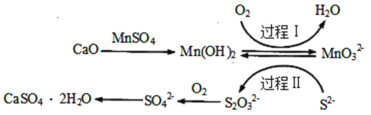
下列说法不正确的是( )
A.过程Ⅰ、Ⅱ中起催化剂作用的物质是Mn(OH)2
B.常温下,56gCaO溶于水配成1L溶液,溶液中Ca2+的数目为6.02×1023个
C.将10L上清液中的S2-转化为SO![]() (S2-浓度为320mg·L-1),理论上共需要0.2mol的O2
(S2-浓度为320mg·L-1),理论上共需要0.2mol的O2
D.过程Ⅱ中,反应的离子方程式为4MnO![]() +2S2-+9H2O=S2O
+2S2-+9H2O=S2O![]() +4Mn(OH)2↓+10OH-
+4Mn(OH)2↓+10OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】有机反应中,加氧或去氢的反应称之为氧化反应,反之则称为还原反应,下列反应中属于还原反应的是
A.CH3CHO ![]() CH3CH3OHB.CH3COOH
CH3CH3OHB.CH3COOH ![]() CH3COOC2H5
CH3COOC2H5
C.![]()
![]()
![]() D.
D.![]()
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究无机盐X(仅含三种元素,摩尔质量为270g·mol-1)的组成和性质,某学习小组进行了如下实验,其中气体单质A能使带火星的木条复燃。
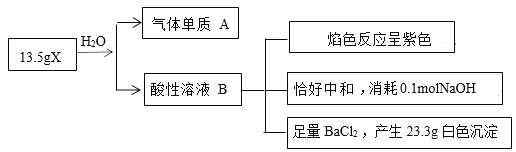
(1)X的组成元素为O和______(用元素符号表示)。
(2)写出X与水反应的化学反应方程式__________。
(3)X氧化能力极强,且对环境友好,可用于脱硫、脱硝。在碱性条件下,X氧化SO32-的离子方程式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中国科学院深圳研究院成功研发出一种基于二硫化钼/碳纳米复合材料的钠型双离子电池,可充放电。其放电时工作原理如图所示。下列说法不正确的是( )

A.二硫化钼/碳纳米复合材料为该电池的负极材料
B.放电时正极的反应式为Cn(PF6)x+xe-═xPF6-+Cn
C.充电时阴极的电极反应式为MoS2-C+xNa++xe-=NaxMoS2-C
D.充电时石墨端铝箔连接外接电源的负极
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,100mL0.1mol·L-1的H2A溶液中滴加0.1mol·L-1NaOH溶液,含A元素相关微粒物质的量随pH的变化如图所示。下列说法正确的是( )
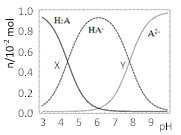
A.将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性
B.X点所加NaOH溶液体积为50mL
C.X点溶液中含A元素的相关离子存在以下关系:c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1
D.Y点溶液中存在以下关系:c(H+)+c(Na+)=c(OH-)+3c(HA-)
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,向20.00 mL 0.1000 mol·L1盐酸中滴加0.1000 mol·L1 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图,已知lg3=0.5。下列说法不正确的是
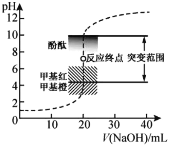
A.选择变色范围在pH突变范围内的指示剂,可减小实验误差
B.用移液管量取20.00 mL 0.1000 mol·L1盐酸时,移液管水洗后需用待取液润洗
C.NaOH标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定NaOH溶液的浓度,标定时采用甲基橙为指示剂
D.V(NaOH)=10.00 mL 时,pH约为1.5
查看答案和解析>>
科目: 来源: 题型:
【题目】全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置(如图)。

已知:
①溶液呈酸性且阴离子为SO42-;
②溶液中颜色:V3+绿色,V2+紫色,VO2+黄色,VO2+蓝色;
③放电过程中,右槽溶液的颜色由紫色变成绿色。
下列说法不正确的是
A.放电时B极为负极
B.放电时若转移的电子数为3.01×1023个,则左槽中H+增加0.5 mol
C.充电过程中左槽的电极反应式为:VO2++H2O-e- =VO2++2H+
D.充电过程中H+通过质子交换膜向右槽移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com