
【题目】工业上除去电石渣浆(含CaO)上清液中的S2-,并制取石膏(CaSO42H2O)的常用流程如图:
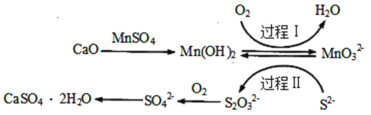
下列说法不正确的是( )
A.过程Ⅰ、Ⅱ中起催化剂作用的物质是Mn(OH)2
B.常温下,56gCaO溶于水配成1L溶液,溶液中Ca2+的数目为6.02×1023个
C.将10L上清液中的S2-转化为SO![]() (S2-浓度为320mg·L-1),理论上共需要0.2mol的O2
(S2-浓度为320mg·L-1),理论上共需要0.2mol的O2
D.过程Ⅱ中,反应的离子方程式为4MnO![]() +2S2-+9H2O=S2O
+2S2-+9H2O=S2O![]() +4Mn(OH)2↓+10OH-
+4Mn(OH)2↓+10OH-
【答案】B
【解析】
A. 催化剂在反应中参加又生成,由图可知,过程Ⅰ、Ⅱ中,起催化剂作用的物质是Mn(OH) 2,故A正确;
B. 56g CaO(1mol)溶于水,与水反应产生1mol氢氧化钙,但氢氧化钙微溶于水,部分会形成沉淀,因此溶液中的钙离子数目小于6.02×1023个,故B错误;
C. 由电子守恒及原子守恒可知,存在2S2-~![]() ~4Mn(OH)2~8e -~2O2,且两个过程消耗氧气,将10L上清液中的S2-转化为
~4Mn(OH)2~8e -~2O2,且两个过程消耗氧气,将10L上清液中的S2-转化为![]() (S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为
(S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为![]() ,故C正确;
,故C正确;
D. 过程Ⅱ中S2-与![]() 发生氧化还原反应,离子反应为4MnO
发生氧化还原反应,离子反应为4MnO![]() +2S2-+9H2O=S2O
+2S2-+9H2O=S2O![]() +4Mn(OH)2↓+10OH-,故D正确;
+4Mn(OH)2↓+10OH-,故D正确;
故选:B。


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1)CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4)∶n(H2O)=__________。当反应达到平衡时,若增大压强,则n(C2H4)___________(填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
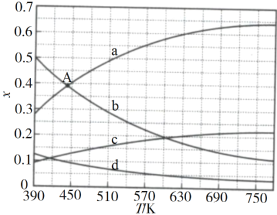
图中,表示C2H4、CO2变化的曲线分别是______、______。CO2催化加氢合成C2H4反应的ΔH______0(填“大于”或“小于”)。
(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数Kp=_________(MPa)3(列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将相同质量的铜分别与过量浓硝酸、稀硝酸反应,下列叙述正确的是( )
A.生成气泡快慢:两者相同
B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图Ⅰ是NO2(g)+CO(g) ![]() CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ所示。
CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ所示。

下列有关说法正确的是
A. 一定条件下,向密闭容器中加入1 mol NO2(g)与1 mol CO(g)反应放出234 kJ热量
B. 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C. 若X表示温度,则Y表示的可能是CO2的物质的量浓度
D. 若X表示反应时间,则Y表示的可能是混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向20.00 mL 0.1000 mol·L1盐酸中滴加0.1000 mol·L1 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图,已知lg3=0.5。下列说法不正确的是
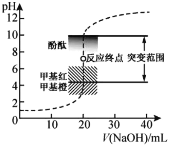
A.选择变色范围在pH突变范围内的指示剂,可减小实验误差
B.用移液管量取20.00 mL 0.1000 mol·L1盐酸时,移液管水洗后需用待取液润洗
C.NaOH标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定NaOH溶液的浓度,标定时采用甲基橙为指示剂
D.V(NaOH)=10.00 mL 时,pH约为1.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸的结构简式是:CH2![]() CHCOOH。试写出它与下列物质反应的方程式。
CHCOOH。试写出它与下列物质反应的方程式。
(1)氢氧化钠溶液________________________________________。
(2)溴水________________________________________。
(3)乙醇________________________________________。
(4)氢气________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取0.68g某一元羧酸甲酯和40mL0.2molL-1的氢氧化钠溶液混合加热,使之完全水解。再用0.2molL-1 的盐酸中和剩余的烧碱,消耗盐酸15mL 。已知27.2mg该甲酯完全燃烧可得70.4mgCO2 和14.4mgH2O .求:
(1)该甲酯的最简式_______;
(2)该甲酯的相对分子质量_______;
(3)该甲酯的化学式、结构简式和名称_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将224L氯化氢气体溶于635mL的水(密度为1 g/cm-3)中,所得盐酸的密度为1.18g/cm3。
(1)该盐酸的质量分数是_________
(2)取这种盐酸10mL,稀释到1.45L,所得的稀盐酸的物质的量浓度________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.摩尔是物质的量的单位,1mol任何物质都含有6.02×1023个分子
B.钠元素和氯元素在自然界存在的形态既有游离态又有化合态
C.气体的体积主要由气体物质的量的多少和气体分子间的平均距离决定的
D.若1克水中含有m个氢原子,则阿伏加德罗常数用含m的代数式可表示为18m
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com