
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
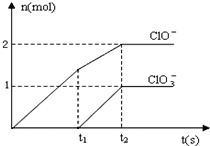 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.| n(ClO-) | n(ClO3-) |
查看答案和解析>>
科目: 来源: 题型:阅读理解

| 仪器 | 加入试剂 | 预期实验现象 |
| A | 绿矾试样 | 残留红棕色固体 残留红棕色固体 |
| B | 无水硫酸铜 无水硫酸铜 |
白色粉末变蓝 白色粉末变蓝 |
| D | 品红或酸性高锰酸钾溶液或溴水 品红或酸性高锰酸钾溶液或溴水 |
溶液褪色 溶液褪色 |
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com