
科目: 来源: 题型:
【题目】废塑料的回收再生利用将工业垃圾变成极有价值的工业生产原料。具有不可忽略的潜在意义。利用如图所示的装置隔绝空气加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,以此探究废塑料的再利用。下列叙述正确的是

A. 聚丙烯的链节是-CH2-CH2-CH2-
B. 装置乙的试管中收集到的物质不能使酸性高锰酸钾溶液褪色
C. 装置丙中的试剂可吸收烯烃且出现溶液分层现象
D. 最后收集的气体可作燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)写出符合下列条件的原子的元素符号并画出其原子结构示意图。
①核外有2个电子层、10个电子的原子__________________;
②质量数为23、中子数为12的原子__________________;
③电子总数是最外层电子数3倍的原子__________________。
(2)用下列原子或离子的结构示意图的编号(A、B、C、D)填空:
A.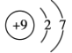 B.
B.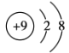 C.
C.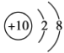 D.
D.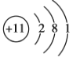
①电子层排布相同的是__________________;
②属于同一种元素的是__________________;
③属于金属元素的是__________________;
④属于稀有气体元素的是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】温室气体CO2资源化利用的一种途径如下,生成物H和I可用作锂离子电池的电解质。
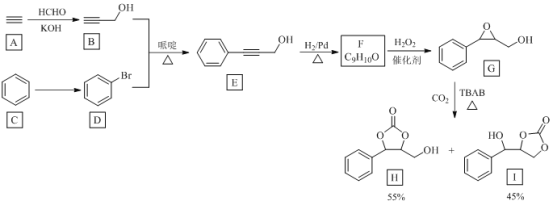
回答下列问题:
(1)由A到B的反应类型为________。
(2)由C到D反应所需试剂为________。
(3)E中官能团的名称是________。
(4)F合成G的反应方程式为________。
(5)H的分子式为________。
(6)写出与G互为同分异构体的羧酸类芳香化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为6:2:1:1)________。
(7)设计由丙炔和甲醛为起始原料制备 和
和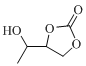 的合成路线 ____(无机试剂任选)。
的合成路线 ____(无机试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeSe 、MgB2等超导材料具有广阔的应用前景。
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为________,基态Se原子的电子占据最高能级的电子云轮廓图为________形。
(2)向FeSe中嵌入吡啶(![]() )能得到具有优异性能的超导材料。吡啶中氮原子的杂化类型为________;该分子内存在________(填标号)。
)能得到具有优异性能的超导材料。吡啶中氮原子的杂化类型为________;该分子内存在________(填标号)。
A.σ键 B.π键 C.配位键 D.氢键
(3)将金属锂直接溶于液氨,得到具有很高反应活性的金属电子溶液,再通过系列反应可制得FeSe基超导材料Li0.6(NH2)0.2(NH3)0.8Fe2Se2。
①NH2-的空间构型为________。
②液氨是氨气液化的产物,氨气易液化的原因是________。
③金属锂溶于液氨时发生反应:Li + (m+n)NH3=X+e-(NH3)n。X的化学式为________。
(4)MgB2晶体结构如图所示。B原子独立为一层,具有类似于石墨的结构,每个B原子周围都有________个与之等距离且最近的B原子;六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA ,该晶体的密度为________ g·cm-3(列出计算式)。

查看答案和解析>>
科目: 来源: 题型:
【题目】氧化亚氮(N2O)是一种强温室气体,且易转换成颗粒污染物。研究氧化亚氮分解对环境保护有重要意义。
(1)污水生物脱氮过程中,在异养微生物催化下,硝酸铵可分解为N2O和另一种产物,该反应的化学方程式为___。
(2)已知反应2N2O(g)=2N2(g)+O2(g)的△H=-163kJ/mol,1molN2(g),1molO2(g)分子中化学键断裂时分别需要吸收945kJ,498kJ的能量,则1molN2O(g)分子中化学键断裂时需要吸收的能量为___kJ。
(3)在一定温度下的恒容容器中,反应2N2O(g)=2N2(g)+O2(g)的部分实验数据如下:
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
c(N2O)/molL-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.010 |
①在0~20min时段,反应速率v(N2O)为___molL-1min1。
②若N2O起始浓度c0为0.150 molL-1,则反应至30min时N2O的转化率α=___。比较不同起始浓度时N2O的分解速率:v(c0=0.150molL-1)___v(c0=0.001molL-1)(填“>”、“=”或“<”)。
③不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1____T2(填“>”、“=”或“<”)。当温度为T1、起始压强为p0,反应至t1min时,体系压强p=___(用p0表示)。
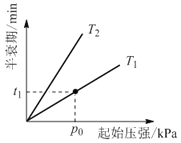
(4)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步 I2(g) ![]() 2I(g) (快反应)
2I(g) (快反应)
第二步 I(g)+N2O(g)→N2(g)+IO(g) (慢反应)
第三步 IO(g)+N2O(g)→N2(g)+O2(g)+I(g) (快反应)
实验表明,含碘时N2O分解速率方程v=kc(N2O)[c(I2)]0.5(k为速率常数)。下列表述正确的是___(填标号)。
A.N2O分解反应中,k(含碘)>k(无碘)
B.第一步对总反应速率起决定作用
C.第二步活化能比第三步大
D.I2浓度与N2O分解速率无关
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。下列说法错误的是
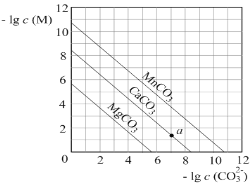
A. Ksp(MnCO3)的数量级为10-11
B. MgCO3的悬浊液中加入少量水充分振荡,c(Mg2+)不变
C. a点表示的溶液中,c(Ca2+)>c(CO32-)
D. 向浓度均为0.01mol·L-1的Mg2+、Ca2+、Mn2+混合溶液中逐滴加入Na2CO3溶液,最先形成MgCO3沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的示意图如下。
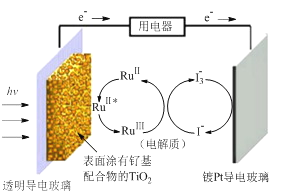
电池工作时发生的反应为:
RuII ![]() RuII *(激发态)
RuII *(激发态)
RuII *→RuIII+e-
I3-+ 2e-→3I-
RuIII+3I-→RuII++ I3-
下列关于该电池叙述错误的是 ( )
A. 电池中镀Pt导电玻璃为正极
B. 电池工作时,I-离子在镀Pt导电玻璃电极上放电
C. 电池工作时,电解质中I-和I3-浓度不会减少
D. 电池工作时,是将太阳能转化为电能
查看答案和解析>>
科目: 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法中正确的是
A. 4g甲烷完全燃烧转移的电子数为2NA
B. 11.2L(标准状况)CCl4中含有的共价键数为2NA
C. 3 mol SO2和1mol O2于密闭容器中催化反应后分子总数为3NA
D. 1L 0.1mol·L-1的Na2S溶液中HS-和S2-离子数之和为0.1 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷(![]() )是其中的一种。下列关于该化合物的说法正确的是
)是其中的一种。下列关于该化合物的说法正确的是
A. 与甲苯(C7H8)互为同分异构体
B. 1mol该化合物完全燃烧时消耗10 mol O2
C. 所有碳原子均处同一平面
D. 一氯代物共有3种(不含立体异构)
查看答案和解析>>
科目: 来源: 题型:
【题目】美宇航局(NASA)提醒人类:环保、素食、节能将有效抑制温室效应;否则两极冰山融化,将引发一系列灾难。美国宇航局(NASA)科研人员发现了一种比二氧化碳高104倍的“超级温室气体”全氟丙烷(C3F8),提醒人们慎用含氟物。有关全氟丙烷的说法正确的是
A. 分子中的三个碳原子可能处于同一直线上
B. 全氟丙烷的电子式为: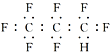
C. 由丙烷转化为全氟丙烷的反应为取代反应
D. 全氟丙烷可由全氟丙烯(CF2=CFCF3)与H2加成得到
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com