
科目: 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①盐卤(含MgCl2)![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液
MgCl2溶液![]() 无水MgCl2
无水MgCl2
②铝土矿![]() AlO2-
AlO2-![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3
③NH3![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
④NaCl溶液![]() Cl2
Cl2![]() 无水FeCl2
无水FeCl2
⑤S![]() SO3
SO3![]() H2SO4
H2SO4
⑥SiO2![]() Na2SiO3溶液
Na2SiO3溶液![]() H2SiO3
H2SiO3
A. ③⑥B. ③⑤⑥C. ①④⑤D. ①③⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对一种废旧合金(含有Cu、Fe、Si等元素)进行分离、回收再利用,所设计工艺流程如图。
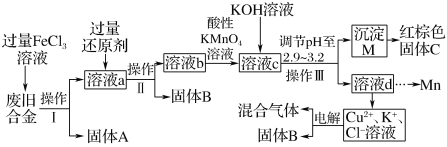
已知:298K时,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Mn(OH)2]=1.9×10-13
回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ为__,固体B为__(填化学式)。
(2)加入过量FeCl3溶液过程中与较不活泼的金属反应的离子方程式__。
(3)调节pH至2.9~3.2的目的是分离__(填离子符号)
(4)①向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为__。
②若用amol/LKMnO4溶液处理溶液b,当恰好反应时消耗KMnO4溶液VmL,所得红棕色固体C的物质的量为__(用含a、V的代数式表示)
(5)用惰性电极电解时阳极产生标准状况下的气体6.72L,阴极得到的电子数为0.8NA,则生成氧气的物质的量为__mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。查阅资料知SO3的熔点为16.83℃,沸点是44.8℃。某化学学习小组欲通过实验测定上述反应中SO2的转化率,他们设计了如下实验。
2SO3(g) ΔH<0。查阅资料知SO3的熔点为16.83℃,沸点是44.8℃。某化学学习小组欲通过实验测定上述反应中SO2的转化率,他们设计了如下实验。

请根据要求回答问题:
(1)各装置接口的连接顺序是a→__。
(2)装置Ⅳ烧杯中盛放冰水的作用是__。
(3)装置Ⅰ所用硫酸,一般选用浓度为70%~80%的硫酸,原因是__。
(4)当装置Ⅰ中反应结束时,要打开止水夹继续通入O2一段时间,继续通入O2的目的是__。
(5)称量agNa2SO3粉末与足量硫酸反应,实验结束后称得装置Ⅳ增重bg,列式表示该实验中SO2的转化率__。
查看答案和解析>>
科目: 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是 ( )

A. 按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B. 图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C. 铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D. 图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,关于pH=11的NH3·H2O溶液,下列分析正确的是
A. c(NH3·H2O)=10-3mol/L
B. 由水电离出的c(H+)=10-11 mol/L
C. 加入少量 NH4Cl固体,NH3·H2O的电离平衡逆向移动,KW值减小
D. 加入等体积 pH=3的盐酸,所得溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】沉积物微生物燃料电池可处理含硫废水,其工作原理如图所示。下列说法错误的是( )
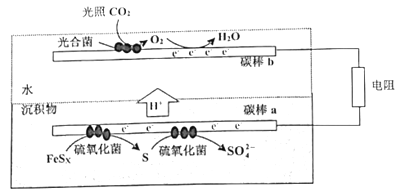
A. 碳棒b的电极反应式为:O2+4e-+4H+=2H2O
B. 光照强度对电池的输出功率有影响
C. 外电路的电流方向:碳棒a→碳棒b
D. 酸性增强不利于菌落存活,故工作一段时间后,电池效率降低
查看答案和解析>>
科目: 来源: 题型:
【题目】下列正确的叙述有
① CO2、SO2、P2O5均为酸性氧化物
②Ca(HCO3)2 、Fe(OH)3、FeCl2均可由化合反应制得
③ 碘晶体分散到酒精中、淀粉溶于水中所形成的分散系分别为:溶液、胶体
④ 灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4Cl的反应均属于氧化还原反应,又是吸热反应
⑤ 需要通电才可进行的有:电离、电解、电泳、电镀、电化学腐蚀
⑥ 氯化铁溶液与氢氧化铁胶体具有的共同性质是:能透过滤纸,加热蒸干、灼烧后都有氧化铁生成
⑦ 按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、盐酸、苛性钾、次氯酸、氨气
⑧ 金属元素和非金属元素形成的化合物不一定是离子化合物
A. 3个B. 4个C. 5个D. 6个
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:Ag2SO4微溶于水,可溶于硝酸。溶液X中可能含有Na+、Ca2+、Fe2+、Cl—、Br—、CO32-、SiO32-、SO42-中的几种离子。为了确定其组成,某同学进行了如下实验:

下列说法正确的是
A.溶液X中一定不含Ca2+、Br—、Fe2+
B.溶液X中一定含有Na+、Cl—和SiO32-
C.为确定溶液X中是否含有SO42-,可取溶液2,加入BaCl2溶液
D.白色沉淀为AgCl和Ag2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】下刎有关实验装置、操作,不能实现相应实验目的的是

A. 装置甲可用酸性KMnO4溶液滴定FeSO4溶液
B. 用装置乙进行实验时若逐滴滴加AgNO3溶液先出现黄色沉淀,可说明 Ksp(AgCl)>Ksp(AgI)
C. 装置丙可用于收集氢气
D. 装置丁可用于 NaOH溶液除去溴苯中单质溴
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质间可能包括多步反应,其总的离子方程式正确的是 ( )
A. 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O===HClO+HSO3-
B. 向FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
C. 向 AlCl3溶液中投入过量Na:Al3++4Na+2H2O===AlO2-+4Na++2H2↑
D. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42- 沉淀完全:2Al3++3SO![]() +3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com