
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A.  由图可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1
由图可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1
B.  表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+
表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+
C.  温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足c(H+)>c(OH-)
温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足c(H+)>c(OH-)
D.  表示反应N2(g)+3H2(g)=2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
表示反应N2(g)+3H2(g)=2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 号中的某元素形成的微粒的结构示意图可表示为
号中的某元素形成的微粒的结构示意图可表示为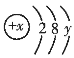 ,其中
,其中![]() 。
。
(1)![]() 表示______,
表示______,![]() 表示______。
表示______。
(2)若该微粒是原子,则![]() 和
和![]() 的数量关系为______。
的数量关系为______。
(3)若该微粒是阳离子,则![]() 和
和![]() 的数量关系为______,该微粒可以是______(写出一种离子符号)。
的数量关系为______,该微粒可以是______(写出一种离子符号)。
(4)若该微粒是阴离子,则![]() 和
和![]() 的数量关系为______,该微粒可以是______(写出一种离子符号)。
的数量关系为______,该微粒可以是______(写出一种离子符号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】废旧光盘金属层中含有金属Ag(其他金属微量忽略不计),从光盘中提取金属Ag的工艺流程如下。请回答下列问题:
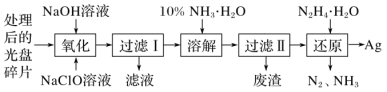
(1)“氧化”阶段需在80℃条件下进行,使用的加热方式为_________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为________。有人提出用HNO3代替NaClO氧化Ag,从反应产物的角度分析,其缺点是_________。
(3)“过滤Ⅰ”中洗涤难溶物的实验操作为__________。
(4)常用10%的氨水溶解AgCl固体,AgCl与NH3·H2O按1∶2反应可生成Cl-和一种阳离子______(填离子符号)的溶液。实际反应中,即使氨水过量,“废渣”中也含有少量AgCl固体,可能的原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)
已知:I.反应A中,4molHCl被氧化,放出115.6kJ热量。
II.
判断下列说法正确的是( )
A. 反应A的△H>-115.6kJ·mol-1
B. H2O中H—O键比HCl中H—Cl键弱
C. 由II中的数据判断氯元素的非金属性比氧元素强
D. 断开1molH—O键与断开1molH—Cl键所需能量相差31.9kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】对于核电荷数为![]() 的元素,下列有关元素性质与原子结构的理解正确的是( )
的元素,下列有关元素性质与原子结构的理解正确的是( )
A.原子最外层电子数小于4的元素一定是金属元素
B.原子最外层电子数大于4的元素一定是非金属元素
C.原子最外层电子数与该元素的常见化合价的绝对值一定相等
D.原子最外层电子数与其电子层数相等的元素一定是金属元素
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为氢氧燃烧电池原理示意图,按照此图的提示,下列叙述正确的是( )

A. a电极是正极
B. b电极的电极反应为:4OH-- 4e-=2H2O + O2↑
C. 电子从a电极经由电解液传递到b电极
D. 氢氧燃烧电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目: 来源: 题型:
【题目】某元素R的原子核外电子数等于核内中子数,2.8 g该元素(设其相对原子质量与R原子的质量数相等)的单质R与氧气充分反应,可得到6.0 g化合物RO2,则下列有关说法错误的是( )
A.该元素原子的质子数为13
B.该元素原子的中子数为14
C.该元素原子的最外层电子数为4
D.该元素原子具有3个电子层
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关原子核外电子及其运动状态的描述正确的是( )
①可以测定某一时刻电子所处的位置
②电子质量很小且带负电荷
③相比原子核的大小,电子运动的空间范围很大
④高速运动
⑤有固定的运动轨道
⑥电子的质量约为氢离子质量的![]()
A.①②③B.②③④⑥
C.③④⑤⑥D.⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60 mol H2(g),2min在某温度下达到平衡,此时NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。请计算(写出计算过程):
2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60 mol H2(g),2min在某温度下达到平衡,此时NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。请计算(写出计算过程):
(1)2min内N2的平均速率;
(2)该条件下此反应的平衡常数K。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲是短周期元素中原子半径最小的元素,乙的气态氢化物的水溶液显碱性,丙是短周期元素中原子半径最大的元素,丁是地壳中含量最多的金属元素。
(1)写出四种元素的名称:甲______,乙______,丙______,丁______。
(2)乙、丙、丁三种元素的原子半径从大到小的顺序是________(填元素符号,下同)![]() ________
________![]() ________。
________。
(3)写出乙、丙、丁的最高价氧化物对应的水化物相互反应的化学方程式:__________________、__________________、__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com