
科目: 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大,X阴离子的电子数与Y原子的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的两种元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的元素名称为___________;五种元素的原子半径从小到大的顺序是(用元素符号表示)______________。
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,用电子式表示A的形成过程_______________,B的结构式为________。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为________。
(4)一定条件下,M与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
A | ||||||
B | C[ | D | ||||
E | F | G | H | |||
请回答下列问题:
(1)写出E元素在周期表中的位置 。
(2)B与D可形成三原子分子X,X的电子式为 。
(3)E、F、H所形成的简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)G的最高价氧化物与B的单质在高温下能发生置换反应,其化学反应方程式为:
。
(5)由A、C、D三种元素组成的强电解质Z溶于水时能促进水的电离,测得Z的水溶液pH<7,其原因是 (用离子方程式来表示)。
(6)盐Y由B、D、E组成。以熔融盐Y为电解质构成的燃料电池如图所示。
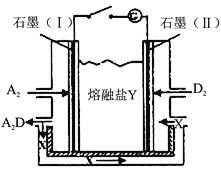
写出石墨(I)电极上发生的电极反应式 。
(7)用熔融盐Y的燃料电池作电源,以石墨为电极,电解一定浓度的CuSO4溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在AlCl3溶液中滴加过量的氨水,反应的化学方程式为__________________。
(2)碳酸氢钠与稀硫酸反应的离子方程式__________________;铜与浓硫酸共热反应的化学方程式__________________。
(3)现有0.284kg质量分数为10%的Na2SO4溶液,则溶液中Na2SO4的物质的量为______;配制250mL2.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液的体积_________mL。
(4)同一主族元素性质具有一定的相似性和递变性;同一主族,从上到下:原子的电子层数逐渐____________,原子半径逐渐____________;失电子能力逐渐____________,金属性逐渐____________ ;得电子能力逐渐 ___________,非金属性逐渐____________ 。
(5)A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1。回答下列问题:
写出E元素的元素符号:________画出B、C的原子结构示意图:B.________C________画出D的离子结构示意图:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚砷酸(H3AsO3)可用于治疗白血病,在溶液中存在多种微粒形态。向1L0.1mol·L-1H3AsO3溶液中逐滴加入0.1mol·L-1KOH溶液,各种微粒物质的量分数与溶液的pH关系如图所示,图中M点对应的pH为a,下列说法正确的是( )
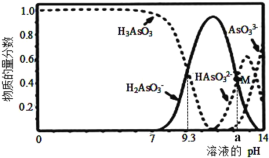
A.H3AsO3的电离常数Ka1的数量级为10-9
B.pH在8.0~10.0时,反应的离子方程式:H3AsO3+OH-=H2AsO3-+H2O
C.M点对应的溶液中:c(H2AsO3-)+c(HAsO32-)+c(AsO33-)+c(H3AsO3)=0.1mol·L-1
D.pH=12 时,溶液中:c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(H3AsO3)>c(H+)+c(K+)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。
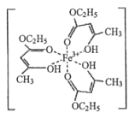
①此配合物中,基态铁离子的价电子排布式为________________。
②此配合物中碳原子的杂化轨道类型有________________。
③此配离子中含有的化学键有____________(填字母)。
A. 离子键 B. 金属键 C. 极性键 D. 非极性键 E. 配位键 F. 氢键 G.σ键 H. π键
④氯化铁在常温下是固体,熔点为 306℃,沸点为 315℃,在 300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断氯化铁的晶体类型为_________。
(2)基态 A 原子的价电子排布式为 3s23p5,铜与A 形成化合物的晶胞如图所示(黑球代表铜原子)。
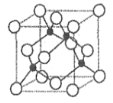
①该化合物的化学式为____________,A原子的配位数是______________。
②已知该化合物晶体的密度为ρg·cm-3,阿伏加德罗常数的值为 NA,则该晶体中 Cu 原子和A 原子之间的最短距离为________pm(列出计算表达式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ. 砷化镓为第三代半导体,以其为材料制造的灯泡寿命长.耗能少。已知砷化镓的晶胞结构如图所示。请回答下列问题:
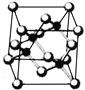
(1)下列说法正确的是__________(填序号)
A.砷化镓晶胞结构与NaCl相同 B.第一电离能 As>Ga
C.电负性 As>Ga D.原子半径 As>Ga
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为_____________________________;
(3)AsH3空间形状为___________;已知(CH3)3 Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ. 金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因_______________________, Cu2+的核外电子排布式为_______________________。
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有_________和_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中 Fe2+和 Fe3+的浓度恰好相等。则已反应的 Fe3+和未反应的 Fe3+的物质的量之比为:
A.4:3B.3:2C.2:3D.1:4
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求填空:
(1)A+和B-的电子层结构都与氩相同,A+的结构示意图为___;
(2)碳原子核外有___种能量不同的电子,分布在___个轨道中;
(3)鉴别碳原子可以利用其激发态原子跃迁到基态所形成的特征___(吸收或发射)光谱;
(4)水、SiO2、硫三种物质沸点由大到小的顺序为___;
(5)下列变化:H-(g)=H(g) +e-吸收的能量为73kJ·mol-1,H(g)=H+(g)+e-吸收的能量为1311kJ·mol-1,则氢负离子H-的第一电离能为___;
(6)短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。四种原子半径的由大到小顺序___(元素符号表示),能证明W、Z两元素非金属性强弱的离子方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】环丙叉环丙烷(A)的结构特殊,根据如下转化判断下列说法正确的是( )
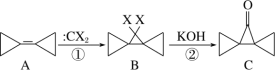
A.反应①、②分别是加成反应和消去反应
B.有机物A 的二氯代物有 4 种(不考虑立体异构)
C.有机物 B 的所有原子都在一个平面内
D.有机物C 的同分异构体中,同时含有苯环和羟基的有 5 种
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是
A. 往Na2SiO3溶液中加入盐酸:2Na++ SiO32- +2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
B. 氯气与烧碱溶液反应:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
C. 稀硫酸滴在铁片上:Fe+6H+![]() 2Fe3++3H2↑
2Fe3++3H2↑
D. 铜片插入硝酸银溶液中:Cu+Ag+![]() Cu2++Ag
Cu2++Ag
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com