
科目: 来源: 题型:
【题目】科学家最近在-100 ℃的低温下合成了一种烃 X,该分子的球棍模型如图所示,下列说法中不正确的是( )
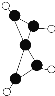
A.该分子的分子式为 C5H4B.该分子中每个碳原子均形成 4 个 化学键
C.该分子在一定条件下可与 H2 发生反应D.该分子中只有 C—C 键,没有![]() 键
键
查看答案和解析>>
科目: 来源: 题型:
【题目】葛根大豆苷元![]() 用于治疗高血压引起的头疼、突发性耳聋等症,其合成路线如下:
用于治疗高血压引起的头疼、突发性耳聋等症,其合成路线如下:
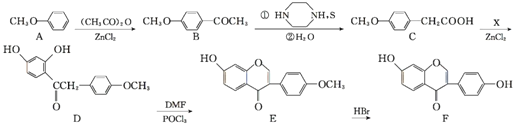
![]() 化合物B中的含氧官能团有 ______
化合物B中的含氧官能团有 ______ ![]() 填官能团名称
填官能团名称![]() ;
;
![]() 已知X为
已知X为![]() ,写出该反应的化学方程式 ______ ;
,写出该反应的化学方程式 ______ ;
![]() 已知D与
已知D与![]() 二甲基甲酰胺,结构简式为
二甲基甲酰胺,结构简式为![]()
![]() 在
在![]() 三氯氧磷
三氯氧磷![]() 的催化下反应生成E,同时还生成
的催化下反应生成E,同时还生成![]() 和另一种有机物,写出该有机物的分子式 ______ ;
和另一种有机物,写出该有机物的分子式 ______ ;
![]() 的分子式为 ______ ,由E生成F的反应类型为 ______ ;
的分子式为 ______ ,由E生成F的反应类型为 ______ ;
![]() 的芳香同分异构体中苯环上有三个取代基,并且既能发生银镜反应,又能发生水解反应的有 ______ 种,其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为 ______
的芳香同分异构体中苯环上有三个取代基,并且既能发生银镜反应,又能发生水解反应的有 ______ 种,其中核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的为 ______ ![]() 写出其中一种的结构简式
写出其中一种的结构简式![]()
![]() 根据已有知识并结合相关信息,写出以
根据已有知识并结合相关信息,写出以![]() 和
和![]() 为原料制备
为原料制备![]() 的合成路线流程图
的合成路线流程图![]() 无机试剂任用
无机试剂任用![]() 合成路线流程图示例如下: ____________
合成路线流程图示例如下: ____________
![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题
(1)表中元素原子半径最大的原子共占据的轨道数是_________个,Y最外层电子排布式为________,Z原子核外有_____种能量不同的电子。
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
从原子结构的角度去解释Y元素的非金属性比S元素的非金属性强的原因:_______
(3)CO2的沸点_________CS2(填“>”或“<”或“=”),原因是_________________
(4)如果向BaCl2溶液中通入足量CO2气体,没有沉淀生成,继续滴加一定量的氨水后,则会生成白色沉淀。用电离平衡移动原理解释上述现象。________
(5)过量的CO2通入NaOH溶液中,得到NaHCO3,在0.1mol/L的NaHCO3溶液中,c(Na+)+c(H+)=________其中有关碳微粒的关系为:___________ = 0.1mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
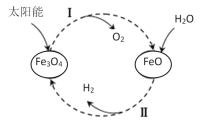
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232gFe3O4转移2mol电子
B.过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=-128.9kJ/mol
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D.铁氧化合物循环制H2具有成本低、产物易分离等优点
查看答案和解析>>
科目: 来源: 题型:
【题目】石油是一种重要的资源。A~F是常见有机物,它们之间的转化关系如图1所示(部分产物和反应条件已略去),其中A的产量可以用来衡量一个国家的石油化工发展水平,E是最简单的芳香烃。回答下列问题:

(1)步骤②所用试剂X为___________(写化学式),D的官能团名称是_______;
(2)F的结构简式为________________,步骤①的反应类型:___________;
(3)写出下列步骤中的化学方程式(注明反应条件):
步骤③_____________________________________;
步骤④_______________________________________;
(4)用图2所示实验装置制取乙酸乙酯。请回答:试管b中所装溶液应为_____,乙酸乙酯生成后,分离出产品时的操作方法是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关同分异构体的叙述正确的是
A. ![]() 苯环上的一氯取代物有5种
苯环上的一氯取代物有5种
B. 丁烷(C4H10)的二氯取代物最多有4种
C. 菲的结构简式为 ,其一硝基取代物有10种
,其一硝基取代物有10种
D.  和
和 互为同分异构体
互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:
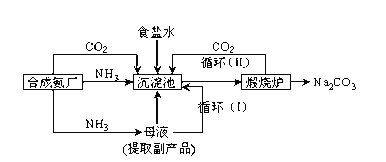
①沉淀池中反应的化学方程式:______;煅烧炉中发生的化学方程式:__________
②在常温下,向饱和Na2CO3的溶液中通入足量的CO2会有晶体析出,此晶体是NaHCO3。析出该晶体的原因是______________;在饱和的食盐水中先通入足量的氨,再通入足量的CO2,会有NaHCO3晶体析出,若在饱和的食盐水中先通入足量的CO2,再通入氨气,往往没有晶体析出,原因:______。
③检验产品碳酸钠中是否含有氯化钠的操作方法为:_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A是日常生活中最常见的金属,其转化关系如图(部分反应物或生成物已略去)。
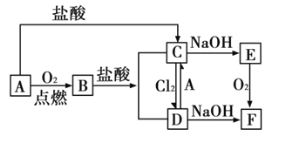
(1)写出![]() 的化学式_____________;溶液
的化学式_____________;溶液![]() 的颜色是______________。
的颜色是______________。
(2)写出下列转化的离子方程式:
①![]() :_________________。
:_________________。
②![]() :__________________。
:__________________。
(3)![]() 转化为
转化为![]() 过程中,可观察到白色沉淀迅速变成灰绿色,最后变成红褐色,该反应的化学方程式为:________________。
过程中,可观察到白色沉淀迅速变成灰绿色,最后变成红褐色,该反应的化学方程式为:________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
①![]() ;②
;②![]() ;③(CH3)3C–CHBr2;④CHCl2–CHBr2;⑤
;③(CH3)3C–CHBr2;④CHCl2–CHBr2;⑤![]() ;⑥CH3Cl
;⑥CH3Cl
A.全部B.②④C.①③⑥D.②③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】向某碳酸钠和碳酸氢钠的混合溶液中逐滴加入稀盐酸,加入稀盐酸的体积与标准状况下产生气体体积的关系如图所示。
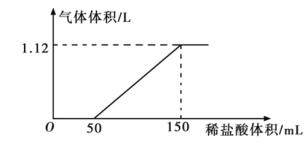
(1)生成![]() 气体的物质的量是多少?________________。
气体的物质的量是多少?________________。
(2)盐酸的物质的量浓度是多少?_____________。
(3)原溶液中碳酸钠与碳酸氢钠的物质的量之比是多少?_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com