
科目: 来源: 题型:
【题目】下列说法正确的是![]()
A.麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖
B.室温下,将![]() HA溶液和
HA溶液和![]() 溶液等体积混合
溶液等体积混合![]() 忽略体积的变化
忽略体积的变化![]() 测得混合溶液的
测得混合溶液的![]() ,则混合溶液中由水电离出的
,则混合溶液中由水电离出的![]()
C.纯碳新材料“碳纳米泡沫”,每个泡沫含有约4000个碳原子,直径约6到9nm,在低于![]() 时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同素异形体
时,泡沫具有永久磁性,“碳纳米泡沫”与石墨互为同素异形体
D.已知![]() 的
的![]() 为
为![]() ,则将等体积的
,则将等体积的![]()
![]() 的
的![]() 溶液和
溶液和![]()
![]()
![]() 溶液混合后会有
溶液混合后会有![]() 沉淀产生
沉淀产生
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关叙述不正确的是![]()
选项 | 已知 | 解释与结论 |
A | 活泼金属Al、不活泼金属Cu和浓硝酸可以形成原电池 | Al作正极,Cu作负极 |
B |
该反应在常温下能自发进行 | 该反应的 |
C | 常温下,
| 向 |
D | 向 | 氧化性: |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是( )
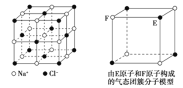
A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.该气态团簇分子的分子式为E4F4或F4E4
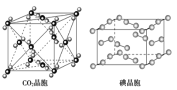
C.在CO2 晶体中,一个CO2 分子周围有4个CO2 分子紧邻
D.在碘晶体中,碘分子的排列有两种不同的方向
查看答案和解析>>
科目: 来源: 题型:
【题目】铜是人类最早发现并广泛使用的一种金属。回答下列问题:
(1)CuFeS2是其中铜的主要存在形式。CuFeS2中存在的化学键类型是_______。其组成的三种元素中电负性较强的是 _______。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是____,中心原子杂化类型为____。
②X的沸点比水低的主要原因是___________。
(3)[Cu(NH3)4]2+中,提供孤对电子的是________。Cu(NH3)2Cl2有两种同分异构体,其中一种可溶于水,则此种化合物是________(填“极性”或“非极性”)分子,由此推知 [Cu(NH3)4]2+的空间构型是________。
(4)某镍白铜合金的立方晶胞结构如图所示。
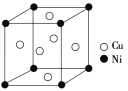
①晶胞中铜原子与镍原子的数量比为________。
②若合金的密度为d g·cm-3,晶胞参数a=________nm。(设NA代表阿伏加德罗常数)
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求写出下列反应的化学方程式。
(1)铁做催化剂,苯与溴单质反应_________________;
(2)CH3CH2CH2OH发生消去反应生成丙烯_____________;
(3)苯乙烯(![]() )在适当引发剂作用下生成聚苯乙烯_________________________。
)在适当引发剂作用下生成聚苯乙烯_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关叙述不正确的是
![]() 在
在![]() ,101KPa条件下,液态水气化热为40.69kJ/mol,则
,101KPa条件下,液态水气化热为40.69kJ/mol,则![]()
![]()
![]() 已知
已知![]() 时,
时,![]() 的
的![]() ,则在该温度下,含有固体
,则在该温度下,含有固体![]() 的溶液中,无论
的溶液中,无论![]() 与
与![]() 是否相等,总有
是否相等,总有![]()
![]() 已知:
已知:
共价键 | C--C |
| C--H | H一H |
键能 | 348 | 610 | 413 | 436 |
则反应![]()
![]()
![]()
![]()
![]() 常温下,在
常温下,在![]() 的
的![]() 溶液中加入少量
溶液中加入少量![]() 晶体,则
晶体,则![]() 电离被抑制,溶液pH减少
电离被抑制,溶液pH减少
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下反应:A2(g)+3 B2(g)![]() 2 AB3(g) (每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
2 AB3(g) (每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
A.Q2 = 2 Q1 B.2Q1 < Q2
C.Q1 < Q2 < 92.4 kJ D.Q1 = Q2 < 92.4 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】设Na为阿伏加德罗常数的值。已知反应:
①CH4 (g) +2O2 (g) = CO2 (g) +2H2O(l) △H1 =a kJ mol -1
②CH4(g) + 2O2 (g) = CO2 (g) +2H2O(g) △H2 =bkJ mol-1
键能定义:在标准状况下,将1 mol气态分子AB(g)解离为气态原子
A(g)、B(g)所需的能量。已知1 mol氧气的键能为xkJ。其他数据如下 表所示,下列说法正确的是
化学键 | C—O | C—H | O—H |
键能/(kJ mol-1) | 798 | 413 | 463 |
A.上文中x=![]()
B.H2O(g) = H2O(1)的△S<0、△H=(a — b) kJ mol -1
C.当有4NA个O—H键生成时,反应放出的热量为a kJ
D.利用反应①设计的原电池电解精炼铜,当负极输出0.2NA个电子时. 理论上电解槽的阴极质量增重6.4 g
查看答案和解析>>
科目: 来源: 题型:
【题目】硅藻土是由无定形SiO2组成的,含有少量Fe2O3、Al2O3及有机物等杂质,通常呈浅黄色或浅灰色,质软多孔。工业上可按如图所示流程,用硅藻土制备纳 米级二氧化硅。
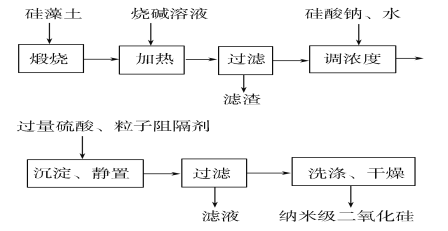
请回答下列问题:
(1)煅烧硅藻土的目的是___________。
(2)在加热条件下加入烧碱溶液时,发生反应的化学方程式为___________、__________。
(3)加入过量硫酸后,生成沉淀的离子方程式为_________。
(4)若用纳米级二氧化硅制成水溶液,则该溶液所具有的性质与下列图片有关的是________(填字母)。

查看答案和解析>>
科目: 来源: 题型:
【题目】“位置”、“结构”和“性质”是我们学习元素周期律的重要思路。
(1)我们可以根据原子结构示意图来推测元素在周期表中的位置,以下为X元素的原子结构示意图(未画全):
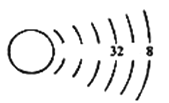
请写出X元素在周期表中的位置_____________________。
(2)我们也可以根据物质性质推测该元素在元素周期表中的位置,如Y元素最高价氧化物既可以溶于浓盐酸,也可以溶于NaOH溶液;其最高价氧化物对应的水化物既可以与酸反应,也可以与碱反应;1mol该元素最高价氧化物对应的水化物在与盐酸反应时,最多能消耗4molHCl。请写出Y元素在周期表中的位置_____________________。
(3)反过来,知道了元素的位置关系,我们可以推测元素性质或者元素对应的单质及化合物的性质。四种短周期元素在周期表中的位置如下图所示,其中只有M为金属元素。则Y和Z原子半径更大的是____(填元素符号或化学式,下同),Y和X最高价氧化物对应水化物的酸性更弱的是______。
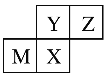
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com