
科目: 来源: 题型:
【题目】在下图所示的装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹,夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有一滴KMnO4;电源有a、b两极。若在A、B中充满0.01 mol/L 的KOH溶液后倒立于同浓度的KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如下图所示,则:
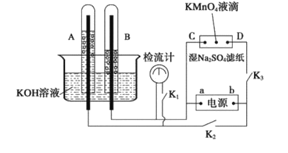
(1)断开K1,闭合K2、K3,通直流电,试管B中产生的气体为_________(填化学式)。
(2)在Na2SO4溶液浸湿的滤纸条中部的KMnO4处现象为_____________。
(3)断开K1,闭合K2、K3,通直流电较长一段时间后,KOH溶液pH变__________(填“变大”“变小”或“不变”)。
(4)电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,检流计有指数,此时该装置A试管中电极上发生的反应为_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】在可逆反应2A(g)+3B(g)![]() xC(g)+D(g)中,已知:反应开始加入的物质只有A、B,起始浓度A为5 mol·L-1,B为3 mol·L-1,前2 min C的平均反应速率为0.5 mol·L-1·min-1。2 min后,测得D的浓度为0.5 mol·L-1。则关于此反应的下列说法中正确的是( )
xC(g)+D(g)中,已知:反应开始加入的物质只有A、B,起始浓度A为5 mol·L-1,B为3 mol·L-1,前2 min C的平均反应速率为0.5 mol·L-1·min-1。2 min后,测得D的浓度为0.5 mol·L-1。则关于此反应的下列说法中正确的是( )
A.2 min末时A和B的浓度之比为5∶3
B.x=1
C.2 min末时B的浓度为1.5 mol·L-1
D.2 min末时A的消耗浓度为0.5 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.用50mL0.50mol/L的盐酸与50mL0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
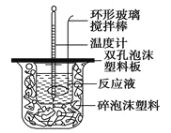
(1)烧杯间填满碎泡沫塑料的作用是______________;
(2)环形玻璃搅拌棒_______(填“能”或“不能”)用环形铁质搅拌棒代替,其原因是________;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是___________。实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量______ (填“相等”“不相等”),若实验操作均正确,则所求中和热_______ (填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:________。
Ⅱ.FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。已知25℃,101 kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1648 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480 kJ·mol-1
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A. 0.1 mol·L1NaOH溶液:Na+、K+、![]() 、
、![]()
B. 0.1 mol·L1FeCl2溶液:K+、Mg2+、![]() 、
、![]()
C. 0.1 mol·L1K2CO3溶液:Na+、Ba2+、Cl、OH
D. 0.1 mol·L1H2SO4溶液:K+、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】天然气因含有少量H2S等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法不正确的是
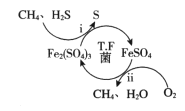
A. 该脱硫过程需要不断添加Fe2(SO4)3溶液
B. 脱硫过程O2间接氧化H2S
C. 亚铁是血红蛋白重要组成成分,FeSO4可用于治疗缺铁性贫血
D. 《华阳国志》记载“取井火煮之,一斛水得五斗盐”,我国古代已利用天然气煮盐
查看答案和解析>>
科目: 来源: 题型:
【题目】铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知![]() 与
与![]() 能发生反应:
能发生反应:![]()
(1)为确定某温度下![]() 固体的分解产物.称取
固体的分解产物.称取![]() 样品,将该样品在坩埚中加热完全分解,冷却至室温后,测得剩余固体质量为
样品,将该样品在坩埚中加热完全分解,冷却至室温后,测得剩余固体质量为![]() ,该固体的成分为 ______ ,若将所得固体溶于足量稀硫酸,所得固体质量为 ______
,该固体的成分为 ______ ,若将所得固体溶于足量稀硫酸,所得固体质量为 ______ ![]()
(2)科学研究发现![]() 可作为太阳光分解水的催化剂.
可作为太阳光分解水的催化剂.
Ⅰ通过以下四种方法来制备![]()
![]() 火法还原:用炭粉在高温条件下还原CuO;
火法还原:用炭粉在高温条件下还原CuO;
![]() 用
用![]() 还原新制电解的
还原新制电解的![]() ;
;
![]() 电解法:
电解法:![]()
![]()
![]() ;
;
![]() 最新实验研究用肼
最新实验研究用肼![]() 还原新制
还原新制![]() 可制备纳米级
可制备纳米级![]() ,同时放出
,同时放出![]() .
.
![]() 该制法的化学方程式为 ______ .
该制法的化学方程式为 ______ .
![]() 肼性质与氨气相似,易溶于水,可发生如下两步电离过程:
肼性质与氨气相似,易溶于水,可发生如下两步电离过程:
![]() /span>I
/span>I
![]() II
II
常温下,某浓度![]() 溶液的pH为4,则该溶液中由水电离产生的
溶液的pH为4,则该溶液中由水电离产生的![]() 为 ______ .
为 ______ .
已知在相同条件下过程I的进行程度大于![]() 的水解程度.常温下,若
的水解程度.常温下,若![]()
![]() 溶液与
溶液与![]() HCl溶液等体积混合,则溶液中
HCl溶液等体积混合,则溶液中![]() 、
、![]() 、
、![]() 、
、![]() 离子浓度由大到小的顺序为 ______ .
离子浓度由大到小的顺序为 ______ .
Ⅱ用制得的![]() 进行催化分解水的实验.
进行催化分解水的实验.
用以上四种方法制得的![]() 在相同条件下分别对水进行催化分解,产生氢气的体积
在相同条件下分别对水进行催化分解,产生氢气的体积![]() 随时间t变化如图所示,则下列说法正确的是 ______ .
随时间t变化如图所示,则下列说法正确的是 ______ .
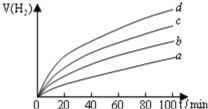
A.c、d方法制得的![]() 催化效率相对较高
催化效率相对较高
B.d方法制得的![]() 作催化剂时,水的平衡转化率最高
作催化剂时,水的平衡转化率最高
C.催化效果与![]() 颗粒的粗细、表面活性等有关
颗粒的粗细、表面活性等有关
D.分解等物质的量的水时,d方法制得的![]() 作催化剂所需吸收的能量最低.
作催化剂所需吸收的能量最低.
查看答案和解析>>
科目: 来源: 题型:
【题目】在25℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式书写正确的是()
A. CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
B. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-1 451.52 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-1 451.52 kJ·mol-1
C. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
D. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l)ΔH=+1451.52 kJ·mol-1
2CO2(g)+4H2O(l)ΔH=+1451.52 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。A是元素Y的单质。常温下,甲的浓溶液和A发生钝化。丙、丁、戊是由这些元素组成的二元化合物,且丙是无色气体。上述物质的转化关系如图所示。下列说法正确的是
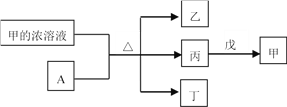
A. 丁和戊中所含元素种类相同
B. 简单离子半径大小:X<Y
C. 气态氢化物的还原性:X>Z
D. Y的简单离子与Z的简单离子在水溶液中可大量共存
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物Y具有抗菌、消炎作用,可由X制得。
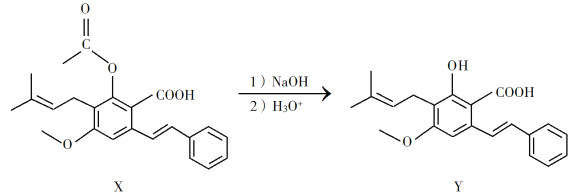
下列有关化合物X、Y的说法正确的是
A. 1 mol X最多能与2 mol NaOH反应
B. Y与乙醇发生酯化反应可得到X
C. X、Y均能与酸性KMnO4溶液反应
D. 室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目相等
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家设计了一种太阳能驱动的H2S分解装置,工作原理如图所示。下列叙述正确的是( )
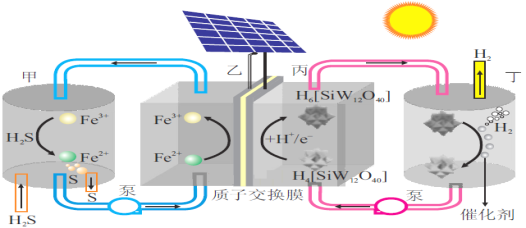
A.甲区发生反应的离子方程式为:2Fe3++S2-=2Fe2++S↓
B.理论上每生成1molS时,H+由质子交换膜右侧向左侧移动的物质的量为2mol
C.丙区发生的电极反应为:H4[SiW12O40]+2e-+2H+=H6[SiW12O40]
D.丁区H6[SiW12O40]在催化剂表面发生电化学反应生成H4[SiW12O40]和H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com