
科目: 来源: 题型:
【题目】汽车用汽油的抗爆剂约含 17%的 1,2一二溴乙烷。某学习小组用下图所示装置制备少量 1,2 一二溴乙烷,具体流秳如下: 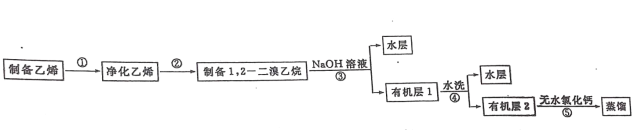
已知:1,2 一二溴乙烷的沸点为131℃,熔点为9.3℃。Ⅰ1,2 一二溴乙烷的制备步聚①、②的实验装置为:

实验步骤:
(ⅰ)在冰水冷却下,将 24mL 浓硫酸慢慢注入12mL乙醇中混合均匀。
(ⅱ)向 D 装置的试管中加入3.0mL 液溴(0.10mol),然后加入适量水液封,幵向烧杯中加入冷却剂。
(ⅲ)连接仪器并检验气密性。向三口烧瓶中加入碎瓷片,通过滴液漏斗滴入一部分浓硫酸与乙醇的混合物,一部分留在滴液漏斗中。
(ⅳ)先切断瓶C与瓶D的连接处,加热三口瓶,待温度上升到约120℃,连接瓶 C与瓶D,待温度升高到180~200℃,通过滴液漏斗慢慢滴入混合液。
(V)继续加热三口烧瓶,待D装置中试管内的颜色完全褪去,切断瓶C与瓶D的连接处,再停止加热。回答下列问题:
(1)图中 B 装置玻璃管的作用为__________________________________________。
(2)(ⅳ)中“先切断瓶C与瓶D的连接处,再加热三口瓶”的原因是__________________________________________。
(3)装置D的烧杯中需加入冷却剂,下列冷却剂合适的为__________________________________________。
a.冰水混合物 b.5℃的水 c.10℃的水
Ⅱ1,2 一二溴乙烷的纯化
步骤③:冷却后,把装置 D 试管中的产物转移至分液漏斗中,用 1%的氢氧化钠水溶液洗涤。
步骤④:用水洗至中性。
步骤⑤:“向所得的有机层中加入适量无水氯化钙,过滤,转移至蒸馏烧瓶中蒸馏,收集
130~132℃的馏分,得到产品5.64g。
(4)步骤③中加入 1%的氢氧化钠水溶液时,发生反应的离子方程式为__________________________________________。
(5)步骤⑤中加入无水氯化钙的作用为_________________________。该实验所得产品的产率为__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
(1)CH3CH2CH2COOH________,
(2)HCOOC2H5________,
(3)CH3CH2CH2CH2Cl________,
(4)CH3CHO________,
(5)![]() _________,
_________,
(6)![]() _________,
_________,
(7)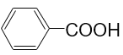 _________,
_________,
(8)CH3CH2CH=CHCH3_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应mA(s)+nB(g)![]() eC(g)+fD(g),当其他条件不变时,C的体积分数[φ(C)]在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是( )
eC(g)+fD(g),当其他条件不变时,C的体积分数[φ(C)]在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是( )

A.达到平衡后,若使用催化剂,C的体积分数将增大
B.该反应的ΔH<0
C.化学方程式中,n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图及操作步骤如下:
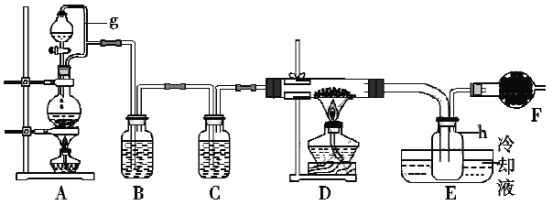
请回答下列问题:
(1)装置A中g管的作用是___;装置B中的试剂是___;E处左方选用较粗玻璃管的原因是___;装置F中盛碱石灰干燥管的作用是___。
(2)检验装置的气密性;点燃A处的酒精灯。写出装置A中发生反应的离子方程式___。
当h中充满黄绿色气体时点燃D处铁屑下方的酒精灯。反应结束,将收集器h密封。
(3)检验收集器h收集到的是FeCl3而木是FeCl2步骤是:①取收集器中的少量样品溶于少量浓盐酸,加水稀释,将溶液分为两份;②一份溶液检验出三价铁离子;③另一份溶液不能检验出二价铁离子。
①中盐酸的作用是___;②中检验出三价铁离子的离子方程式___。③检验无二价铁离子的方法是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6C1F3= 6CoF3+3C12+4X。下列有关该反应的说法,正确的是
A. X与O3互为同位素 B. ClF3中氯元素为-3价
C. Co3O4在反应中作氧化剂 D. lmol Co3O4参加反应转移9 mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】反应4A(g)+3B(g)=2C(g)+D(g),经2min,B的浓度减少0.6 molL-1。对此反应速率的表示正确的是( )
①用A表示的反应速率是0.4 molL-1min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 molL-1min-1
④在这2 min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的
A. ①②
B. ③
C. ①
D. ②④
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列物质的名称:
A.(CH3)3CCH(CH3)(CH2)2CH(C2H5)2 A的名称是________;
B.(CH3)3CC≡CCH2CH3 B的名称是____;
C.![]() C的名称是_____
C的名称是_____
D.CH2OHCH(C2H5) CH2OH D的名称是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
下列说法错误的是( )
A.CH3OH转变成H2的反应不一定要吸收能量
B.1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ
C.反应①中的能量变化如图所示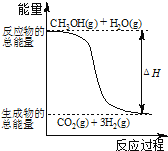
D.根据反应①和②推知:H2(g)+1/2O2(g)=H2O(g) ΔH=-241.9kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】无水三氯化铬(CrCl3)为紫色晶体,在工业上主要用作媒染剂和催化剂,某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示。
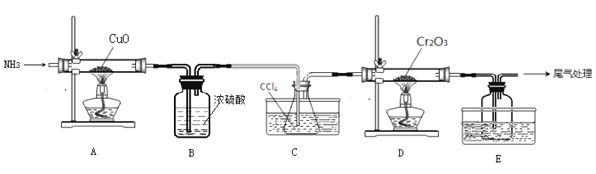
已知:①CrCl3熔点为83℃,易潮解,易升华,易溶于水但不易水解,高温下易被氧气氧化;②Cr2O3和CCl4在高温下反应的产物为CrCl3和光气(COCl2 )。请回答下列问题:
(1)装置A是氮气制备装置,氮气的作用是____________。
(2)装置B的作用为________。装置C和装置E的水槽中应分别盛有__________、____________。
(3)装置D中生成CrCl3和光气(COCl2 )的化学方程式为_________。
(4)该实验装置有设计不合理的地方,请写出改进方法:_________(写一点即可)
(5)产品中CrCl3质量分数的测定:
(i)称取0.3000 g得到的CrCl3样品溶于水并于250mL容量瓶中定容。
(ii)取25.00mL样品溶液于带塞的锥形瓶中,加热至沸腾后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的H2SO4酸化,将Cr3+氧化为Cr2O72-;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在
(iii)加入1mL指示剂,用0.0250 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL(已知2Na2S2O3+I2= Na2S4O6+2NaI)
①ii中加入稍过量的Na2O2后要加热煮沸,其主要原因是____________;加入KI发生反应的离子方程式为________________
②滴定实验可选用的指示剂为____________产品中CrCl3质量分数为_______%(结果保留两位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com