
科目: 来源: 题型:
【题目】氢气不仅是新能源,也是重要的化工原料。
(1)氢气可由甲烷制备:CH4 (g)+H2O(l)![]() CO(g)+3H2 (g)ΔH=+250.1 kJ·mol-1,已知298 K时,CH4(g)、CO(g)的燃烧热分别为890 kJ·mol-1、283 kJ·mol-1。写出氢气燃烧热的热化学方程式___________。
CO(g)+3H2 (g)ΔH=+250.1 kJ·mol-1,已知298 K时,CH4(g)、CO(g)的燃烧热分别为890 kJ·mol-1、283 kJ·mol-1。写出氢气燃烧热的热化学方程式___________。
(2)利用反应CO(g)+2H2(g)![]() CH3OH(g) ΔH合成清洁能源CH3OH,CO的平衡转化率与温度的关系如图所示:
CH3OH(g) ΔH合成清洁能源CH3OH,CO的平衡转化率与温度的关系如图所示:
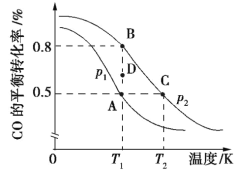
①该可逆反应的正反应ΔH______0; A、B、C三点平衡常数KA、KB、KC的大小关系是_____; 压强p1___p2(填“>”“<”或“=”); 在T1和p2条件下,由D点到B点过程中,正、逆反应速率之间的关系: v正___v逆(填“>”“<”或“=”)。
②若在恒温恒容条件下进行上述反应,能表示该可逆反应达到平衡状态的是_____________________ (填序号)。
a.CO物质的量保持不变
b.单位时间内消耗CO的浓度和生成甲醇的浓度相等
c.混合气体的压强不再变化
d.混合气体的密度不再变化
③在2 L恒容密闭容器中充入2 mol CO和4 mol H2,在p2 (和T2条件下经10 min达到平衡状态C点,在该条件下,v(CH3OH)=______________________;平衡常数K为_________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CH3OH的摩尔质量是__gmol-1。
(2)2molH2O中所含原子的物质的量为__mol。
(3)__g的氢气中所含H原子的数目与1molCH3OH相同。
(4)含0.1NA个O的CO2中有__个电子,标况下该CO2的体积为__L。
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
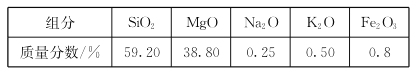
通过下图流程可由蛇纹石制备较纯净的二氧化硅。
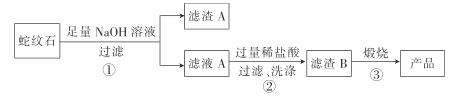
(1)蛇纹石中涉及的可溶性金属氧化物有___________________(写化学式)。
(2)步骤①中涉及SiO2 反应的离子方程式为_________________________ 。
(3)滤渣 A的成分有__________________ (填化学式)。
(4)步骤②中洗涤沉淀的方法是 _____________________________________________。
(5)步骤③反应的化学方程式为 _______________________________________;实验室进行步骤③需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、________和____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(化学——选修5:有机化学基础)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:
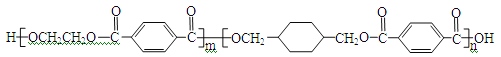
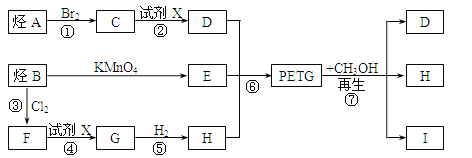
这种材料可采用如下图所示的合成路线:
已知:(1)![]()
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)⑥的反应类型是____,试剂X为_______,E中官能团的名称为_______。
(2)写出I的结构简式:__________________。
(3)合成时应控制的单体的物质的量:n(D)∶n(E)∶n(H)=___________(用m、n表示)。
(4)写出反应③的化学方程式:_____________________。
(5)与G的分子式相同,且只含有一个酚羟基的同分异构体(醚类除外)有_______种,其中核磁共振氢谱有6种不同类型的吸收峰,且峰的面积之比为1∶1∶1∶2∶2∶3的结构简式为_____。
(6)D和E在催化剂作用下可生产一种聚酯纤维——涤纶,请写出生产该物质的化学方程式________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用生活中或实验室中的常用物品,根据氧化还原反应知识和电化学知识,自己动手设计一个原电池.请填写下列空白:
(1)实验原理:Fe+2H+=Fe2++H2↑
(2)实验用品:电极(__、__)、稀硫酸、__、__耳机(或电流计).
(3)①按如图所示装置连接好实验仪器,这时可以听见耳机发出“嚓嚓……”的声音。其原因是在原电池中化学能转化为__,在耳机中__又转化为声波这种能量。
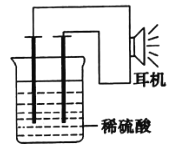
②在该原电池内中,Fe在___极发生了___反应,H+在___极发生了___反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】对反应A+B=AB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol
②50 mL溶液中含A、B各0.05 mol
③0.1 mol·L-1的A、B溶液各10 mL
④0.5 mol·L-1的A、B溶液各50 mL
四者反应速率的大小关系是
A.②>①>④>③B.④>③>②>①
C.①>②>④>③D.①>②>③>④
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为一重要的烃的衍生物,以下关于它的说法中不正确的是( )
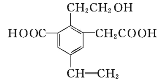
A.1mol该物质,最多可以和4molH2发生加成反应
B.1mol该物质消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
C.可以用酸性高锰酸钾溶液检验其中的碳碳双键
D.该物质能够在催化剂作用下被氧化为醛
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,物质的量均为0.3mol的X(g)与Y(g)在容积固定的密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g),ΔH=-akJ·mol-1,下列说法正确的是( )
2Z(g),ΔH=-akJ·mol-1,下列说法正确的是( )
A.反应一段时间后,X与Y的物质的量之比仍为1:1
B.达到平衡时,反应放出0.1akJ的热量
C.达到平衡后,向平衡体系中充入稀有气体,正反应速率不发生变化
D.X的体积分数保持不变,说明反应已达到平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:

(1)A是一种遇到碘单质能变蓝的多糖,A的分子式是_______________。
(2)物质B、C都能在加热条件下与新制的氢氧化铜反应产生砖红色沉淀,但不能发生水解反应,B中官能团的名称为____________,写出反应②的化学方程式___________________。
(3)下图是实验室通过反应①制取少量E的装置图。

实验时,加热前试管a中三种化学试剂的加入顺序依次为__________________(填名称),其中浓硫酸的作用是____________,写出试管a中生成E的化学反应方程式___________________。
(4)上述流程中C2H3Cl的结构简式____________。
(5)上述流程中标号①至④的反应中,与下列反应属同一反应类型的有______________。
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式的书写及相关说法正确的是( )
A. CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ
B. C(s)+![]() O2(g)===CO(g) ΔH=-101.5 kJ·mol-1,该方程式的ΔH可表示碳的燃烧热
O2(g)===CO(g) ΔH=-101.5 kJ·mol-1,该方程式的ΔH可表示碳的燃烧热
C. 2 mol氢气燃烧得水蒸气放热484 kJ,则H2O(g)===H2(g)+![]() O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1
D. Ba(OH)2(aq)+H2SO4(aq)===BaSO4(s)+2H2O(l) ΔH=-2a kJ·mol-1,则任何强酸和强碱发生中和反应生成1 mol H2O(l)的反应热均为-a kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com