
【题目】CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CH3OH的摩尔质量是__gmol-1。
(2)2molH2O中所含原子的物质的量为__mol。
(3)__g的氢气中所含H原子的数目与1molCH3OH相同。
(4)含0.1NA个O的CO2中有__个电子,标况下该CO2的体积为__L。
【答案】32 6 4 1.1NA 1.12L
【解析】
(1)摩尔质量的数值等于相对分子质量,单位为gmol-1。
(2)计算分子中所含原子数,应利用化学式建立关系式。
(3)求含相同某原子的两分子的质量或物质的量关系,可利用相等的原子建立两分子的数量关系。
(4)利用分子中的一个量求另一个量,可利用化学式建立关系式,再利用公式进行转换。
(1)M(CH3OH)=(12×1+1×4+16×1 )gmol-1=32gmol-1。答案为:32;
(2)已知每个水分子中含有两个氢原子和一个氧原子,则n(原子数)=3×2 mol=6mol。答案为:6;
(3)1mol CH3OH中含有n(H)=4×1mol=4 mol,则氢气中氢原子物质的量也为4 mol,那么n(H2)=2 mol,m(H2)=2mol×2 gmol-1=4g。答案为:4;
(4)n(O)=![]() =0.1mol,那么n(CO2)=0.05mol,又因为每个CO2中含有电子数为6+8×2=22个,则含0.1NA个O的CO2中有电子数= n(CO2)×NA×22=1.1NA,V(CO2)= n(CO2)×Vm=0.05mol×22.4 Lmol-1=1.12 L。答案为:1.1NA;1.12L。
=0.1mol,那么n(CO2)=0.05mol,又因为每个CO2中含有电子数为6+8×2=22个,则含0.1NA个O的CO2中有电子数= n(CO2)×NA×22=1.1NA,V(CO2)= n(CO2)×Vm=0.05mol×22.4 Lmol-1=1.12 L。答案为:1.1NA;1.12L。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】研究金属与硝酸的反应,实验如下。

(1)Ⅰ中的无色气体是_________。
(2)Ⅱ中生成H2的离子方程式是______________________________________。
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于NO3-,所以NO3-没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是_______________________________。
②乙同学通过分析,推测出NO3-也能被还原,依据是___________________________,进而他通过实验证实该溶液中含有NH4+,其实验操作是__________________________
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有_________________________试推测还可能有哪些因素影响_________(列举1条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)H2O的相对分子质量是______;1 molH2O质量是______克;1.5 mol H2O的质量为_____;H2O的摩尔质量是_____。
(2)3.01×1022个OH-的物质的量为____mol,质量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
(1)C分子的质谱图如图所示,从图中可知其相对分子质量是__,则C的分子式是__。
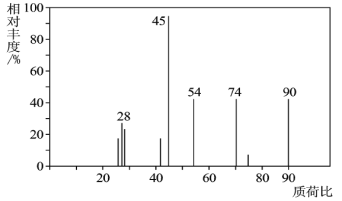
(2)C能与NaHCO3溶液发生反应,C一定含有的官能团是__。
(3)C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则C的结构简式是__。
(4)0.1molC与1.0mol/L的氢氧化钠溶液反应,需溶液的体积是__mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示。下列叙述中不正确的是: ( )
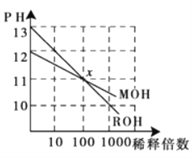
A. ROH是一种强碱
B. 在x点,MOH并没有完全电离
C. 在x点,c(M+)=c(R+)
D. 稀释前,c(ROH)=10c(MOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式书写正确的是
A.往稀盐酸中逐滴加入Na2CO3溶液,开始时:H++CO32-=HCO3-
B.草酸(H2C2O4)溶液中加入酸性KMnO4溶液:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
C.往少量澄清石灰水中加入Ca(HCO3)2溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
D.用HI溶液溶解Fe2O3固体:Fe2O3+6H+=2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知: C(s)+O2(g) = CO2(g) △H1 = 393.5kJ·mol1
2C(s)+O2(g) = 2CO(g) △H2 = 221.0 kJ·mol1
N2(g)+O2(g) = 2NO(g) △H 3 =+180.5 kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_________________________。
(2)研究CO和NO的催化反应,用气体传感器测得在某温度下、一定体积的密闭容器中,不同时间NO和CO浓度如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(______)4mol·L1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(______)3mol·L1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前4 s内的平均反应速率υ(CO) =______mol·L1·s1。
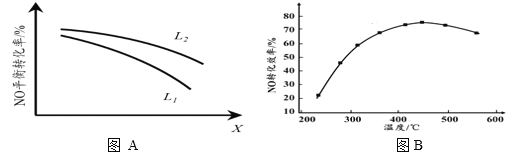
② L、X可分别代表压强或温度。下图A表示L一定时,NO(g)的平衡转化率随X的变化关系。X代表的物理量是______。判断L1、L2的大小关系,并简述理由:______________________________。
(3)实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2) ·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数______(填“>”、“
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆 =___________。(保留一位小数)
II. 有人利用反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率是不是对应温度下的平衡转化率及判断理由是________________________;
N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率是不是对应温度下的平衡转化率及判断理由是________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水电池常用在海上浮标等助航设备中,其示意图如图所示。电池反应为2Li+2H2O=2LiOH+H2↑。电池工作时,下列说法错误的是( )
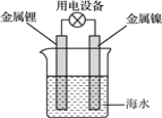
A.金属锂作负极
B.电子从锂电极经导线流向镍电极
C.海水作为电解质溶液
D.可将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某高能锂离子电池的总反应为:2Li+FeS= Fe +Li2S,电解液为含LiPF6·SO(CH3)2的有机溶液(Li+可自由通过)。某小组以该电池为电源电解废水并获得单质镍,工作原理如图所示。
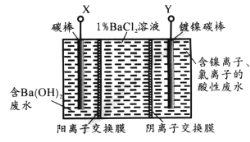
下列分析正确的是
A.X与电池的Li电极相连
B.电解过程中c(BaC12)保持不变
C.该锂离子电池正极反应为:FeS+2Li++2e =Fe +Li2S
D.若去掉阳离子膜将左右两室合并,则X电极的反应不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com