
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃКCO(g) ЃЋ H2O(g) ![]() H2(g) ЃЋ CO2(g)ЕФЦНКтГЃЪ§KЫцЮТЖШЕФБфЛЏШчЯТБэЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ ЃЈ ЃЉ
H2(g) ЃЋ CO2(g)ЕФЦНКтГЃЪ§KЫцЮТЖШЕФБфЛЏШчЯТБэЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ ЃЈ ЃЉ
ЮТЖШ/Ёц | 400 | 500 | 830 | 1000 |
ЦНКтГЃЪ§K | 10 | 9 | 1 | 0.6 |
A.ИУЗДгІЕФе§ЗДгІЪЧЮќШШЗДгІ
B.КуЮТЪБМѕаЁШнЦїЬхЛ§діДѓбЙЧПЃЌе§ЗДгІЫйТЪдіДѓ
C.830 ЁцЪБЃЌЗДгІДяЕНЦНКтЃЌвЛЖЈЪЧc(CO) ЃН c(CO2)
D.400 ЁцЪБЃЌЩњГЩCO2ЮяжЪЕФСПдНЖрЃЌЦНКтГЃЪ§KдНДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌдквЛИеадШнЦїФкВПгавЛИіВЛТЉЦјЧвПЩвдЛЌЖЏЕФЛюШћЃЌНЋШнЦїЗжИюГЩзѓгвСНЪвЁЃзѓЪвГфШыN2ЃЌгвЪвГфШыH2КЭO2ЃЌЛюШће§КУЪЙN2еМШнЦїЬхЛ§ЕФ1ЃЏ4ЃЈШчЭМЃЉЁЃШЛКѓЕуШМH2КЭO2ЕФЛьКЯЦјЬхЃЌЗДгІЭъБЯКѓЛжИДжСдРДЕФЮТЖШЃЌЛюШће§КУЭЃСєдкШнЦїЕФжаМфЁЃОМьбщЃЌДЫЪБгвЪвжаЦјЬхПЩЪЙДјЛ№аЧЕФФОЬѕИДШМЁЃ
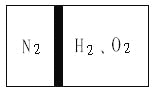
ЃЈ1ЃЉЧѓЗДгІЧАH2КЭO2ЕФЮяжЪЕФСПжЎБШЁЃ
ЃЈ2ЃЉЧѓЗДгІЧАH2КЭO2ЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФЦШлШкбЮШМСЯЕчГигЕгаБШяЎЕчГиИпвЛБЖЕФФмСПУмЖШЃЌдкЭЌЕШЕчГиЬхЛ§ЯТЃЌПЩШУЕчЖЏЦћГЕааЪЛОрРыГЩБЖЬсЩ§ЁЃШчЭМЫљЪОЪЧФГФЦШлШкбЮШМСЯЕчГиЃЌЦфжаЩњГЩЮяYЪЧвЛжжбѕЛЏЮяЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
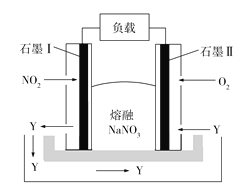
A. ЕчГиЙЄзїЪБЃЌЪЏФЋЕчМЋЂёЩЯЕчМЋЗДгІЪНЮЊ2NO2 2e +O2![]() N2O5
N2O5
B. ЕчГиЙЄзїЪБЃЌ![]() ЯђЪЏФЋЕчМЋЂёвЦЖЏ
ЯђЪЏФЋЕчМЋЂёвЦЖЏ
C. ИУЕчГиГфЕчЪБЃЌЪЏФЋЕчМЋЂђСЌНгЕчдДЕФИКМЋ
D. ЕчГиЙЄзїЪБЃЌЭтЕчТЗжаСїЙ§1 molЕчзгЃЌдђЯћКФ46 g NO2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПКуЮТЁЂКубЙЯТЃЌдквЛИіШнЛ§ПЩБфЕФШнЦїжаЗЂЩњШчЯТЗДгІЃКN2(g)ЃЋ3H2(g)![]() 2NH3(g)
2NH3(g)
ЃЈ1ЃЉШєПЊЪМЪБЗХШы1 mol N2КЭ3 mol H2ЃЌДяЕНЦНКтКѓЃЌЩњГЩa mol NH3ЃЌетЪБN2ЕФЮяжЪЕФСПЮЊ________mol
ЃЈ2ЃЉШєПЊЪМЪБЮоNH3ЃЌжЛЗХШыN2КЭH2ЃЌДяЕНЦНКтЪБЩњГЩNH3ЕФЮяжЪЕФСПЮЊ3a molЃЌдђПЊЪМЪБЗХШыH2ЕФЮяжЪЕФСПЮЊ________mol(ЦНКтЪБNH3ЕФжЪСПЗжЪ§гы(1)жаЯрЭЌ)ЁЃ
ЃЈ3ЃЉШєПЊЪМЪБЗХШыx mol N2ЁЂ6 mol H2КЭ2 mol NH3ДяЕНЦНКтКѓЃЌN2КЭNH3ЕФЮяжЪЕФСПЗжБ№ЮЊy molКЭ3a molЃЌдђyЃН________ЁЃЦНКтЪБH2ЕФЮяжЪЕФСП________(бЁЬювЛИіБрКХ)ЁЃ
AЃЎДѓгк6 mol BЃЎЕШгк6 mol CЃЎаЁгк6 mol DЃЎПЩФмДѓгкЁЂаЁгкЛђЕШгк6 mol
ЃЈ4ЃЉШєдкЃЈ3ЃЉЕФЦНКтЛьКЯЮяжаЃЌдйМгШы6 mol NH3ЃЌдйДЮДяЕНЦНКтКѓЃЌNH3ЕФжЪСПЗжЪ§ЮЊ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПфхБНЪЧвЛжжГЃМћЕФЛЏЙЄдСЯЁЃВщдФзЪСЯжЊЃКБНКЭвКфхдкфхЛЏЬњЃЈFeBr3ЃЉДцдкЕФЬѕМўЯТПЩЗЂЩњЗДгІЩњГЩфхБНЃЌДЫЗДгІЮЊЗХШШЗДгІЁЃЪЕбщЪвКЯГЩфхБНЕФзАжУЪОвтЭММАгаЙиЪ§ОнШчЯТЁЃЯШЯђAжаМгШы16.0mLЕФЮоЫЎБНКЭ5.0mLвКфхЃЌдйНЋЛьКЯвКТ§Т§ЕЮШыЗДгІЦїBжаЁЃЧыЛиД№ЯТСаЮЪЬтЃК
БН | фх | фхБН | |
ЯрЖдЗжзгжЪСП | 78 | 160 | 157 |
беЩЋзДЬЌ | ЮоЩЋвКЬх | ЩюКьзиЩЋвКЬх | ЮоЩЋвКЬх |
УмЖШ/gЁЄcm-3 | 0.88 | 3.10 | 1.50 |
ЗаЕу/Ёц | 80 | 59 | 156 |
ЫЎжаЕФШмНтад | ФбШм | ЮЂШм | ФбШм |

ЃЈ1ЃЉвЧЦїAЕФУћГЦЮЊ____ЁЃ
ЃЈ2ЃЉЗДгІЦїBжаЗЂЩњЕФжївЊгаЛњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ___ЁЃ
ЃЈ3ЃЉЯТСаЙигкИУЪЕбщВйзїЛђа№ЪіДэЮѓЕФЪЧ___ЃЈЬюзжФИађКХЃЉЁЃ
a.ЯђЗДгІЦїBжаЕЮМгБНКЭфхЕФЛьКЯвКЧАашЯШЙиБеK
b.ЪЕбщжазАжУCжаЕФвКЬхж№НЅБфЮЊЧГКьЩЋ
c.ЪЕбщжазАжУDжаЕФЕМЙмПкИННќгаАзЮэВњЩњЃЌШмвКжаВњЩњЕЛЦЩЋЕФГСЕэЃЌИљОнИУЯжЯѓЫЕУїБНКЭвКфхЗЂЩњЕФЗДгІЮЊМгГЩЗДгІ
d.зАжУDжаЕФЕМЙмВЛФмВхШывКУцвдЯТКЭзАжУEжаЕМЙмФЉЖЫСЌНгЕЙПлзХЕФТЉЖЗЖМЪЧЮЊСЫЗРЕЙЮќ
e.фхБНВЛФмгыAgNO3ШмвКЗДгІВњЩњЕЛЦЩЋГСЕэ
ЃЈ4ЃЉЪЕбщЭъБЯД§РфШДКѓЃЌОЙ§ЯТСаВНжшЖдфхБННјааЗжРыЬсДПЃК
ЂйЯђBжаМгШы10mLЫЎЃЌШЛКѓЙ§ТЫГ§ШЅЮДЗДгІЕФЬњаМЃЛ
ЂкТЫвКвРДЮгУ10mLЫЎЁЂ8mL10%ЕФNaOHШмвКЁЂ10mLЫЎЯДЕгЁЃгУNaOHШмвКЯДЕгЕФзїгУЪЧ___ЃЛ
ЂлЯђЗжРыГіЕФДжфхБНжаМгШыЩйСПЕФЮоЫЎТШЛЏИЦЃЌОВжУЁЂЙ§ТЫЁЃ
ЃЈ5ЃЉОЙ§ЩЯЪіЗжРыВйзїКѓЃЌДжфхБНжаЛЙКЌгаЕФжївЊдгжЪЮЊ__ЃЌвЊНјвЛВНЬсДПЃЌЯТСаВйзїжаБиаыЕФЪЧ___ЁЃ
a.нЭШЁ b.еєСѓ c.жиНсОЇ d.Й§ТЫ e.ЗжвК
ЃЈ6ЃЉШєОЙ§ЩЯЪіЗжРыЬсДПЕФВйзїЃЌОНјвЛВНОЋжЦЕУЕН6.2mLЕФфхБНЃЌдђИУЪЕбщжафхБНЕФВњТЪЪЧ___ЃЈМЦЫуНсЙћБЃСєШ§ЮЛгааЇЪ§зжЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋЬњЗлКЭЛюадЬПЕФЛьКЯЮягУNaClШмвКЪЊШѓКѓЃЌжУгкШчЭМЫљЪОзАжУжаЃЌНјааЬњЕФЕчЛЏбЇИЏЪДЪЕбщЁЃЯТСагаЙиИУЪЕбщЕФЫЕЗЈе§ШЗЕФЪЧ
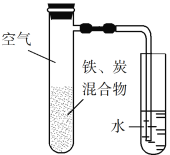
A. ЬњБЛбѕЛЏЕФЕчМЋЗДгІЪНЮЊFe3e![]() Fe3+
Fe3+
B. ЬњИЏЪДЙ§ГЬжаЛЏбЇФмШЋВПзЊЛЏЮЊЕчФм
C. ЛюадЬПЕФДцдкЛсМгЫйЬњЕФИЏЪД
D. вдЫЎДњЬцNaClШмвКЃЌЬњВЛФмЗЂЩњЮќбѕИЏЪД
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАБХ№Эщ(NH3ЁЄBH3)ЕчГиПЩдкГЃЮТЯТЙЄзїЃЌзАжУШчЭМЫљЪОЁЃИУЕчГиЙЄзїЪБЕФзмЗДгІЮЊЃКNH3ЁЄBH3+3H2O2=NH4BO2+4H2OЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ

A. зАжУзѓВрЕчМЋЮЊИКМЋЃЌЕчзггЩИУМЋГіЗЂЃЌвРДЮЭЈЙ§е§МЋЁЂЕчНтжЪШмвКЃЌЛиЕНИКМЋ
B. е§МЋЕФЗДгІЪНЮЊЃКH2O2+2H++2eЃ=2H2O
C. ЕчГиЙЄзїЪБЃЌH+ЭЈЙ§жЪзгНЛЛЛФЄЯђе§МЋвЦЖЏЃЌ
D. ЯћКФ3.lgАБХ№ЭщЃЌРэТлЩЯзЊвЦ0.6molЕчзг
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЗДгІO2(g)+2Cl2(g) ![]() 2Cl2O(g) ЁїH>0ЃЌдкШ§ИіКуЮТЁЂКуШнЕФУмБеШнЦїжаЗжБ№ГфШЫlmolO2гы2molCl2ЃЌВтЕУЦНКтЪБO2ЕФзЊЛЏТЪШчЯТБэЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
2Cl2O(g) ЁїH>0ЃЌдкШ§ИіКуЮТЁЂКуШнЕФУмБеШнЦїжаЗжБ№ГфШЫlmolO2гы2molCl2ЃЌВтЕУЦНКтЪБO2ЕФзЊЛЏТЪШчЯТБэЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
ШнЦїБрКХ | ЮТЖШЃЈЁцЃЉ | ШнЦїЬхЛ§/L | ЦНКтЪБO2зЊЛЏТЪ | ЦНКтЪБбЙЧПЃЈPaЃЉ |
Ђй | 200 | V1 | 50% | P1 |
Ђк | 200 | V2 | 70% | P2 |
Ђл | 350 | V3 | 50% | P3 |
A. ЗДгІЫйТЪЃКЂлЃОЂйЃОЂк
B. ЦНКтЪБбЙЧПЃКP1>P2
C. ШнЦїЬхЛ§ЃКV1<V3
D. ШєЪЕбщЂкжаO2КЭCl2гУСПОљМгБЖЃЌдђЦНКтЪБO2ЕФзЊЛЏТЪаЁгк70%
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПБНЗгОпгаЮЂШѕЕФЫсадЃЌПЩРћгУЕчГЁДйЪЙC6H5OЃЖЈЯђвЦЖЏЁЂЭбРыЗЯЫЎЃЌВЂИЛМЏЛиЪеЁЃЕчЩјЮізАжУЪОвтЭМШчЯТЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ

A. БНЗгЕФЕчРыЗНГЬЪНЮЊЃК
B. AЁЂBЗжБ№ЮЊРызгНЛЛЛФЄЃЌЦфжаAЪЧвѕРызгНЛЛЛФЄ
C. ЕчНтЙ§ГЬжаЃЌбєМЋЪвЕФpHдіДѓ
D. ЕБЭЈЙ§ЯпТЗжаЕФЕчзгЪ§ФПЮЊ0.1 NAЪБЃЌгаКЌ0.1mol C6H5OЃЕФЗЯЫЎБЛДІРэ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛИіЮТЖШКуЖЈЁЂШнЛ§ЙЬЖЈЕФУмБеШнЦїжаЃЌЗЂЩњПЩФцЗДгІ
mA(s)+nB(g) ![]() pC(g)+qD(g)ЃЌвбжЊn=p+qЃЌЧвИУЗДгІЮЊЗХШШЗДгІЃЌЗДгІДяЕНЦНКтЕФБъжОЪЧЃЈ ЃЉ
pC(g)+qD(g)ЃЌвбжЊn=p+qЃЌЧвИУЗДгІЮЊЗХШШЗДгІЃЌЗДгІДяЕНЦНКтЕФБъжОЪЧЃЈ ЃЉ
ЂйЬхЯЕЕФбЙЧПВЛдйИФБф ЂкЦјЬхЕФУмЖШВЛдйИФБф
ЂлИїЦјЬхЕФХЈЖШВЛдйИФБф ЂмИїЦјЬхЕФжЪСПЗжЪ§ВЛдйИФБф
ЂнЗДгІЫйТЪv(C)ЁУv(D)=pЁУq
ЂоЕЅЮЛЪБМфФкnmol BЖЯМќЗДгІ,ЭЌЪБpmol CвВЖЯМќЗДгІ
A. ЂкЂлЂмЂо B. ЂйЂкЂлЂм C. ЂйЂкЂлЂмЂо D. ЂмЂнЂо
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com