
科目: 来源: 题型:
【题目】某化学研究性学习小组模拟工业上从浓缩的海水中提取液溴的过程,设计了如下实验装置(夹持装置略去)和操作流程。已知:![]() 的沸点为59℃,微溶于水,有毒。
的沸点为59℃,微溶于水,有毒。
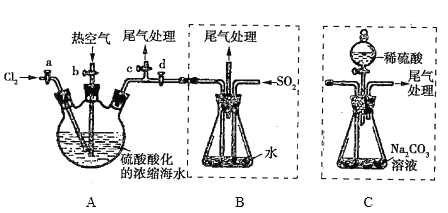
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入![]() 至反应完全;
至反应完全;
②关闭活塞a、c,打开活塞b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量![]() ;
;
④关闭活塞b,打开活塞a,再通过A向B中缓慢通人足量![]() ;
;
⑤将B中所得液体进行萃取、分液、蒸馏并收集液溴。
请回答下列问题:
(1)实验室中制备氯气的化学方程式为________________________________________________。
(2)步骤②中鼓入热空气的作用是_______________________________________。
(3)步骤③中发生的主要反应的离子方程式为_______________________________________。
(4)进行步骤③时,B中尾气可用_____(填序号)吸收处理。
a.水 b.浓硫酸 c. ![]() 溶液 d.饱和
溶液 d.饱和![]() 溶液
溶液
(5)步骤⑤中,用下图所示装置进行蒸馏,收集液溴,将装置图中缺少的主要仪器补画出来___________。
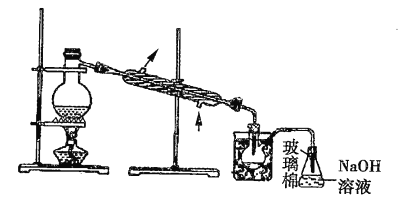
(6)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了![]() 等物质,该反应的化学方程式为_______________。
等物质,该反应的化学方程式为_______________。
(7)与B装置相比,采用C装置的优点为______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知![]() 是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中
是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中![]() 、
、![]() 、
、![]() 的组成百分率与pH的关系如图所示,下列说法正确的是( )
的组成百分率与pH的关系如图所示,下列说法正确的是( )
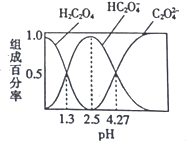
A.![]() 的溶液中:
的溶液中:![]()
B.反应![]() 的平衡常数为
的平衡常数为![]()
C.向溶液中加入KOH溶液将pH由1.3调至4.27的过程中水的电离程度先增大后减小
D.![]() 的溶液中:
的溶液中:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )


A. ①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应N2O4(g)![]() 2NO2(g) ΔH>0,平衡体系中总质量(m总)与总物质的量(n总)之比M(M=
2NO2(g) ΔH>0,平衡体系中总质量(m总)与总物质的量(n总)之比M(M=![]() )在同温度下随压强的变化曲线如图所示。下列说法正确的是:
)在同温度下随压强的变化曲线如图所示。下列说法正确的是:
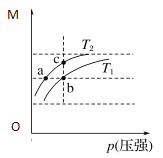
A. 温度:T1<T2
B. 平衡常数:K(a)=K(b)<K(c)
C. 反应速率:vb<va
D. 当M=69 g·mol-1时,n(NO2)∶n(N2O4)=1∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)![]() Z(g)+W(s) ΔH>0。下列叙述正确的是( )
Z(g)+W(s) ΔH>0。下列叙述正确的是( )
A. 加入少量W,逆反应速率增大,正反应速率减小 B. 升高温度,平衡逆向移动
C. 当容器中气体压强不变时,反应达到平衡 D. 反应平衡后加入X,上述反应的ΔH增大
查看答案和解析>>
科目: 来源: 题型:
【题目】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:
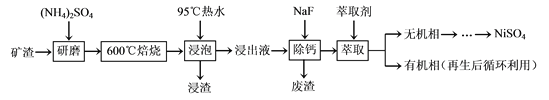
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。
(1)焙烧过程中NiFe2O4发生反应的化学方程式是___。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___,“浸渣”的成分除Fe2O3、FeO(OH)、Fe(OH)3外还含有___、___(填化学式)。
(3)“浸泡”过程中温度低于95℃,可能导致的主要问题有___(写出一点即可)。
(4)“浸出液”中c(Ca2+)=1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=___mol·L-1。[已知Ksp(CaF2)=4.0×10-11]
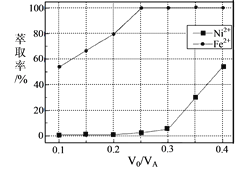
(5)本工艺中,萃取剂与溶液的体积比(![]() )对溶液中Ni2+、Fe2+的萃取率影响如图所示,
)对溶液中Ni2+、Fe2+的萃取率影响如图所示,![]() 的最佳取值是___。
的最佳取值是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
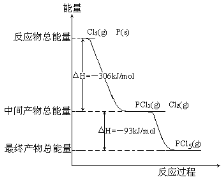
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式___。
(2)PCl5分解成PCl3和Cl2的热化学方程式___。
(3)P和Cl2分两步反应生成1molPCl5的△H3=__,P和Cl2一步反应生成1molPCl5的△H4___△H3 (填“大于”、“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】美国计划2020年再次登陆月球,并在月球上建立永久性基地,为人类登陆新的行星做好前期准备。为了解决基地人员的供氧问题,科学家设想利用月球富氧岩石制取氧气。其提氧原理是用氢气还原富氧岩石获取水,再利用太阳能电池电解水得到氢气和氧气。
玄武岩(含钛铁矿)是月球的主要岩石之一,其质地坚硬,钛铁矿的主要成分为钛酸亚铁(![]() )。用上述提氧原理,理论上,从1 kg
)。用上述提氧原理,理论上,从1 kg ![]() 中可获取105.3g
中可获取105.3g ![]() 。
。
(1)写出![]() 与
与![]() 反应的化学方程式:______________________________________________。
反应的化学方程式:______________________________________________。
(2)研究表明,月球上平均直径为40微米的小圆珠形成的堆积物(富含![]() )是最适合提氧的矿物。这种堆积物作为提氧原料的优点是____________________________________________________________。
)是最适合提氧的矿物。这种堆积物作为提氧原料的优点是____________________________________________________________。
(3)研究人员查阅文献后,得知钛铁矿在高温下还能被炭粉还原: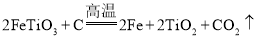 ,
,![]() 通过植物的光合作用可获得
通过植物的光合作用可获得![]() ,化光学方程式为
,化光学方程式为![]() (葡萄糖)
(葡萄糖)![]() 。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
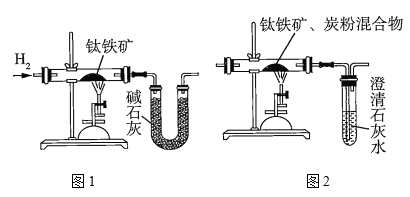
研究人员用图1装置从钛铁矿中提取氧,实验中得出的可提取氧的质量分数大于理论值,产生这种情况的原因可能是______________________;用图2装置进行实验的过程中,称得反应前钛铁矿的质量为![]() ,炭粉的质量为
,炭粉的质量为![]() ,钛铁矿完全反应后,测得生成
,钛铁矿完全反应后,测得生成![]() 的质量为
的质量为![]() ,则钛铁矿中可提取氧的质量分数为________________。
,则钛铁矿中可提取氧的质量分数为________________。
(4)在钛铁矿提氧过程中科学家们常选用![]() 而不用其他还原剂,其主要原因是______________________。
而不用其他还原剂,其主要原因是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在固定容积的密闭容器中,放入amolX,发生反应:2X![]() Y(g)+Z(s),并达到平衡状态,此时升高温度,气体的密度增大。下列叙述正确的是
Y(g)+Z(s),并达到平衡状态,此时升高温度,气体的密度增大。下列叙述正确的是
A.平衡后移走部分Z,平衡正向移动
B.若X为非气态,则正反应为放热反应
C.若正反应为放热反应,则X一定为气态
D.若X为气态,再向容器中充入amolX,达到平衡后,X的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
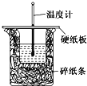
(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________,烧杯间填满碎泡沫塑料的作用是________________________。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值__(填“偏大”、“偏小”或“无影响”)。
(3)实验中若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等”或“不相等”),所求中和热的数值______(填“相等”或“不相等”),理由是_______________________________。
(4)三次平行操作测得的数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为2.3 ℃、2.4 ℃、2.9 ℃,则最终代入计算式的温度差的平均值为_____℃。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com